
【題目】化學中常用圖像直觀地描述化學反應的進程或結果。只改變一個條件,則下列對圖像的解讀正確的是
①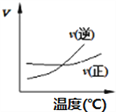 ②
②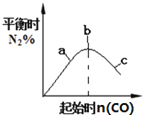 ③
③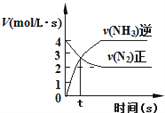 ④
④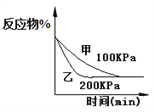
A. A2(g)+3B2(g)![]() 2AB3(g),如圖①說明此反應的正反應是吸熱反應
2AB3(g),如圖①說明此反應的正反應是吸熱反應
B. 4CO(g)+2NO2(g)![]() N2(g)+4CO2(g),如圖②說明NO2的轉化率b>a>c
N2(g)+4CO2(g),如圖②說明NO2的轉化率b>a>c
C. N2(g)+3H2(g)![]() 2NH3(g),如圖③說明t秒時合成氨反應達到平衡
2NH3(g),如圖③說明t秒時合成氨反應達到平衡
D. 2A(g)+2B(g)![]() 3C(g)+D(?),如圖④說明生成物D一定是氣體
3C(g)+D(?),如圖④說明生成物D一定是氣體
 名題訓練系列答案
名題訓練系列答案 期末集結號系列答案
期末集結號系列答案科目:高中化學 來源: 題型:
【題目】常溫下用0.1000mol/L的鹽酸分別逐滴加入到20.00mL0.1000mol/L的三種一元堿XOH、MOH、YOH溶液中,溶液的pH隨加入鹽酸體積的變化如圖所示。下列敘述錯誤的是
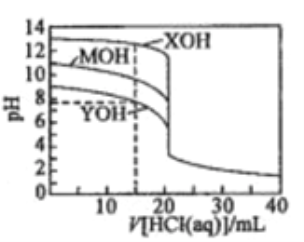
A. XOH為強堿,MOH、YOH均為弱堿
B. V[HCl(aq)]=15.00mL時,三種溶液中離子總濃度大小順序:XOH>MOH>YOH
C. V[HCl(aq)]=20.00mL時,三種溶液中水的電離程度:XOH>MOH>YOH
D. V[HCl(aq)]=40.00ml.時,YOH溶液中:c(H+)=c(Y+)+c(OH-)+2c(YOH)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是常溫下,濃度為0.01mol/L的NaOH溶液與幾種酸或鹽混合后的情況:
混合組別 | 混合前酸或鹽的總濃度 | 混合比例及混合溶液性質 |
① | c(HA)=0.02mol/L | 等體積混合,pH>7 |
② | HB溶液的pH=2 | V1mLNaOH溶液與V2mLHB溶液,pH=7 |
③ | c(H2C)=0.01mol/L | 等體積混合,pH>7 |
④ | c(NaHD)=0.01mol/L | 等體積混合,pH=7 |
回答下列問題:
(1)①組混合液中,HA、A-、Na+三種粒子濃度由大到小的順序為________,若pH=8,則c(Na+)-c(A-)=________mol/L(填具體數字)。
(2)由②組混合液pH=7可推知,V1____V2。
(3)③組混合液中,pH>7的原因是______________________。
(4)0.01mol/LNaHD溶液中,水的電離度=_________。(已知:水的電離度=[已電離的水分子的個數/水分子總數]×100%)
(5)僅憑上述結果,一定能確定HA、HB、H2C、H2D四種酸中屬于弱酸的是_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】幾種物質在酸性溶液中的還原性強弱順序如下:SO2>I->Fe2+>H2O2。據此判斷下列反應不能發生的是
A. 2Fe3++SO2+2H2O=2Fe2++SO![]() +4H+
+4H+
B. H2O2+H2SO4=SO2↑+O2↑+2H2O
C. SO2+I2+2H2O=H2SO4+2HI
D. 2Fe3++2I-=2Fe2++I2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】W、X、Y、Z是短周期元素,W的一種同位素無中子,X的單質在空氣中含量約占78%,Y的單質在空氣中燃燒發出耀眼白光,Z的單質用于工業制漂白粉。下列說法錯誤的是
A. W和X形成的化合物中可能既存在極性鍵,又存在非極性鍵
B. 含氧酸的酸性Z一定大于X
C. 工業上采取電解熔融Y和Z化合物的方法冶煉Y
D. W和X的化合物與W和Z的化合物反應可產生白煙
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列離子方程式錯誤的是
A. 鹽酸與燒堿溶液反應:H++OH-===H2O
B. 澄清石灰水中通入CO2變渾濁:CO2+Ca2++2OH-===CaCO3↓+H2O
C. 向氯化鋁溶液中加入足量氨水:Al3++3OH-===Al(OH)3↓
D. Cl2與水反應生成鹽酸和次氯酸:Cl2+H2O![]() H++Cl-+HClO
H++Cl-+HClO
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學探究小組設計實驗探究某種氮的化合物的制備及性質。
【探究一】下圖A為某氣體制備裝置,圖中未畫出。
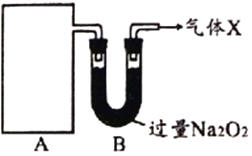
據此回答:
(1)①只用一種試劑制備A中某氣體,選取的試劑是____________。
a.NH4HCO3 b.NH4Cl c.Ca(OH)2 d.NH4NO3
②裝置A所用的主要玻璃儀器是____________(填儀器名稱)。
(2)從裝置A進入裝置B的物質在B中被充分吸收,寫出B中發生反應的化學方程式_______________________________(寫出一個即可)。
【探究二】為探究上述裝置中產生的氣體性質,該化學探究小組又組裝了如下裝置,其中C處硬質試管中裝有紅色粉末銅粉。
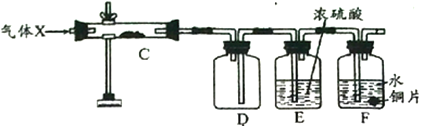
用酒精燈加熱C處硬質試管一段時間后,再通入上述實驗產生的氣體,過一會撤去C處酒精燈。
據此回答:
(3)若實驗過程中發現F處銅片逐漸溶解。則:
①D中觀察到的現象是________________________________。
②C中發生反應的化學方程式為________________________________。
③F處銅片逐漸溶解的原因是________________________________。
④該裝置的不足之處是________________________________。
(4)若實驗過程中F處銅片沒有任何變化,D中無任何現象發生,只觀察到C中粉末在紅色和黑色間交替變化。則C中發生反應的化學方程式為________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】黨的十八大以來,我國在科技創新和重大工程建設方面取得了豐碩成果,在新時代更需要新科技創新世界。2018年3月5日,《自然》連刊兩文報道石墨烯超導重大發現,第一作者均為中國科大10級少年班現年僅21歲的曹原。曹原團隊在雙層石墨烯中發現新的電子態,可以簡單實現絕緣體到超導體的轉變。石墨烯是一種由碳原子組成六角形呈蜂巢晶格的二維碳納米材料(如圖甲),石墨烯中部分碳原子被氧化后,其平面結構會發生改變,轉化為氧化石墨烯(如圖乙)。
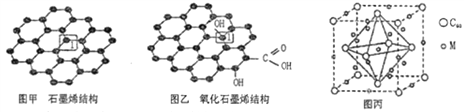
(1)圖甲中,1號C與相鄰C形成σ鍵的個數為__________。
(2)圖乙中,1號C的雜化方式是__________,該C與相鄰C形成的鍵角__________(填“>”、“<”或“=”)圖甲中1號C與相鄰C形成的鍵角。
(3)我國制墨工藝是將50nm左右的石墨烯或氧化石墨烯溶于水,在相同條件下所得到的分散系后者更為穩定,其原因是____________________。
(4)石墨烯可轉化為富勒烯(C60),某金屬M與C60可制備一種低溫超導材料,晶胞如圖丙所示,M原子位于晶胞的棱心與內部。該晶胞中M原子的個數為____________,該材料的化學式為_______________。
(5)金剛石與石墨都是碳的同素異形體。若碳原子半徑為r,金剛石晶胞的邊長為a,根據硬球接觸模型,金剛石晶胞中碳原子的空間占有率為___________。
(6)一定條件下,CH4、CO2都能與H2O形成籠狀結構(如下圖所示)的水合物晶體,其相關參數見下表。CH4與H2O形成的水合物晶體俗稱“可燃冰”。
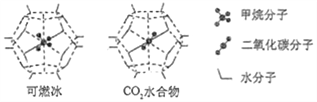
①“可燃冰”中分子間存在的2種作用力是___________________________;
②為開采深海海底的“可燃冰",有科學家提出用CO2置換CH4的設想。已知上圖中籠狀結構的空腔直徑為0.586nm,結合圖表從物質結構及性質的角度分析,該設想的依據是:___________________。
參數 分子 | 分子直徑/nm | 分子與H2O的結合能E/(kJ·mol-1) |
CH4 | 0.436 | 16.40 |
CO2 | 0.512 | 29.91 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com