
(1)在3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O反應中,_______是氧化劑;_______是還原劑;_______元素被氧化;_______元素被還原;______是氧化產物;_______是還原產物,被還原的HNO3與參加反應的HNO3物質的量之比是___ __。用雙線橋標出該反應電子轉移的方向和數目。
(2)雙線橋標出反應KClO3+ 6HCl=KCl + 3 Cl2↑ + 3H2O電子轉移的方向和數目。(2分)
(11分)(1)HNO3;Cu ;Cu;N;Cu(NO3)2;NO ,1:4(每空1分,共7分)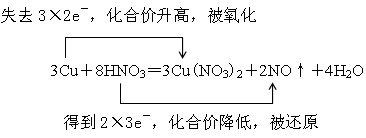 ((2分)
((2分)
(2)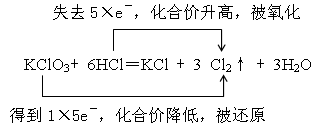 (2分)
(2分)
解析試題分析:(1)在3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O反應中銅元素的化合價從0價升高到+2價,失去2個電子,被氧化,作還原劑,硝酸銅是氧化產物;硝酸中N元素的化合價從+5價降低到+2價,得到3個電子,被還原,硝酸是氧化劑,氮氣是還原產物。根據反應的方程式可知被還原的HNO3與參加反應的HNO3物質的量之比是2:8=1:4;根據電子得失守恒可知,其電子轉移的方向和數目可表示為 。
。
(2)在反應KClO3+ 6HCl=KCl + 3 Cl2↑ + 3H2O,氯化氫中氯元素的化合價從-1價升高到0價,失去1個電子。氯酸鉀中氯元素的化合價從+5價降低0價,得到5個電子,則根據電子得失守恒可知,其電子轉移的方向和數目可表示為 。
。
考點:考查氧化還原反應的有關判斷、表示


 小學課時作業全通練案系列答案
小學課時作業全通練案系列答案 金版課堂課時訓練系列答案
金版課堂課時訓練系列答案科目:高中化學 來源: 題型:填空題
甲、乙兩同學研究Na2SO3溶液與FeCl3溶液反應的情況。
| 步驟 | 操作 | 現象 |
| I | 向2 mL 1 mol·L-1FeCl3溶液中加入一定量的Na2SO3溶液 | 溶液由棕黃色變為紅褐色, 并有少量刺激性氣味的氣體逸出 |
 SO32- +
SO32- + =
= F e2+ +
F e2+ + +
+

| 1.Fe2+與SO32-反應生成墨綠色的絮狀沉淀FeSO3; 2.墨綠色的FeSO3與黃色的FeCl3溶液混合后,溶液呈紅褐色。 |
| 步驟 | 操作 | 現象 |
| II | 用激光筆照射步驟I中的紅褐色溶液 | 出現“丁達爾效應” |
| 步驟 | 操作 | 現象 |
| III | 向1 mol?L-1的FeCl3溶液中通入一定量的SO2 | 溶液由黃色變為紅褐色 |
| IV | 用激光筆照射步驟III中的紅褐色溶液 | 沒有出現“丁達爾效應” |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
肼(N2H4)是火箭發射常用的燃料。
(1)最新實驗研究用肼還原新制Cu(OH)2可制備納米級Cu2O,同時放出N2。請寫出該制法的化學反應方程式____________________________,當反應中轉移0.2 mol電子 時,可制得Cu2O的質量為__________。
(2)一種以肼(N2H4)為燃料的電池裝置如圖所示。該燃料電池的電極材料采用多孔導電材料,以提高電極反應物在電極表面的吸附量,并使它們與電解質溶液充分接觸,以空氣中的氧氣作為氧化劑,KOH溶液作為電解質。負極上發生的電極反應為_________________; ②電池工作時產生的電流從_______電極經過負載后流向________電極(填“左側”或“右側”)。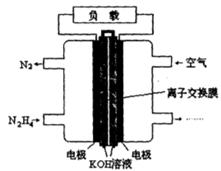
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(1)用甲烷制氫是一種廉價的制氫方法。有關的熱化學方程式如下:
CH4(g)+1/2O2(g)  CO(g)+2H2(g);△H= -36kJ/mol……… ①
CO(g)+2H2(g);△H= -36kJ/mol……… ①
CH4(g)+H2O(g)  CO(g)+3H2(g);△H= +216kJ/mol…………②
CO(g)+3H2(g);△H= +216kJ/mol…………②
①下列說法正確的是 ____
| A.2H2O(l)=2H2(g)+O2(g) △H=+504kJ/mol |
| B.當反應①中υ(CH4)正=υ(CO)正時,表明該反應達平衡狀態 |
| C.其它條件不變時,增大體系壓強,反應①②中甲烷的轉化率均增大 |
| D.為維持恒定溫度(不考慮熱量損失),某反應器中同時發生反應①與②時,消耗甲 |
 CO(g)+3H2(g)。當甲烷的轉化率為0.5時,此時平衡常數為 _______
CO(g)+3H2(g)。當甲烷的轉化率為0.5時,此時平衡常數為 _______ 3Na2FeO2+H2O+NH3↑…………①;
3Na2FeO2+H2O+NH3↑…………①;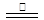 4Na2Fe2O4+3NH3↑……②;
4Na2Fe2O4+3NH3↑……②;查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(1)粗鹽中常含有泥沙和Ca2+、Mg2+、Fe3+、SO2-4等雜質,必須精制后才能供電解使用。精制時,粗鹽溶于水過濾后,還要加入的試劑分別為①Na2CO3、②HCl(鹽酸)③BaCl2,這3種試劑添加的合理順序是______________(填序號
(2)工業生產硫酸時,利用催化氧化反應將SO2轉化為SO3是一個關鍵步驟。選擇適宜的催化劑,是否可以提高SO2的轉化率? (填“是”或“否”),是否可以增大該反應所放出的熱量? (填“是”或“否”);
(3)氮化硅(Si3N4)是一種新型陶瓷材料,它可由石英與焦碳在高溫的氮氣流中,通過以下反應制得: SiO2 + C + N2 = Si3N4 + CO)
①配平上述反應的化學方程式
②該反應的平衡常數表達式為K=
(4)水是一種重要的自然資源,天然水在凈化處理過程中加入的混凝劑可以是 __ (填兩種物質名稱),其凈水作用的原理是
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(1)已知將鹽酸滴入高錳酸鉀溶液中,產生黃綠色氣體,而溶液的紫紅色褪去。 現有一個氧化還原反應的體系中共有KCl、Cl2、H2SO4、H2O、KMnO4、MnSO4、K2SO4七種物質:
①該反應中,化合價升高的反應物是________,化合價沒有發生變化的反應物是_______。
②寫出一個包含上述七種物質的氧化還原反應方程式(不需配平) ___________。
③上述反應中,氧化劑是________,1 mol氧化劑在反應中________(填“得到”或“失去”)________mol電子。
④如果在反應后的溶液中加入NaBiO3,溶液又變紫紅色。說出NaBiO3的一個性質:___________________________________________________________________。
(2)某反應體系中的物質有:NaOH、Au2O3、Na2S4O6、Na2S2O3、Au2O、H2O。
①將氧化劑與還原劑填入下列空格中,并標出電子轉移的方向和數目。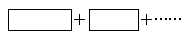
反應中,被還原的元素是________,氧化產物是______________。
②紡織工業中常用氯氣作漂白劑,Na2S2O3可作為漂白布匹的“脫氯劑”,Na2S2O3和Cl2反應的產物是H2SO4、NaCl和HCl,則還原劑與氧化劑的物質的量之比為________。
(3)一定條件下,向廢水中加入CH3OH,將HNO3還原成N2。若該反應消耗3.2 g CH3OH轉移0.6 mol電子,則氧化產物為(填化學式),氧化產物與還原產物的物質的量之比是________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
近年來,地震、洪水、泥石流等各種自然災害頻發,災害過后,對環境進行消毒殺菌、獲取潔凈的飲用水都需要大量消毒劑,開發具有廣譜、高效、低毒的殺菌、消毒劑是今后發展的趨勢。
(1)Cl2、H2O2、ClO2(還原產物為Cl-)、O3(1 mol O3轉化為1 mol O2和1 mol H2O)常被用作消毒劑。等物質的量的上述物質中消毒效率最高的是 (填序號)。
A.Cl2 B.H2O2 C. O3 D.ClO2
(2)過氧乙酸(CH3COOOH)是一種多用途的新型液體消毒殺菌劑, 它具有CH3COOH 和H2O2的雙重性質。下列物質與過氧乙酸混合,不會使過氧乙酸失效的是 (填序號)。
A.FeCl3 B.KMnO4溶液 C.稀鹽酸 D.NaHCO3溶液
(3)消毒試劑亞氯酸鈉(NaClO2)在常溫與黑暗處可保存一年。亞氯酸不穩定可分解,反應的離子方程式為:HClO2―→ClO2↑+H++Cl-+H2O(未配平)。在該反應中,當有1 mol ClO2生成時,轉移的電子數是 。
(4)氯氨(NH2Cl)可作殺菌劑,請用化學方程式表示氯氨在水中的殺菌機理: .
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(1)用“單線橋”表示下列反應電子轉移的方向和數目:2KMnO4 + 16HCl=" 2KCl" + 2MnCl2 + 5Cl2↑+ 8H2O 反應中物質的氧化性:KMnO4_____ Cl2(填“>、<、=”);氧化產物與還原產物的物質的量之比為_____________。
(2)配平下列氧化還原反應方程式:___KMnO4+___H2S+__H2SO4(稀) —— __K2SO4+__MnSO4+__S↓+__H2O
(3)Cl2是一種黃綠色有毒氣體,化工廠可用濃氨水來檢驗有毒氣體Cl2是否泄漏,有關反應的化學方程式為:3Cl2+8NH3=6NH4Cl +N2若反應中NH3消耗6.8 g,則轉移電子個數為 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
寫出下列反應的化學方程式,并指出氧化劑和還原劑。
(1)鋰在空氣中燃燒
(2)鉀與水反應
(3)鎂條在二氧化碳氣體中燃燒
(4)曾青得鐵則化為銅——濕法煉銅
(5)從赤鐵礦中提煉鐵——工業冶鐵
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com