
【題目】制備鋅印刷電路板是用稀硝酸腐蝕鋅板產生的廢液稱“爛板液”。“爛板液”中除含硝酸鋅外,還含有自來水帶入的Cl-和Fe3+,在實驗室里,用“爛板液制取ZnSO47H2O的過程如圖所示
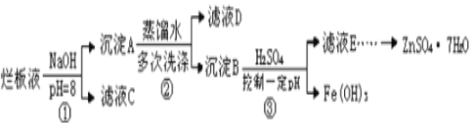
(1)若稀硝酸腐蝕鋅板時還原產物為N2O,氧化劑與還原劑的物質的量之比是____。
(2)若步驟①的pH>12,則Zn(OH) 2溶解生成四羥基合鋅酸鈉,Zn(OH) 2溶解的離子方程式為_____。
(3)濾液D中除了含有OH-離子外,還含有的陰離子有___________(填離子符號)。
(4)若濾液E的pH=4,c(Zn2+)=2mol·L-1,c(Fe3+)=2.6×10-9mo·L-l試求出Fe(OH)3的溶度積常數__(只需寫出結果即可)。
(5)已知:①Fe(OH)3(s) Fe3+(aq)+3OH-(aq)H=a kJ mol·L-1②H2O(l) H+(aq)+OH-(aq)H=b kJ·mol·L-1,若①的溶度積常數為Ksp,②的離子積常數為Kw,Fe3+發生水解反應的平衡常數:K=____(用含Kw、Ksp的代數式表示)。
【答案】1:2 Zn(OH)2+2OH=[Zn(OH)4]2 Cl、NO3 2.6×10-39 ![]()
【解析】
根據實驗目的及流程圖分析各步發生的反應及沉淀組成,書寫相關反應離子方程式;根據電離及水解原理,運用平衡常數表達式進行相關計算。
因為廢液是用稀硝酸腐蝕鋅板后得到的,所以廢液中含有大量的鋅離子、氫離子、硝酸根離子和少量的Cl、Fe3+,加入氫氧化鈉調節溶液的pH=8使鐵離子、鋅離子完全沉淀,然后在沉淀B中加硫酸并控制pH,使氫氧化鐵沉淀,鋅離子溶解得到硫酸鋅溶液,最終得到硫酸鋅晶體;
(1)若稀硝酸腐蝕鋅板時還原產物為N2O,則反應的方程式為4Zn+10HNO3=4Zn(NO3)2+N2O↑+5H2O,由方程式可知反應中HNO3為氧化劑,Zn為還原劑,當4molZn參加反應時,有2molHNO3被還原,則氧化劑與還原劑的物質的量之比1:2,故答案為:1:2;
(2)Zn(OH)2溶解生成四羥基合鋅酸鈉,反應的離子方程式為Zn(OH)2+2OH=[Zn(OH)4]2,
故答案為:Zn(OH)2+2OH=[Zn(OH)4]2;
(3)固體具有吸附性,沉淀A可吸附溶液中的Cl、NO3等離子,則濾液中應含有Cl、NO3,故答案為:Cl、NO3;
(4)若濾液E的pH=4,則c(OH-)=1×10-10mo·L-l,得到的沉淀為Fe(OH)3,則Fe(OH)3的溶度積常數為:![]() ,故答案為:2.6×10-39;
,故答案為:2.6×10-39;
(5)Fe3+發生水解反應的方程式為Fe3++3H2O![]() Fe(OH)3+3H+,已知①Fe(OH)3(s) Fe3+(aq)+3OH-(aq)
Fe(OH)3+3H+,已知①Fe(OH)3(s) Fe3+(aq)+3OH-(aq)![]() , ②H2O(l) H+(aq)+OH-(aq)
, ②H2O(l) H+(aq)+OH-(aq) ![]() ,則②×3①可得Fe3+(aq)+3H2O(l)Fe(OH)3(aq)+3H+(aq),則Fe3+發生水解反應的平衡常數為:
,則②×3①可得Fe3+(aq)+3H2O(l)Fe(OH)3(aq)+3H+(aq),則Fe3+發生水解反應的平衡常數為:![]() ,故答案為:
,故答案為:![]() 。
。


 七星圖書口算速算天天練系列答案
七星圖書口算速算天天練系列答案 初中學業考試導與練系列答案
初中學業考試導與練系列答案科目:高中化學 來源: 題型:
【題目】根據下列提供的一組物質回答問題:
①NH4Cl ②MgCl2 ③H2S ④Na2O2 ⑤MgO ⑥Cl2 ⑦NaOH
(1)僅含有共價鍵的是_________;既有離子鍵又有共價鍵的是_________(用序號表示)
(2)離子化合物有_____________________;(用序號表示)
(3)Na2O2 的電子式_____________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖,在注射器中加入少量Na2SO3晶體,并吸入少量濃硫酸(以不接觸紙條為準).則下列有關說法正確的是( )
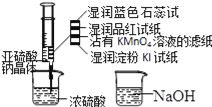
A. 濕潤淀粉碘化鉀試紙未變藍說明硫元素的非金屬性強于碘元素
B. 沾有KMnO4溶液的濾紙褪色證明了SO2具有漂白性
C. 實驗后,可把注射器中的物質緩緩推入NaOH溶液中,以減少環境污染
D. 藍色石蕊試紙變紅說明SO2顯酸性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】亞氯酸鈉(NaClO2)用于漂白織物、纖維、紙漿,具有對纖維損傷小的特點.其在溶液中可生成ClO2、HClO2、ClO2﹣、Cl﹣等,其中HClO2和ClO2都具有漂白作用.已知pOH=﹣lgc(OH﹣),經測定25℃時各組分含量隨pOH變化情況如圖所示(Cl﹣沒有畫出),此溫度下,下列分析正確的是
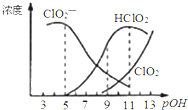
A.HClO2的電離平衡常數的數值Ka=10﹣6
B.亞氯酸鈉在酸性條件下較穩定
C.pH=7時,溶液中含氯微粒的濃度大小為:c(HClO2)>c(ClO2﹣)>c(ClO2)>c(Cl﹣)
D.同濃度的HClO2溶液和NaClO2溶液等體積混合,則混合溶液中有c(HClO2)-2c(H+)=c(ClO2﹣)-2c(OH﹣)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一個絕熱的、容積固定的密閉容器中,發生可逆反應mA(g)+nB(g)![]() pC(g)+qD(g)(m、n、p、q為任意正整數)。下列能說明該可逆反應達到平衡狀態的是( )
pC(g)+qD(g)(m、n、p、q為任意正整數)。下列能說明該可逆反應達到平衡狀態的是( )
①混合氣體的密度不再發生變化 ②體系的溫度不再發生變化 ③A的轉化率不再改變 ④各組分的百分含量不再改變 ⑤反應速率v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q
A. ②③④B. ①③⑤C. ②④⑤D. ①②③④⑤
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】今年是門捷列夫發現元素周期律150周年。下表是元素周期表的一部分,W、X、Y、Z為短周期主族元素,W與X的最高化合價之和為8。下列說法錯誤的是

A. 原子半徑:W<X
B. 常溫常壓下,Y單質為固態
C. 氣態氫化物熱穩定性:Z<W
D. X的最高價氧化物的水化物是強堿
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應中,電子轉移發生在同種物質的同種元素之間的是( )
A. 2H2S+SO2=3S+2H2OB. 2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
C. 2KClO3![]() 2KCl+3O2↑D. Cu2O+H2SO4=CuSO4+Cu+H2O
2KCl+3O2↑D. Cu2O+H2SO4=CuSO4+Cu+H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】高分子材料PET聚酯樹脂和PMMA的合成路線如下圖:
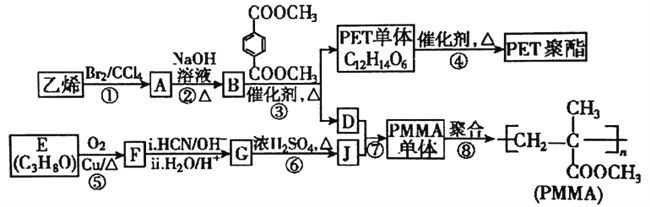
已知:
I.RCOOR+R "OH![]() RCOOR "+ROH (R.R'、R"代表烴基)
RCOOR "+ROH (R.R'、R"代表烴基)
II.  (R代表烴基)。
(R代表烴基)。
(1)PMMA單體的結構簡式為_______,PET單體中的官能團名稱為________。
(2)反應⑤的反應類型是________;反應②的化學方程式為_________。
(3)若反應④得到的某一條鏈狀產物聚合度為n,則縮聚反應中脫去的小分子有(___)個。
(4)PMMA單體有多種同分異構體,某種異構體K具有如下性質:①不能發生銀鏡反應②不能使溴水褪色③分子內沒有環狀結構④核磁共振氫譜有面積比為3:1的兩種峰,則K的結構簡式為:__________;另一種異構體H含有醛基、羥基和碳碳雙鍵,在銅催化下氧化,官能團種類會減少一種,則H合理的結構共有___種(不考慮立體異構和空間異構)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:① CH3CH=CHCH2CH3![]() CH3COOH+CH3CH2COOH
CH3COOH+CH3CH2COOH
② R-CH=CH2![]() R-CH2-CH2-Br
R-CH2-CH2-Br
香豆素的核心結構是芳香內酯A,A經下列步驟轉變為水楊酸。
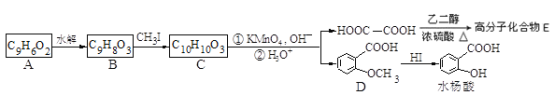
請回答下列問題:
(1)下列有關A、B、C的敘述中不正確的是___________
a. C中核磁共振氫譜共有8種峰
b. A、B、C均可發生加聚反應
c. 1mol A最多能和5mol氫氣發生加成反應
d. B能與濃溴水發生取代反應
(2)B分子中有2個含氧官能團,分別為______和______(填官能團名稱),B→C的反應類型為_____________。
(3)在上述轉化過程中,反應步驟B→C的目的是_________________________。
(4)化合物D有多種同分異構體,其中一類同分異構體是苯的對二取代物,且水解后生成的產物之一能發生銀鏡反應。請寫出其中一種的結構簡式:_____________。
(5)寫出合成高分子化合物E的化學反應方程式:_______________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com