
【題目】恒溫條件下,可逆反應:2NO(g)+O2(g)![]() 2NO2(g)在體積固定的密閉容器中進行,達到平衡狀態的標志的是( )
2NO2(g)在體積固定的密閉容器中進行,達到平衡狀態的標志的是( )
①單位時間內生成n mol O2的同時生成2n mol NO2②單位時間內生成n mol O2的同時生成2n mol NO③用NO2、NO、O2表示的反應速率的比為2:2:1的狀態④混合氣體的顏色不再改變的狀態⑤混合氣體的密度不再改變的狀態⑥混合氣體的壓強不再改變的狀態⑦混合氣體的平均相對分子質量不再改變的狀態.
A. ①④⑥⑦ B. ②③⑤⑦ C. ①③④⑤ D. 全部
【答案】A
【解析】試題分析:可逆反應達到平衡狀態時,正逆反應速率相等(同種物質)或正逆反應速率之比等于系數之比(不同物質),平衡時各種物質的物質的量、濃度等不再發生變化,由此衍生的一些物理量不變,以此分析。①υ(NO2)正=2υ(O2)逆,證明正逆反應速率相等,化學反應達到了平衡狀態,故正確;②υ(NO)正=2υ(O2)正,只能體現反應的正反應方向,不能證明正逆反應速率相等,化學反應不一定達到了平衡狀態,故錯誤;③化學反應進行到任何程度,化學反應速率之比均等于方程式的系數之比,所以用NO2、NO、O2表示的反應速率的比為2:2:1的狀態不一定是平衡狀態,故錯誤;④混合氣體顏色不再改變,證明二氧化氮的濃度不隨時間的改變而改變,證明達到了平衡狀態,故正確;⑤混合氣體密度ρ=![]() ,質量在反應前后是守恒的,體積保持不變,所以密度自始至終都不變,所以混合氣體密度不改變的狀態不一定是平衡狀態,故錯誤;⑥反應是一個前后氣體系數和變化的反應,當混合氣體壓強不再改變的狀態是平衡狀態,故正確;⑦混合氣體平均相對分子質量M=
,質量在反應前后是守恒的,體積保持不變,所以密度自始至終都不變,所以混合氣體密度不改變的狀態不一定是平衡狀態,故錯誤;⑥反應是一個前后氣體系數和變化的反應,當混合氣體壓強不再改變的狀態是平衡狀態,故正確;⑦混合氣體平均相對分子質量M=![]() ,質量在反應前后是守恒的,反應是一個前后氣體系數和變化的反應,即n是變化的,所以M不變證明反應達到了平衡狀態,故正確,故選A。
,質量在反應前后是守恒的,反應是一個前后氣體系數和變化的反應,即n是變化的,所以M不變證明反應達到了平衡狀態,故正確,故選A。


 口算小狀元口算速算天天練系列答案
口算小狀元口算速算天天練系列答案 天天練口算系列答案
天天練口算系列答案科目:高中化學 來源: 題型:
【題目】某溫度時,在一個容積為2 L的密閉容器中,X、Y、Z三種物質的物質的量隨時間的變化曲線如圖所示。根據圖中數據,試填寫下列空白:

(1)該反應的化學方程式為_____________________。
(2)反應開始至2 min,氣體Z的平均反應速率為______________。
(3)若X、Y、Z均為氣體,反應達到平衡時:

①壓強是開始時的_________倍;
②若此時將容器的體積縮小為原來的![]() 倍,達到平衡時,容器內溫度將升高(容器不與外界進行熱交換),則該反應的正反應為_______反應(填“放熱”或“吸熱”)。
倍,達到平衡時,容器內溫度將升高(容器不與外界進行熱交換),則該反應的正反應為_______反應(填“放熱”或“吸熱”)。
(4)若上述反應在2 min后的t1~t6內反應速率與反應時間圖象如下,在每一時刻均改變一個影響反應速率的因素,則(_____)
A.在t1時增大了壓強
B.在t3時加入了催化劑
C.在t4時降低了溫度
D. t2~t3時X的轉化率最高
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對于2X(g)![]() Y(g)的體系,在壓強一定時,平衡體系中Y的質量分數w(Y)隨溫度的變化情況如圖所示(實線上的任何一點為對應溫度下的平衡狀態)。
Y(g)的體系,在壓強一定時,平衡體系中Y的質量分數w(Y)隨溫度的變化情況如圖所示(實線上的任何一點為對應溫度下的平衡狀態)。

(1)該反應的正反應方向是一個________反應(“吸熱”或“放熱”)。
(2)A、B、C、D、E各狀態中,v正<v逆的點是____________。
(3)維持t1不變,E→A所需時間為x,維持t2不變,D→C所需時間為y,則x ______ y(填“<”、“>”或“=”)。
(4)欲使E狀態從水平方向到C狀態后,再沿平衡曲線到達A狀態,從理論上來講,可選用的條件是____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知在25℃,101kPa下,16g氣態CH4充分燃燒生成液態水時放出890kJ熱量.請計算:
(1)112LCH4(標準狀況)在25℃,101kPa下,充分燃燒生成液態水時放出的熱量;
(2)上述過程中同時產生二氧化碳的體積(標準狀況).
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應中,屬于離子反應,同時又屬于有顏色變化的氧化還原反應的是( )
A. 氫氣和氯氣混合點燃
B. 氯化鋇溶液和硫酸溶液混合
C. 把銅放入硫酸汞溶液中
D. 氯化鐵溶液與氫氧化鈉溶液反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知熱化學方程式:
① C2H2(g) +5/2O2(g) == 2CO2(g)+H2O(l) ΔH1=-1301.0 kJmol-1
② C(s)+ O2(g) == CO2(g) △H2=-393.5 kJmol-1
③ H2(g)+ ![]() O2(g) == H2O(1) △H3 = -285.8 kJ·mol-1
O2(g) == H2O(1) △H3 = -285.8 kJ·mol-1
則反應④ 2C(s)+ H2(g) == C2H2(g)的△H為( )
A. +228.2 kJ·mol-1 B. -228.2 kJ·mol-1
C. +1301.0 kJ·mol-1 D. +621.7 kJ·mol-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各組物質的分類都正確的是(括號里的是類別)
A. 空氣(混合物)、C2H5OH(醇)、H2SO4(離子化合物)、CO2(非電解質)
B. 液氨(氫化物)、NH4Cl(銨鹽)、HNO3(含氧酸)、NaOH(強電解質)
C. HCl(共價化合物)、CH3COOH(羧酸)、Na2O2(堿性氧化物)、CH3I(鹵代烴)
D. NO2(酸性氧化物)、CH3CHO(有機物)、CO(有機物)、CH3COOCH3(酯)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定量混合氣體在密閉容器中發生如下反應:mA(g)+nB(g) ![]() pC(g),達到平衡后,溫度不變,將氣體體積壓縮到1/2,當達到平衡時C的濃度為原來的1.9倍,則下列敘述正確的是( )
pC(g),達到平衡后,溫度不變,將氣體體積壓縮到1/2,當達到平衡時C的濃度為原來的1.9倍,則下列敘述正確的是( )
A. m+n>p B. A的轉化率增加
C. 平衡向逆反應方向移動 D. C的體積分數增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對溫室氣體二氧化碳的研究一直是科技界關注的重點。
I.在催化劑存在下用H2還原CO2是解決溫室效應的重要手段之一,相關反應如下:
主反應:CO2(g)+4H2(g)=CH4(g)+2H2O(g)
副反應:CO2(g)+H2(g)=CO(g)+H2O(g)
(1)工業上提高甲烷反應選擇性的關鍵因素是____________。
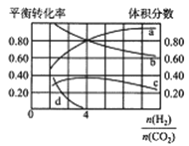
(2)T℃時,若在體積恒為2L的密閉容器中同時發生上述反應,將物質的量之和為5mol的H2和CO2以不同的投料比進行反應,結果如圖所示。若a、b表示反應物的轉化率,則表示H2轉化率的是____________,c、d分別表示CH4(g)和CO(g)的體積分數,由圖可知![]() =____________時,甲烷產率最高。
=____________時,甲烷產率最高。
Ⅱ.CO2加氫合成低碳烯烴的技術在節能減排等方面具有重要意義,由CO2和H2合成CH3OH的反應如下:CO(g)+3H2(g)=CH3OH(g)+H2O(g) △H,在10L的恒容密閉容器中投入1molCO2和2.75molH2,在不同條件下發生上述反應,測得平衡時甲醇的物質的量隨溫度、壓強的變化如圖所示。
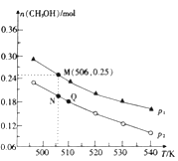
(3)判斷P1____________P2 (填“大于”、“小于”或“等于”)
說明理由_____________________________________。
(4)經測定Q點時容器的壓強是反應前壓強的9/10,若反應從開始到平衡所需的時間為5min,則05min內H2的反應速率v(H2)=____________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com