
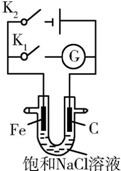
| A. | K1閉合,鐵棒上發生的反應為2H++2e-═H2↑ | |
| B. | K1閉合,石墨棒周圍溶液的pH逐漸降低 | |
| C. | K2閉合,鐵棒不會被腐蝕,屬于犧牲陽極的陰極保護法 | |
| D. | K2閉合,電路中通過0.002NA個電子時,兩極共產生0.002 mol氣體 |
分析 A.K1閉合,該裝置是原電池,中性條件下,鐵發生吸氧腐蝕,Fe易失電子生成亞鐵離子而作負極;
B.K1閉合,該裝置是原電池,中性條件下,Fe發生吸氧腐蝕,Fe作負極、C作正極,正極上氧氣得電子和水反應生成OH-;
C.K2閉合,該裝置是電解池,C作陽極、Fe作陰極,Fe被保護,屬于外加電源的陰極保護法;
D.K2閉合,該裝置是電解池,C作陽極、Fe作陰極,Fe被保護,陽極上Cl-放電生成氯氣、陰極上水得電子生成氫氣和OH-,根據電極反應式計算生成氣體物質的量.
解答 解:A.K1閉合,該裝置是原電池,中性條件下,鐵發生吸氧腐蝕,Fe易失電子生成亞鐵離子而作負極,負極反應式為Fe-2e-=Fe2+、正極反應式為O2+4e-+2H2O=4OH-,故A錯誤;
B.K1閉合,該裝置是原電池,中性條件下,Fe發生吸氧腐蝕,Fe作負極、C作正極,正極反應式為O2+4e-+2H2O=4 OH-,正極附近有OH-生成導致溶液pH增大,故B錯誤;
C.K2閉合,該裝置是電解池,C作陽極、Fe作陰極,Fe被保護,因為有外加電源,所以屬于外加電源的陰極保護法,故C錯誤;
D.K2閉合,該裝置是電解池,C作陽極、Fe作陰極,Fe被保護,陽極上Cl-放電生成氯氣、陰極上水得電子生成氫氣和OH-,陽極反應式為2Cl--2e-=Cl2↑、陰極反應式為2H2O+2e-=H2↑+2OH-,根據電極反應式知,電路中通過0.002NA個電子即0.002mol電子,陽極上生成n(Cl2)=$\frac{0.002mol}{2}×1$=0.001mol,陰極上生成n(H2)=$\frac{0.002mol}{2}×1$=0.001mol,所以兩個電極共產生0.002mol氣體,故D正確;
故選D.
點評 本題考查原電池和電解池原理,為高頻考點,明確原電池和電解池根本根本及各個電極上發生的反應是解本題關鍵,會正確書寫電極反應式,題目難度不大.


 新課標快樂提優暑假作業陜西旅游出版社系列答案
新課標快樂提優暑假作業陜西旅游出版社系列答案 暑假銜接培優教材浙江工商大學出版社系列答案
暑假銜接培優教材浙江工商大學出版社系列答案 欣語文化快樂暑假沈陽出版社系列答案
欣語文化快樂暑假沈陽出版社系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
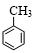 +3HNO3$→_{△}^{濃硫酸}$
+3HNO3$→_{△}^{濃硫酸}$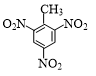 +3H2O.
+3H2O.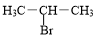 +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$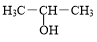 +NaBr.
+NaBr.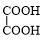 +
+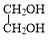 $→_{△}^{催化劑}$
$→_{△}^{催化劑}$ +2H2O.
+2H2O.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 正極有 O2 逸出 | |
| B. | 銅片上有 H2 逸出 | |
| C. | 電子通過導線由銅片流向鋅片 | |
| D. | 正極附近的 SO42- 離子濃度逐漸增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
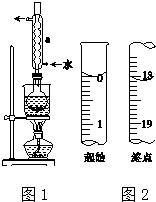 Na2S2O3是重要的化工原料,易溶于水,在中性或堿性環境中穩定.
Na2S2O3是重要的化工原料,易溶于水,在中性或堿性環境中穩定.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | SO2具有還原性,可用于蔗糖脫色 | |
| B. | 雙氧水具有強氧化性,可用于殺菌消毒 | |
| C. | 鐵粉表面積大,可用作食品干燥劑 | |
| D. | SiO2具有導電性,可用于制造光導纖維 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 金屬鈉著火時使用泡沫滅火器滅火 | |
| B. | 明礬常用于水體的凈化、殺菌和消毒 | |
| C. | 熱的純堿溶液去污效果更好 | |
| D. | 84消毒液與潔廁靈混合后用于清潔洗手間的效果更好 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com