
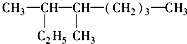
| m |
| M |
| ||
|
| 1120 |
| 770 |
| 11g |
| 22g |
| 11g |
| 22g |
| 26.5g |
| 106g/mol |
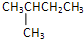 、
、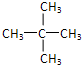 ;其核磁共振氫譜圖中顯示三種峰且面積之比為6:4:1,說明一氯戊烷的分子中含有3種等效H,其中氫原子個數之比為6:4:1,滿足該條件的一氯戊烷的結構簡式為:
;其核磁共振氫譜圖中顯示三種峰且面積之比為6:4:1,說明一氯戊烷的分子中含有3種等效H,其中氫原子個數之比為6:4:1,滿足該條件的一氯戊烷的結構簡式為: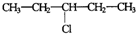 ;
;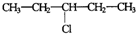 .
.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
| A、CO32-、Na+、OH-、Cl- |
| B、K+、NO3-、SO42-、CO32- |
| C、Fe2+、Na+、H+、NO3- |
| D、Cl-、Mg2+、Na+、SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、NaOH和HCl |
| B、Na和O2 |
| C、NaOH和CO2 |
| D、C和O2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、在水中的溶解性:NaHCO3>Na2CO3 |
| B、與同一種且質量分數相同的鹽酸溶液反應的速率:NaHCO3<Na2CO3 |
| C、熱穩定性:NaHCO3<Na2CO3 |
| D、Na2CO3是小蘇打,而NaHCO3是蘇打 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、在金剛石網狀結構中,由共價鍵形成的最小碳環上有6個碳原子 |
| B、在氯化鈉晶體中,每個鈉離子的周圍與它最近且等距離的鈉離子有12個 |
| C、在干冰晶體中,每個二氧化碳分子周圍距離最近且相等的二氧化碳分子數是12 |
| D、在氯化銫的晶體中,每個銫離子的周圍與它最近且等距離的銫離子有8個 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com