
【題目】磷和砷的相關化合物在化工、醫藥、材料等領域有著廣泛的應用。回答下列問題:
(1)基態As原子的核外電子排布式為[Ar]_________;As原子的逐級電離能(kJ/mol)數據如下:
第一電離能 | 第二電離能 | 第三電離能 | 第四電離能 | 第五電離能 | 第六電離能 |
947.0 | 1798 | 2735 | 4837 | 6043 | 12310 |
第五電離能與第六電離能相差顯著的原因:_____________________________________。
(2)紅磷是巨型共價分子,無定型結構。能證明紅磷是非晶體的最可靠方法是__________。
A.質譜 B.原子發射光譜 C.核磁共振譜 D.X射線衍射
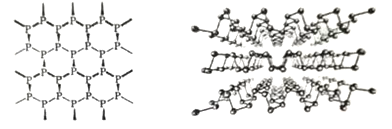
(3)黑磷是新型二維半導體材料,具有類似石墨一樣的片層結構(如圖),層與層之間以_____結合。從結構上看,單層磷烯導電性優于石墨烯的原因是____________________________。
(4)白磷(P4)分子是正四面體結構,3.1g白磷中σ鍵的數目為________;白磷(P4)易溶于二硫化碳,難溶于水,其原因是_____________________________________________。
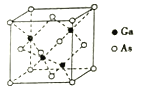
(5)GaAs的熔點為1238℃,其晶胞結構如圖所示。該晶體的類型為_________,Ga原子的雜化方式為______________,每個As原子周圍最近的As原子數目為________。已知GaAs的密度為dg/cm3,摩爾質量為Mg/mol,則晶胞中最近的As和Ga原子核間距為_____(阿伏加德羅常數值用NA表示,列出算式即可)nm。
【答案】 3d104s24p3 As原子最外層有五個電子,失去的第六個電子來自全滿的次外層,所需能量較高 D 范德華力 石墨烯同層碳原子中,1個碳原子和周圍3個碳原子結合后,還剩1個價電子 ,單層磷烯同層磷原子中,1個磷原子和周圍3個磷原子結合后,還剩2個價電子 0.15NA 二硫化碳和白磷都是非極性分子,水是極性分子,由相似相溶原理可知,白磷易溶于二硫化碳,難溶于水 原子晶體 sp3 12 ![]() ×
×![]() ×107
×107
【解析】 (1) As為第四周期第VA族元素,基態As原子的核外電子排布式為[Ar] 3d104s24p3;As原子最外層有五個電子,失去的第六個電子來自全滿的次外層,所需能量較高,使得As原子的第五電離能與第六電離能相差顯著,故答案為:3d104s24p3;As原子最外層有五個電子,失去的第六個電子來自全滿的次外層,所需能量較高;
(2)紅磷是巨型共價分子,無定型結構。能證明紅磷是非晶體的最可靠方法是X射線衍射實驗,故答案為:D;
(3)黑磷是新型二維半導體材料,具有類似石墨一樣的片層結構(如圖),層與層之間以范德華力結合。石墨烯同層碳原子中,1個碳原子和周圍3個碳原子結合后,還剩1個價電子 ,單層磷烯同層磷原子中,1個磷原子和周圍3個磷原子結合后,還剩2個價電子,因此單層磷烯導電性優于石墨烯,故答案為:范德華力;石墨烯同層碳原子中,1個碳原子和周圍3個碳原子結合后,還剩1個價電子 ,單層磷烯同層磷原子中,1個磷原子和周圍3個磷原子結合后,還剩2個價電子;
(4)白磷(P4)分子是正四面體結構,1個白磷分子中含有6個P-P鍵,3.1g白磷的物質的量為![]() =0.025mol,σ鍵的數目為0.025mol×6 NA=0.15NA;二硫化碳和白磷都是非極性分子,水是極性分子,由相似相溶原理可知,白磷易溶于二硫化碳,難溶于水,故答案為:0.15NA;二硫化碳和白磷都是非極性分子,水是極性分子,由相似相溶原理可知,白磷易溶于二硫化碳,難溶于水;
=0.025mol,σ鍵的數目為0.025mol×6 NA=0.15NA;二硫化碳和白磷都是非極性分子,水是極性分子,由相似相溶原理可知,白磷易溶于二硫化碳,難溶于水,故答案為:0.15NA;二硫化碳和白磷都是非極性分子,水是極性分子,由相似相溶原理可知,白磷易溶于二硫化碳,難溶于水;
(5)GaAs的熔點為1238℃,熔點較高,屬于原子晶體。根據結構圖,Ga原子與周圍的4個As原子相連接,雜化方式為sp3,As原子位于立方體的頂點和面心,每個As原子周圍最近的As原子數目為12個。每個晶胞中含有4個Ga原子和8×![]() +6×
+6×![]() =4個As原子,則晶胞的邊長=
=4個As原子,則晶胞的邊長=![]() =
=![]() cm=
cm=![]() ×107 nm,晶胞中最近的As和Ga原子核間距為晶胞體對角線長度的
×107 nm,晶胞中最近的As和Ga原子核間距為晶胞體對角線長度的![]() =
=![]() ×107 nm×
×107 nm×![]() =
=![]() ×
×![]() ×107 nm,故答案為:原子晶體;sp3;12;
×107 nm,故答案為:原子晶體;sp3;12;![]() ×
×![]() ×107。
×107。


 小學期末沖刺100分系列答案
小學期末沖刺100分系列答案 期末復習檢測系列答案
期末復習檢測系列答案 超能學典單元期中期末專題沖刺100分系列答案
超能學典單元期中期末專題沖刺100分系列答案 黃岡360度定制密卷系列答案
黃岡360度定制密卷系列答案科目:高中化學 來源: 題型:
【題目】將一鐵、銅混合物粉末平均分成三等份,分別加入到同濃度、不同體積的稀硝酸中,充分反應后,收集到NO氣體的體積及剩余固體的質量如表 (設反應前后溶液的體積不變,氣體體積已換算為標準狀況時的體積):
實驗序號 | 稀硝酸的體積/mL | 剩余固體的質量/g | NO的體積/L |
1 | 100 | 17.2 | 2.24 |
2 | 200 | 8.00 | 4.48 |
3 | 400 | 0 | V |
下列說法正確的是( )
A. 表中V=7.84 L
B. 原混合物粉末的質量為25.6 g
C. 原混合物粉未中鐵和銅的物質的量之比為2:3
D. 實驗3所得溶液中硝酸的物質的量濃度為0.875 molL﹣1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知反應A+B==C+D的能量變化如圖所示,下列說法正確的是
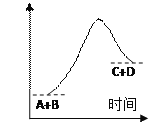
A. 該反應為吸熱反應
B. 該反應只有在加熱條件下才能進行
C. 反應物的總能量高于產物的總能量
D. 形成產物C和D的化學鍵所放出的總能量高于斷開反應物A 和B的化學鍵所吸收的總能量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ已知銅在常溫下能被HNO3溶解。反應方程式為: 3Cu+8HNO3=3Cu(NO3)2+2NO ↑+4H2O
(1)請將上述反應改成離子方程式,并用單線橋法表示電子得失的方向和數目________________。
(2)若生成448mL的NO(標準狀況下),則該過程中轉移的電子是___________mol。
(3)被還原的硝酸占參加反應硝酸的比例為___________。
Ⅱ某反應體系有反應物和生成物共7種物質:C、H2SO4、K2CrO4、K2SO4、CO2 、Cr2(SO4)3和H2O。已知該反應中發生如下過程:C→CO2。該反應的化學方程式:__________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于強、弱電解質的敘述中正確的是( )
A. 強電解質都是離子化合物,弱電解質都是共價化合物
B. 強電解質都是可溶性化合物,弱電解質都是難溶性化合物
C. 強電解質熔化時都完全電離,弱電解質在水溶液中部分電離
D. 強電解質不一定能導電,弱電解質溶液的導電能力不一定比強電解質弱
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某白色粉末由兩種物質組成,為鑒別其成分進行如下實驗:
①取少量樣品加入足量水仍有部分固體未溶解;再加入足量稀鹽酸,有氣泡產生,固體全部溶解;
②取少量樣品加入足量稀硫酸有氣泡產生,振蕩后仍有固體存在。
該白色粉末可能為( )
A. ![]() 、
、![]() B. AgCl、
B. AgCl、![]()
C. ![]() 、
、![]() D.
D. ![]() 、
、![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列物質中的雜質(括號中是雜質)分別可以用什么試劑和方法除去。
物質 | 試劑 | 方法 |
①乙醇(水) | ___ | ___ |
②乙酸乙酯(乙酸) | ___ | ___ |
③甲烷(乙烯) | ___ | ___ |
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鹽在化學工業中有重要的應用,請回答下列問題:
(1)用化學方程式表示配制FeCl3溶液時常加入濃鹽酸的原因______________________________________________
(2)常溫下,在pH=3的Al2(SO4)3溶液與pH=11的Na2S溶液中,水電離出來的c(OH﹣)之比為______,將兩溶液混合后,產生白色沉淀和有臭雞蛋味的氣體,其反應的離子方程式為_________________________
(3)c(NH4+)相等的下列溶液①NH4Cl ②NH4HSO4 ③(NH4)2SO4 ④CH3COONH4 ⑤NH3·H2O,溶液的物質的量濃度由小到大的順序是______________________________________________________ (用序號表示)
(4)已知t℃時①AgCl的Ksp=2×10﹣10;②在t℃時,Ag2CrO4在水中的沉淀溶解平衡曲線如圖所示.下列正確的是_______

A.在飽和Ag2CrO4溶液中加入K2CrO4可使溶液由Y點到X點
B.在t℃時Ag2CrO4的Ksp為1×10-12
C.在t℃時反應:Ag2CrO4(s)+2Cl-(aq)![]() 2AgCl(s)+CrO42-(aq)的平衡常數為2.5×107
2AgCl(s)+CrO42-(aq)的平衡常數為2.5×107
D.在t℃時以0.01mol/L的AgNO3溶液滴定20mL濃度均為0.01mol/L的KCl和K2CrO4的混合溶液,CrO42-先沉淀
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】研究硫元素及其化合物的性質具有重要意義。
(1)25 ℃,在0.10 mol·L-1H2S溶液中,通入HCl氣體或加入NaOH固體以調節溶液pH,溶液pH與c(S2-)關系如下圖(忽略溶液體積的變化、H2S的揮發)。

①pH=11時,溶液中的c(H2S)+c(HS-)=________mol·L-1。
②某溶液含0.020 mol·L-1Mn2+、0.10 mol·L-1H2S,當溶液pH=________時,Mn2+開始沉淀。[已知:Ksp(MnS)=2.8×10-13]
(2)25 ℃,兩種酸的電離常數如下表。
Ka1 | Ka2 | |
H2SO3 | 1.3×10-2 | 6.3×10-8 |
H2CO3 | 4.2×10-7 | 5.6×10-11 |
①HCO![]() 的電離常數表達式K=________。
的電離常數表達式K=________。
②0.10 mol·L-1Na2SO3溶液中離子濃度由大到小的順序為___________________。
③H2SO3溶液和NaHCO3溶液反應的主要離子方程式為__________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com