
| A、FeO溶于足量稀HNO3:FeO+2H+═Fe2++H2O |
| B、NH4HCO3溶液與足量Ba(OH)2溶液混合:HCO3-+Ba2++OH-═BaCO3↓+H2O |
| C、等物質的量的KHCO3和Ba(OH)2的溶液混合:HCO3-+Ba2++OH-═BaCO3↓+H2O |
| D、將0.2mol/L的NH4Al(SO4)2溶液與0.4mol/L的Ba(OH)2溶液等體積混合2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ |


科目:高中化學 來源: 題型:
| 15 |
| 16 |
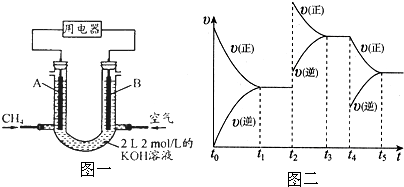
查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:

| A、該反應是吸熱反應 |
| B、催化劑改變了該反應的焓變 |
| C、曲線b表示使用催化劑后的能量變化 |
| D、該反應的焓變△H=-510kJ?mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、1mol醛基中含有電子的數目為16NA |
| B、1L pH=1的水溶液中含氫離子數目為NA |
| C、每生成1mol O2,電子轉移數目一定是4NA |
| D、30g二氧化硅晶體中含共價鍵的數目為2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、0.1 mol/L的下列溶液:①NH4Al(SO4)2 ②NH4Cl ③NH3?H2O ④CH3COONH4中c(NH4+)由大到小的順序是:②>①>④>③ |
| B、NaHCO3溶液和Na2CO3溶液混合一定存在:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) |
| C、25℃時,pH=11的氨水和pH=3的硫酸等體積混合:c(NH4+)>c(SO42-)>c(OH-)>c(H+) |
| D、室溫下,向100mL 0.1mol/L NH4HSO4溶液中滴加0.1mol/L NaOH溶液至中性,混合溶液中各離子濃度大小關系:c(Na+)>c(NH4+)>c(SO42-)>c(OH-)=c(H+) |
查看答案和解析>>
科目:高中化學 來源: 題型:
 研究發現,可以用石墨作陽極、鈦網作陰極、熔融CaF2-CaO作電解質,利用如圖所示裝置獲得金屬鈣,并以鈣為還原劑還原二氧化鈦制備金屬鈦.下列說法中,不正確的是( )
研究發現,可以用石墨作陽極、鈦網作陰極、熔融CaF2-CaO作電解質,利用如圖所示裝置獲得金屬鈣,并以鈣為還原劑還原二氧化鈦制備金屬鈦.下列說法中,不正確的是( )| A、由TiO2制得1mol金屬Ti,理論上外電路轉移4mol電子 |
| B、陽極的電極反應式為:C+2O2--4e-═CO2↑ |
| C、若用鉛蓄電池作該裝置的供電電源,“+”接線柱應連接Pb電極 |
| D、在制備金屬鈦前后,整套裝置中CaO的總量不變 |
查看答案和解析>>
科目:高中化學 來源: 題型:
 科研、生產中常涉及鈉、硫及其化合物.如圖為鈉硫高能電池的結構示意圖,該電池的工作溫度為320℃左右,電池反應為2Na+xS═Na2Sx,下列敘述錯誤的是( )
科研、生產中常涉及鈉、硫及其化合物.如圖為鈉硫高能電池的結構示意圖,該電池的工作溫度為320℃左右,電池反應為2Na+xS═Na2Sx,下列敘述錯誤的是( )| A、該電池的負極材料是鈉 |
| B、陶瓷材料的作用是導電(電解質)兼隔膜 |
| C、當電池中轉移1.204×1024個電子時,消耗鈉的物質的量為2mol |
| D、外電路中電子的移動方向是:S→Na |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、原子半徑:W>Y>Z>M>X |
| B、化合物乙中一定只有共價鍵 |
| C、由W元素形成的單質以及W與Z兩元素形成的化合物都是原子晶體 |
| D、X分別與Y、Z、M、W形成的常見化合物中,穩定性最好的是XM,沸點X2Z>XM |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com