
(14分) 某化學興趣小組欲驗證:“銅和一定量的濃硝酸反應有一氧化氮產生”。設計使用了如下裝置進行實驗。(假設氣體體積均為標準狀況,導氣管中氣體體積忽略不計,且忽略反應中的溶液體積變化)
試回答下列問題:
(1)將銅粉分散在石棉絨中的原因是___________________________________。
(2)在銅和濃硝酸反應前,擠壓打氣球,經A、B、C反應后,進入D中的氣體主要成分是_________(填化學式),通入該氣體的目的是_________________________________;進行此步操作時應關閉_________,打開_________ (填K1、K2或K3)。
(3)關閉K1、K2,打開K3,由分液漏斗向D中滴加濃硝酸。待Cu和濃硝酸反應結束后,再通過分液漏斗向D中加入CCl4至滿。則D中一定發生反應的離子方程式為:_______________________________________________________________________。
(4)若E中出現倒吸,可采取的應急操作是_________________________________。
(5)Ⅰ.從E裝置所得溶液中取出25.00mL,加兩滴酚酞,用0.1000 mol·L-1的NaOH溶液滴定,當滴定完成后消耗NaOH溶液18.00mL,則E容器中所得硝酸的物質的量濃度為__________________mol·L-1。
Ⅱ.若實驗測得F裝置所收集到的氣體體積為139.00 mL,則銅和一定量的濃硝酸反應___________(填“有”或“無”)NO生成,其依據是(請用數據和文字說明)__________________________________________________________________________________________________________________________________________________________________________________________________________________________。
科目:高中化學 來源: 題型:
(14分) 某化學興趣小組,專門研究了氧族元素及其某些化合物的部分性質。查得的資料如下:
①常溫下,硒(Se)和碲(Te)為固體,H2Se和H2Te為氣體;
②Te和H2不能直接化合生成H2Te;
③氧氣、硫、硒、碲與1 mol H2反應的焓變(△H)情況如下表所示。
| 物質 | O2 | S | Se | Te |
| ΔH(kJ·mol-1) | -242 | -20 | 81 |
|
請回答下列問題:
(1)寫出氧族元素中含有18個電子的兩種氫化物的化學式 、 。
(2)寫出硒化氫發生分解反應的熱化學方程式: 。
(3)已知H2Te分解反應的ΔS>0,ΔH=-154kJ·mol-1,請解釋Te和H2不能直接化合的原因
。
(4)H2S的水溶液顯弱酸性,寫出其電離方程式 ;它的第一級電離常數可用Ka1來表示,當溫度升高時,Ka1的值 (填“一定增大”、“一定減小”或“不能確定”)。
(5)在容積均為1 L(容器體積不可變)的甲、乙兩個容器中,分別充入2 mol SO2、1 molO2 和4 mol SO2、2 mol O2,在相同條件下使其反應。最終達到平衡后,甲、乙兩容器中SO2轉化率分別為50%和α(乙),則反應的平衡常數Kc= L·mol-1(填寫具體數據),此時α(乙) 50%(填“大于”、“小于”或“等于”)。
查看答案和解析>>
科目:高中化學 來源:2010年湖南省六校高三第二次聯考(理綜)化學部分 題型:填空題
(14分) 某化學興趣小組,專門研究了氧族元素及其某些化合物的部分性質。查得的資料如下:
①常溫下,硒(Se)和碲(Te)為固體,H2Se和H2Te為氣體;
②Te和H2不能直接化合生成H2Te;
③氧氣、硫、硒、碲與1 mol H2反應的焓變(△H)情況如下表所示。
| 物質 | O2 | S | Se | Te |
| ΔH(kJ·mol-1) | -242 | -20 | 81 | |
 (填“一定增大”、“一定減小”或“不能確定”)。
(填“一定增大”、“一定減小”或“不能確定”)。查看答案和解析>>
科目:高中化學 來源:2010年重慶市高三年級5月月考(理綜)化學部分 題型:實驗題
(14分) 某化學興趣小組欲驗證:“銅和一定量的濃硝酸反應有一氧化氮產生”。設計使用了如下裝置進行實驗。(假設氣體體積均為標準狀況,導氣管中氣體體積忽略不計,且忽略反應中的溶液體積變化)
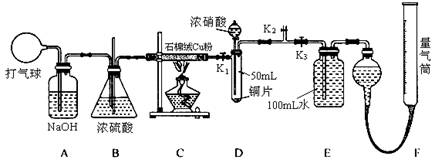
試回答下列問題:
(1)將銅粉分散在石棉絨中的原因是___________________________________。
(2)在銅和濃硝酸反應前,擠壓打氣球,經A、B、C反應后,進入D中的氣體主要成分是_________(填化學式),通入該氣體的目的是_________________________________;進行此步操作時應關閉_________,打開_________ (填K1、K2或K3)。
(3)關閉K1、K2,打開K3,由分液漏斗向D中滴加濃硝酸。待Cu和濃硝酸反應結束后,再通過分液漏斗向D中加入CCl4至滿。則D中一定發生反應的離子方程式為:_______________________________________________________________________。
(4)若E中出現倒吸,可采取的應急操作是_________________________________。
(5)Ⅰ.從E裝置所得溶液中取出25.00mL,加兩滴酚酞,用0.1000 mol·L-1的NaOH溶液滴定,當滴定完成后消耗NaOH溶液18.00mL,則E容器中所得硝酸的物質的量濃度為__________________ mol·L-1。
Ⅱ.若實驗測得F裝置所收集到的氣體體積為139.00 mL,則銅和一定量的濃硝酸反應___________(填“有”或“無”)NO生成,其依據是(請用數據和文字說明)__________________________________________________________________________________________________________________________________________________________________________________________________________________________。
查看答案和解析>>
科目:高中化學 來源:2010年湖南省六校高三第二次聯考(理綜)化學部分 題型:填空題
(14分) 某化學興趣小組,專門研究了氧族元素及其某些化合物的部分性質。查得的資料如下:
①常溫下,硒(Se)和碲(Te)為固體,H2Se和H2Te為氣體;
②Te和H2不能直接化合生成H2Te;
③氧氣、硫、硒、碲與1 mol H2反應的焓變(△H)情況如下表所示。
|
物質 |
O2 |
S |
Se |
Te |
|
ΔH(kJ·mol-1) |
-242 |
-20 |
81 |
|
請回答下列問題:
(1)寫出氧族元素中含有18個電子的兩種氫化物的化學式 、 。
(2)寫出硒化氫發生分解反應的熱化學方程式: 。
(3)已知H2Te分解反應的ΔS>0,ΔH=-154 kJ·mol-1,請解釋Te和H2不能直接化合的原因
。
(4)H2S的水溶液顯弱酸性,寫出其電離方程式 ;它的第一級電離常數可用Ka1來表示,當溫度升高時,Ka1的值 (填“一定增大”、“一定減小”或“不能確定”)。
(5)在容積均為1 L(容器體積不可變)的甲、乙兩個容器中,分別充入2 mol SO2、1 molO2 和4 mol SO2、2 mol O2,在相同條件下使其反應。最終達到平衡后,甲、乙兩容器中SO2轉化率分別為50%和α(乙),則反應的平衡常數Kc= L·mol-1(填寫具體數據),此時α(乙) 50%(填“大于”、“小于”或“等于”)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com