
【題目】鼠尾草酚可用于防治骨質疏松,鼠尾草酸可兩步轉化得到鼠尾草酚,下列說法正確的是( )

A.X、Y、Z分子中均含有2個手性碳原子
B.X、Y、Z均能與FeCl3溶液發生顯色反應
C.1molY最多能消耗2molH2
D.1molZ與NaOH溶液反應最多消耗3molNaOH
科目:高中化學 來源: 題型:
【題目】藥物瑞德西韋(Remdesivir)對新冠病毒有明顯抑制作用,化合物 M是合成瑞德西韋的中間體,下列關于M的說法錯誤的是
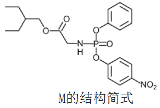
A.核磁共振氫譜共有11個吸收峰
B.分子中含有3種含氧官能團
C.分子中N原子一個是sp2雜化,一個是sp3雜化
D.1mol該物質與足量NaOH溶液反應時消耗3molNaOH
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】CO、SO2是主要的大氣污染氣體,利用化學反應原理是治理污染的重要方法。
I.甲醇是一種新型燃料,甲醇燃料電池即將從實驗室走向工業化生產。工業上一般以CO和H2為原料合成甲醇,該反應的熱化學方程式為:CO(g)+2H2(g)![]() CH3OH(g) △H1=-116kJ·mol-1
CH3OH(g) △H1=-116kJ·mol-1
(1)下列措施中有利于增大該反應的反應速率的是___;
A.隨時將CH3OH與反應混合物分離 B.降低反應溫度
C.增大體系壓強 D.使用高效催化劑
(2)已知:CO(g)+2H2(g)![]() CH3OH(g) △H1=-116kJ·mol-1
CH3OH(g) △H1=-116kJ·mol-1
CO(g)+![]() O2(g)=CO2(g) △H2=-283kJ·mol-1
O2(g)=CO2(g) △H2=-283kJ·mol-1
H2(g)+![]() O2(g)=H2O(g) △H3
O2(g)=H2O(g) △H3
化學鍵 | H—H | O=O | O—H |
鍵能/KJmol-1 | 436 | 498 | 463.5 |
則△H3=___,表示1mol氣態甲醇完全燃燒生成CO2和水蒸氣時的熱化學方程式為___;
Ⅱ.當溫度高于500 K時,科學家成功利用二氧化碳和氫氣合成了乙醇,2CO2(g)+6H2(g)![]() C2H5OH(g)+3H2O(g)。這在節能減排、降低碳排放方面具有重大意義。回答下列問題:
C2H5OH(g)+3H2O(g)。這在節能減排、降低碳排放方面具有重大意義。回答下列問題:
(1)其平衡常數表達式為K=____。
(2)在恒容密閉容器中,判斷上述反應達到平衡狀態的依據是___。
a.體系壓強不再改變 b.H2的濃度不再改變
c.氣體的密度不隨時間改變 d.單位時間內消耗H2和CO2的物質的量之比為3∶1
(3)在一定壓強下,測得由CO2制取CH3CH2OH的實驗數據中,起始投料比、溫度與CO2的轉化率的關系如圖。根據圖中數據
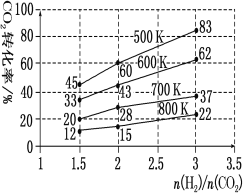
①降低溫度,平衡向____方向移動。
②在700K、起始投料比![]() =1.5時,H2的轉化率為___。
=1.5時,H2的轉化率為___。
③在500K、起始投料比![]() =2時,達到平衡后H2的濃度為amol·L-1,則達到平衡時CH
=2時,達到平衡后H2的濃度為amol·L-1,則達到平衡時CH
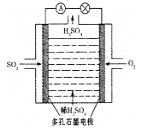
Ⅲ.某學習小組以SO2為原料,采用原電池法制取硫酸。該小組設計的原電池原理如圖所示。該電池中右側為___極,寫出該電池負極的電極反應式___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】乙炔是一種無色無味的氣體,微溶于水,易溶于有機溶劑。實驗室常用如圖所示裝置制取乙炔,并驗證乙炔的性質。完成實驗,觀察實驗現象,回答下列問題:
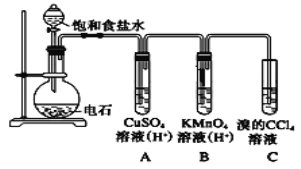
(1)寫出電石(碳化鈣CaC2)與水反應,制取乙炔的化學方程式_________________
(2)用飽和食鹽水代替蒸餾水的目的是__________________
(3)裝置A的作用是_______________,裝置B中的現象是__________________
(4)如果要進行乙炔的可燃性實驗,首先應該__________________。
(5)若乙炔加氫后得到乙烷,則乙烷在光照條件下與氯氣反應,生成的一氯代烷最多有__________種。
(6)若稱取a g CaC2,反應完全后,將生成的乙炔全部通入足量溴的CCl4溶液中溶液增重b g,則CaC2的純度為___________(用百分數表示)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】白皮杉醇具有抗炎、抗菌、抗氧化、抗白血病、提高免疫調節功能等功效,其人工合成過程涉及了如下轉化:
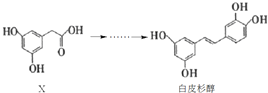
下列說法正確的是
A.X的分子式為C8H10O4
B.化合物X、白皮杉醇均可與Na2CO3溶液反應并放出氣體
C.白皮杉醇與濃溴水反應時,最多可消耗6molBr2
D.在一定條件下,白皮杉醇可發生加成、取代、氧化和聚合反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】按要求回答下列問題:
(1)黃銅礦(CuFeS2)是煉銅的最主要礦物。火法冶煉黃銅礦的過程中,其中一步反應是2Cu2O+Cu2S![]() 6Cu+SO2↑。則29Cu的外圍電子軌道表示式為____;比較Cu2O與Cu2S,熔點較高的是____,原因為____。
6Cu+SO2↑。則29Cu的外圍電子軌道表示式為____;比較Cu2O與Cu2S,熔點較高的是____,原因為____。
(2)一種銅金合金晶體具有面心立方最密堆積結構,在晶胞中Cu原子處于面心,Au原子處于頂點,則該合金中Cu原子與Au原子數量之比為____;該晶體中原子之間的作用力是____。
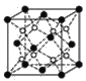
(3)上述晶體具有儲氫功能,氫原子可進入到由Cu原子與Au原子構成的四面體空隙中。若將Cu原子與Au原子等同看待,該晶體儲氫后的晶胞結構與CaF2的結構相似(如圖),該晶體儲氫后的化學式應為____。
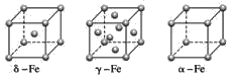
(4)鐵有δ、γ、α三種同素異形體(如圖),γ晶體晶胞中所含有的鐵原子數為____,δ、α兩種晶胞中鐵原子的配位數之比為____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示,高溫下,超氧化鉀晶體呈立方體結構,晶體中氧的化合價部分為0價,部分為![]() 價。如圖為超氧化鉀晶體的一個晶胞(晶體中最小的重復單元),則下列說法中錯誤的是( )
價。如圖為超氧化鉀晶體的一個晶胞(晶體中最小的重復單元),則下列說法中錯誤的是( )

A.超氧化鉀的化學式為KO2,每個晶胞含有4個K+和4個O2-
B.晶體中,每個O2-周圍距離最近的O2-有8個
C.晶體中與每個K+周圍有8個O2-
D.晶體中,0價氧與-2價氧的數目比為3∶1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】研究氮及其化合物的性質,可以有效改善人類的生存環境。氮元素化合價—物質類別關系圖如下。
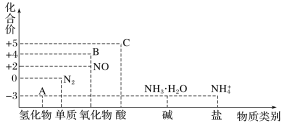
回答下列問題:
(1)在催化劑和加熱的條件下,物質A生成NO是工業制硝酸的重要反應,化學方程式是_______。
(2)在加熱條件下,物質C的濃溶液與碳單質反應,寫出反應的化學方程式:_______。
(3)實驗室中,檢驗溶液中含有NH4+的操作方法是_________。
(4)物質B為紅棕色氣體,寫出該物質與水反應的離子方程式:__________,當反應消耗3.36L(標準狀況)物質B時,轉移電子的物質的量為________mol。
(5)寫出一種人工固氮的化學反應原理_______。
(6)Cu與一定濃度的硝酸溶液反應生成NO時的離子反應方程式為_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法中不正確的是( )
A. 反應CaCO3(s)===CaO(s)+CO2(g)在常溫下不能自發進行,則該反應的ΔH<0
B. 鍋爐中沉積的CaSO4可用飽和Na2CO3溶液浸泡,再將不溶物用稀鹽酸溶解除去
C. 不能用玻璃瓶來盛裝氟化鈉水溶液
D. 常溫下Ksp[Mg(OH)2]=5.6×10-12,pH=10的含Mg2+溶液中,c(Mg2+)≤5.6×10-4mol·L-1
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com