
第四周期過渡元素Mn、Fe、Ti可與C、H、O形成多種化合物。(1)下列敘述正確的是 。(填字母)
A.CH2O與水分子間能形成氫鍵 B.CH2O和CO2分子中的中心原子均采用sp2雜化
C.C6H6分子中含有6個 鍵和1個大
鍵和1個大 鍵,C6H6是非極性分子
鍵,C6H6是非極性分子
D.CO2晶體的熔點、沸點都比二氧化硅晶體的低
(2)Mn和Fe的部分電離能數據如下表:
|
元 素 |
Mn |
Fe |
|
|
電離能 /kJ·mol-1 |
I1 |
717 |
759 |
|
I2 |
1509 |
1561 |
|
|
I3 |
3248 |
2957 |
Mn元素價電子排布式為 ,氣態Mn2+再失去一個電子比氣態Fe2+再失去一個電子難,其原因是 。
(3)根據元素原子的外圍電子排布的特征,可將元素周期表分成五個區域,其中Ti屬于 區。
(4)Ti的一種氧化物X,其晶胞結構如圖所示,則X的化學式為 。已知晶胞邊長為bcm,阿伏伽德羅常數為NA該氧化物的密度為__________________g/cm-3

(5)電鍍廠排放的廢水中常含有劇毒的CN-離子,可在X的催化下,先用NaClO將CN-氧化成CNO-,再在酸性條件下CNO-繼續被NaClO氧化成N2和CO2。
①H、C、N、O四種元素的電負性由小到大的順序為 。
②與CNO-互為等電子體微粒的化學式為 (寫出一種即可)。
③氰酸(HOCN)是一種鏈狀分子,它與異氰酸(HNCO)互為同分異構體,其分子內各原子最外層均已達到穩定結構,試寫出氰酸的結構式 。
(1)AD (2)3d54s2 Mn2+轉化為Mn3+時,3d能級由較穩定的3d5半充滿狀態轉變為不穩定的3d4狀態(或Fe2+轉化為Fe3+時,3d能級由不穩定的3d6狀態轉變為較穩定的3d5半充滿狀態。)(3)d區
(4) TiO2 160/( NA·b3) .(5)① H<C<N<O ②CO2(N2O)、SCN ③ N≡C—O—H
【解析】
試題分析:(1)A.由于CH2O分子和H2O中O原子的電負性大,原子半徑小,所以它們之間能形成氫鍵。正確。B. CH2O和CO2分子中的中心原子前者采用sp2雜化,后者采用sp雜化。錯誤。C.C6H6分子中的碳原子與碳原子之間含有6個σ鍵和1個大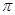 鍵,。碳原子與氫原子之間形成的也是σ鍵。化學鍵與化學鍵之間的夾角是120度。整個分子中各個化學鍵排列對稱,電荷分布均勻。C6H6是非極性分子。錯誤。D.CO2晶體是分子晶體,分子間以分子間作用力結合。分子間作用力比較弱,斷裂比較容易,所以它的熔點、沸點低。而二氧化硅晶體是原子晶體,原子間以強的共價鍵結合。斷裂需要消耗很多的能量。所以使物質融化或氣化需要消耗很多能量。故溶沸點高。因此CO2晶體的熔點、沸點都比二氧化硅晶體的低。正確。(2)Mn元素是25號元素,其核外電電子排布1s22s22p63s23p63d54s2.
價電子排布式為3d54s2. 氣態Mn2+再失去一個電子比氣態Fe2+再失去一個電子難,是因為Mn2+價電子排布式為3d5.處于半充滿的穩定狀態。若Mn2+轉化為Mn3+時,3d能級由較穩定的3d5半充滿的穩定狀態轉變為不穩定的3d4狀態。而氣態Fe2+再失去一個電子,由Fe2+轉化為Fe3+時,3d能級由不穩定的3d6狀態轉變為較穩定的3d5半充滿的穩定狀態。(3)根據元素原子的外圍電子排布的特征,可將元素周期表分成五個區域,其中Ti屬于d區。Ti:8×1/8+1=2;O:4×1/2+2=4;Ti:O=2:3=1:2.所以該晶體的化學式是TiO2 。。ρ·b3=(2×80)÷NA.解得ρ= 160/( NA·b3)
. (5)① H、C、N、O四種元素的電負性由小到大的順序為H<C<N<O;② 與CNO-互為等電子體微粒的化學式為CO2(N2O)、SCN。③氰酸的結構式N≡C—O—H。
鍵,。碳原子與氫原子之間形成的也是σ鍵。化學鍵與化學鍵之間的夾角是120度。整個分子中各個化學鍵排列對稱,電荷分布均勻。C6H6是非極性分子。錯誤。D.CO2晶體是分子晶體,分子間以分子間作用力結合。分子間作用力比較弱,斷裂比較容易,所以它的熔點、沸點低。而二氧化硅晶體是原子晶體,原子間以強的共價鍵結合。斷裂需要消耗很多的能量。所以使物質融化或氣化需要消耗很多能量。故溶沸點高。因此CO2晶體的熔點、沸點都比二氧化硅晶體的低。正確。(2)Mn元素是25號元素,其核外電電子排布1s22s22p63s23p63d54s2.
價電子排布式為3d54s2. 氣態Mn2+再失去一個電子比氣態Fe2+再失去一個電子難,是因為Mn2+價電子排布式為3d5.處于半充滿的穩定狀態。若Mn2+轉化為Mn3+時,3d能級由較穩定的3d5半充滿的穩定狀態轉變為不穩定的3d4狀態。而氣態Fe2+再失去一個電子,由Fe2+轉化為Fe3+時,3d能級由不穩定的3d6狀態轉變為較穩定的3d5半充滿的穩定狀態。(3)根據元素原子的外圍電子排布的特征,可將元素周期表分成五個區域,其中Ti屬于d區。Ti:8×1/8+1=2;O:4×1/2+2=4;Ti:O=2:3=1:2.所以該晶體的化學式是TiO2 。。ρ·b3=(2×80)÷NA.解得ρ= 160/( NA·b3)
. (5)① H、C、N、O四種元素的電負性由小到大的順序為H<C<N<O;② 與CNO-互為等電子體微粒的化學式為CO2(N2O)、SCN。③氰酸的結構式N≡C—O—H。
考點:考查Fe Ti等過渡元素的原子結構、晶體結構及有關計算等的知識。


科目:高中化學 來源: 題型:閱讀理解
 第四周期過渡元素Mn、Fe、Ti可與C、H、O形成多種化合物.
第四周期過渡元素Mn、Fe、Ti可與C、H、O形成多種化合物.| 元 素 | Mn | Fe | |
| 電離能 /kJ?mol-1 |
I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
查看答案和解析>>
科目:高中化學 來源:2013-2014學年湖北省荊門市高三元月調考理綜化學試卷(解析版) 題型:填空題
第四周期過渡元素Mn、Fe、Ti可與C、H、O形成多種化合物。
(1)下列敘述正確的是?????? 。(填字母)
A.CH2O與水分子間能形成氫鍵
B.CH2O和CO2分子中的中心原子均采用sp2雜化
C.C6H6分子中含有6個 鍵和1個大
鍵和1個大 鍵,C6H6是非極性分子
鍵,C6H6是非極性分子
D.CO2晶體的熔點、沸點都比二氧化硅晶體的低
(2)Mn和Fe的部分電離能數據如下表:
元??? 素 | Mn | Fe | |
電離能 /kJ·mol-1 | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 |
Mn元素價電子排布式為?????????? ,氣態Mn2+再失去一個電子比氣態Fe2+再失去一個電子難,其原因是????????????????????????? 。
(3)根據元素原子的外圍電子排布的特征,可將元素周期表分成五個區域,其中Ti屬于 區。
(4)Ti的一種氧化物X,其晶胞結構如圖所示,則X的化學式為???????????? 。

(5)電鍍廠排放的廢水中常含有劇毒的CN-離子,可在X的催化下,先用NaClO將CN-氧化成CNO-,再在酸性條件下CNO-繼續被NaClO氧化成N2和CO2。
①H、C、N、O四種元素的電負性由小到大的順序為??????????????????? 。
②與CNO-互為等電子體微粒的化學式為?????????? (寫出一種即可)。
③氰酸(HOCN)是一種鏈狀分子,它與異氰酸(HNCO)互為同分異構體,其分子內各原子最外層均已達到穩定結構,試寫出氰酸的結構式?????? 。
查看答案和解析>>
科目:高中化學 來源:不詳 題型:問答題
| 元 素 | Mn | Fe | |
| 電離能 /kJ?mol-1 |
I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |

查看答案和解析>>
科目:高中化學 來源:2011年江西省新余一中高考化學模擬試卷(解析版) 題型:解答題
| 元 素 | Mn | Fe | |
| 電離能 /kJ?mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com