
【題目】磷酸氯喹是一種抗瘧疾藥物, 研究發現,該藥在細胞水平上能有效抑制新型冠狀病毒的感染。其合成路線如下:
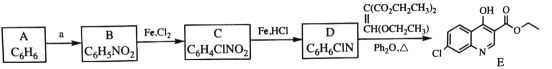

已知:

回答下列問題:
(1)A是一種芳香經, B 中官能團的名稱為__________________。
(2)反應 A→B 中須加入的試劑a 為___________________。
(3)B 反應生成 C 的反應化學反應方程式是______________________。
(4)C→D 反應類型是_________, D的結構簡式為_______________。
(5)F→G反應類型為________________。
(6)I是E的同分異構體,與E 具有相同的環狀結構, 寫出任意一種符合下列條件的I的結構簡式是__________________________。
①I是三取代的環狀有機物, 氯原子和羥基的取代位置與E相同;
②核磁共振氫譜顯示I 除了環狀結構上的氫外,還有4組峰, 峰面積比3:1:1:1;
③I加入NaHCO3溶液產生氣體。
【答案】硝基 濃硫酸、濃硝酸  +Cl2
+Cl2 +HCl 還原反應
+HCl 還原反應  取代反應
取代反應 
【解析】
產物中含有苯環,則A是苯,B為硝基苯,B到C是一個取代反應,考慮到E中氮原子和氯原子處于間位,因此C是間硝基氯苯,D則是硝基被還原后變成了間氨基氯苯,E到F即題目信息中給出的反應,從F到G,分子式中少1個O和1個H,而多出了一個Cl,因此為一個取代反應,用氯原子取代了羥基,最后再進一步取代反應得到H,據此來分析本題即可。
(1)根據分析,B是硝基苯,其官能團為硝基;
(2)硝化反應需要用到濃硫酸和濃硝酸組成的混酸;
(3)B到C即取代反應,方程式為 +Cl2
+Cl2 +HCl;
+HCl;
(4)C到D是硝基被還原為氨基的過程,因此是一個還原反應,D為鄰氨基氯苯,即 ;
;
(5)根據分析,F到G是一個取代反應;
(6)加入碳酸氫鈉溶液能產生氣體,因此分子中一定含有羧基,結合其它要求,寫出符合條件的同分異構體,為 。
。


科目:高中化學 來源: 題型:
【題目】常溫下,0.1mol/LH2C2O4水溶液中存在H2C2O4、HC2O4-和C2O42-三種形態含碳粒子,用NaOH或HCl調節該溶液的pH,三種含碳粒子的分布系數δ隨溶液pH變化的關系如圖[已知:a=1.35,b=4.17,Ksp(CaC2O4)=2.3×10-9,忽略溶液體積變化]。下列說法正確的是( )

A.pH=5時,溶液中主要含碳物種濃度大小關系為:c(C2O42-)>c(H2C2O4)>c(HC2O4-)
B.已知pKa=-lgKa,則pKa2(H2C2O4)=4.17
C.0.1mol·L-1NaHC2O4溶液中:c(H+)=c(OH-)+c(C2O42-)-c(H2C2O4)
D.一定溫度下往CaC2O4飽和溶液中加入少量CaCl2固體,c(C2O42-)將減小,c(Ca2+)不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】砷化鎵(GaAs)是優良的半導體材料,可用于制作微型激光器或太陽能電池的材料等。回答下列問題:
(1)寫出基態As原子的核外電子排布式___________。
(2)AsCl3分子的立體構型為_________,其中As的雜化軌道類型為________。
(3)GaF3的熔點高于1000℃,GaCl2的熔點為77.9℃,其原因是______________。
(4)GaAs的熔點為1238℃,密度為ρ g/cm3,其晶胞結構如圖所示。該晶體的類型為______________,Ga與As以______________鍵結合。Ga和As的摩爾質量分別為MGa g/mol和MAs g/mol,原子半徑分別為rGa pm和rAs pm,阿伏加德羅常數值為NA,則GaAs晶胞中原子的體積占晶胞體積的百分率為______________。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鎳鎘(Ni﹣Cd)可充電電池在現代生活中有廣泛應用。電解質溶液為KOH溶液,電池反應為:Cd+2NiO(OH)+2H2O![]() Cd(OH)2+2Ni(OH)2,下列有關鎳鎘電池的說法正確的是( )
Cd(OH)2+2Ni(OH)2,下列有關鎳鎘電池的說法正確的是( )
A.充電過程是化學能轉化為電能的過程
B.充電時陽極反應為Cd(OH)2+2e-=Cd+2OH-
C.放電時電池內部OH-向負極移動
D.充電時與直流電源負極相連的電極上發生Ni(OH)2轉化為NiO(OH)的反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】汽車尾氣中的CO和NO在排放時會發生復雜的化學反應。回答下列問題:
(1)通過NO傳感器可監測汽車排放尾氣中NO含量, 其工作原理如圖所示。
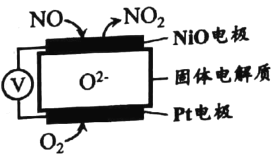
該傳感器正極的電極反應式為 _________________。
(2)已知如下發生反應:
①2CO(g)+O2(g)=2CO2(g) △H1 =-606.6 kJ·mol-1
②2NO(g)+O2(g)=2NO2(g) △H2= -114.1 kJ·mo l-1
則反應CO(g) +NO2(g) = CO2(g) +NO(g)的△H =__________kJmo l-1
(3)300K時,將等濃度的CO 和 NO2混合加入剛性密閉容器中,發生反應CO(g) +NO2(g) = CO2(g) +NO(g), 測得 c(CO)濃度隨時間t 的變化如表所示。
t/min | 0 | 20 | 90 | 170 | 560 | 1600 | 13200 | 14000 | ∞ |
c(CO)/mol·L-1 | 0.100 | 0.075 | 0.055 | 0.047 | 0.034 | 0.025 | 0.013 | 0.013 | 0.013 |
①300K時反應的平衡轉化率α=_______%。平衡常數K=_______(保留1 位小數)。
②在300K下: 要提高CO轉化率, 可采取的措施是_____________;要縮短反應達到平衡的時間,可采取的措施有______________、____________________。
③實驗測得:反應物濃度按任意比時,該反應的正反應速率均符合v正=k正c2(NO2)。其中:k正為正反應速率常數,是與平衡常數K類似的只受溫度影響的常數。請推理出v逆的表達式:v逆=_____________ (用k正 、 K 與c(CO)、c(CO2 )、c(NO)表達)。
④根據v逆的表達式 ,一定溫度下,當反應達平衡后, t1時刻增大CO濃度, 平衡發生移動,下列圖像正確的是______________。
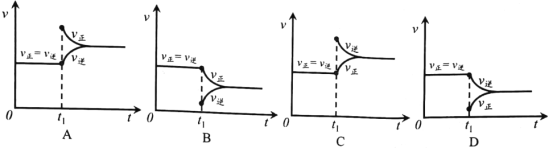
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將2molSO2和1molO2混合置于體積可變,壓強恒定的密閉容器中,在一定溫度下發生如下反應:2SO2(g)+O2(g)![]() 2SO3(g);△H<0,當反應進行到時間t1點時達到平衡狀態,測得混合氣體總物質的量為2.1mol。試回答下列問題:
2SO3(g);△H<0,當反應進行到時間t1點時達到平衡狀態,測得混合氣體總物質的量為2.1mol。試回答下列問題:
(1)反應進行到t1時,SO2的體積分數為__;
(2)若在t1時充入一定量的氬氣(Ar),SO2的物質的量將__(填“增大”、“減小”或“不變”);
(3)若在t1時升溫,重新達到平衡狀態,新平衡混合物中氣體的總物質的量_2.1mol(填“<”、“>”或“=”),簡單說明原因:__。
(4)若t1達到平衡后,保持容器的體積不再變化。再加入0.2molSO2、0.1molO2和1.8molSO3,此時v逆_v正(填“<”、“>”或“=”)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】慶祝新中國成立 70 周年閱兵式上,“東風-41 洲際彈道導彈”“殲 20”等護國重器閃耀亮相,它們都采用了大量合金材料。
回答下列問題:
(1)某些導彈的外殼是以碳纖維為增強體,金屬鈦為基體的復合材料。基態鈦原子的外圍電子排布式為_____。鈦可與 C、N、O 等元素形成二元化合物,C、N、O 元素的電負性由大到小的順序是_________。
(2)鈦比鋼輕,比鋁硬,鈦硬度比鋁大的原因是_____。
(3)鈦鎳合金可用于戰斗機的油壓系統,該合金溶于熱的硫酸生成 Ti(SO4)2、NiSO4,其中陰離子的立體構型為_____,S 的_____雜化軌道與 O 的 2p 軌道形成_____鍵(填 “π”或“σ”)。
(4)金屬鈦采用六方最密堆積的方式形成晶體,其晶胞的俯視圖為_____(填字母序號)。
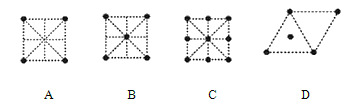
(5)氮化鈦熔點高,硬度大,其晶胞結構如圖所示。
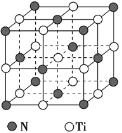
若氮化鈦晶體中 Ti 原子的半徑為 a pm,N 原子的半徑為 b pm,則氮化鈦晶體中原子的空間利用率的計算式為_____(用含 a、b 的式子表示)。碳氮化鈦化合物在航天航空領域有廣泛的應用,其結構是用碳原子代替氮化鈦晶胞頂點的氮原子,則這種碳氮化鈦化合物的化學式為_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下將NaOH溶液添加到己二酸(H2X)溶液中,混合溶液的pH與離子濃度變化的關系如圖所示。下列敘述錯誤的是

A. Ka2(H2X)的數量級為10-6
B. 曲線N表示pH與 的變化關系
的變化關系
C. NaHX溶液中c(H+)>c(OH-)
D. 當混合溶液呈中性時,c(Na+)>c(HX-)>c(X2-)>c(H+)=c(OH-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】酪氨酸是一種生命活動不可缺少的氨基酸,它的結構簡式如下:
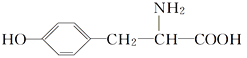
(1)酪氨酸能發生的化學反應類型有________(填字母)。
A.取代反應 B.氧化反應
C.酯化反應 D.中和反應
(2)在酪氨酸的同分異構體中,同時滿足如下三個條件的,除酪氨酸外還有________種。
①屬于氨基酸且“碳骨架”與酪氨酸相同;②與氯化鐵溶液能發生顯色反應;③氨基(—NH2)不與苯環直接相連。
(3)已知氨基酸能與堿反應,寫出酪氨酸與足量的NaOH溶液反應的化學方程式:___________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com