
【題目】鈉和鈉的化合物有許多重要的用途。
(1)碳酸鈉可用于從海水提取溴,涉及的反應如下:3Br2+6Na2CO3+3H2O=5NaBr+NaBrO3+6NaHCO3,在上述反應中用雙線橋法標出電子轉移的方向和數目_______________;該反應中氧化劑與還原劑的物質的量之比是 __________。
(2)少量的鈉應保存在_________中;鈉著火時應采取的滅火措施是_______。
(3)過氧化鈉作潛艇供氧劑時發生的化學反應方程式是__________________;該反應的氧化產物是_____________。
(4)廚房中存放的純堿和小蘇打無法用外觀區別時,請你設計用廚房現有的物質來區分它們的方法_________________。
【答案】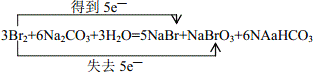 5 :1煤油用沙土撲滅2Na2O2+2CO2=2Na2CO3+O2O2取等量的白醋與兩種物質反應,觀察反應的劇烈程度,反應較劇烈的為小蘇打;另一種則為純堿
5 :1煤油用沙土撲滅2Na2O2+2CO2=2Na2CO3+O2O2取等量的白醋與兩種物質反應,觀察反應的劇烈程度,反應較劇烈的為小蘇打;另一種則為純堿
【解析】
(1)根據3Br2+6Na2CO3+3H2O=5NaBr+NaBrO3+6NaHCO3反應中,溴元素的化合價由0價分別變為-1價和+5價,其它各元素的化合價都不變,溴既是氧化劑又是還原劑,結合元素化合價變化解答該題。
(2)鈉與水反應生成氫氧化鈉和氫氣;根據鈉的密度比水小比煤油大及其性質特別活潑易與水等反應來判斷。
(3)根據過氧化鈉與二氧化碳反應生成碳酸鈉和氧氣,過氧化鈉在反應中既做氧化劑又做還原劑進行分析。
(4)利用純堿和小蘇打與酸反應的快慢來分析。
(1)反應3Br2+6NaOH=5NaBr+NaBrO3+3H2O中,溴元素的化合價由0價分別變為-1價和+5價,溴既是氧化劑又是還原劑,氧化產物是溴酸鈉,還原產物是溴化鈉,由化學方程式可以知道氧化劑和還原劑物質的量之比為5:1,用雙線橋標出電子轉移的方向和數目為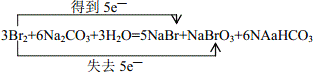 ,
,
因此,本題正確答案是: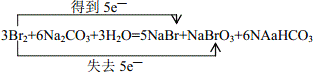 ,5:1。
,5:1。
(2)鈉的性質非常活潑,鈉與水反應生成氫氧化鈉和氫氣,鈉與氧氣反應生成氧化鈉;又因為鈉的密度比水小比煤油大,所以少量的鈉應保存在煤油中;鈉著火時應采取的滅火措施是:用干的沙土滅火;正確答案:煤油;干的沙土滅火。
(3)過氧化鈉和二氧化碳反應生成碳酸鈉和氧氣,該反應為2Na2O2+CO2═2Na2CO3+O2;過氧化鈉中氧元素為-1價,可以升高到0價,可以降低到-2價,因此氧化產物為氧氣;正確答案是:2Na2O2+CO2═2Na2CO3+O2;O2。
(4)因為純堿(碳酸鈉)與酸反應沒有小蘇打(碳酸氫鈉)與酸反應產生的氣泡快,所以廚房里可以用等量的醋滴入兩種固體,產生氣泡快的為小蘇打;正確答案:取等量的白醋與兩種物質反應,觀察反應的劇烈程度,反應較劇烈的為小蘇打;另一種則為純堿。


 靈星計算小達人系列答案
靈星計算小達人系列答案 孟建平錯題本系列答案
孟建平錯題本系列答案科目:高中化學 來源: 題型:
【題目】“封管實驗”具有簡易、方便、節約、綠色等優點,下列關于四個“封管實驗”![]() 夾持裝置未畫出、
夾持裝置未畫出、![]() 固體易升華
固體易升華![]() 的說法正確的是
的說法正確的是
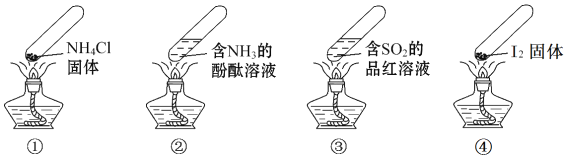
A. 加熱時,![]() 中封管內固體消失
中封管內固體消失
B. 加熱時,![]() 中溶液變紅,冷卻后又變為無色
中溶液變紅,冷卻后又變為無色
C. 加熱時,![]() 中溶液變紅,冷卻后紅色褪去,體現
中溶液變紅,冷卻后紅色褪去,體現![]() 的漂白性
的漂白性
D. 加熱又冷卻的過程中,![]() 屬于物理變化,
屬于物理變化,![]() 屬于化學變化
屬于化學變化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有關物質的轉化關系如下圖所示(部分物質和條件已略去)。A是由兩種元素組成的難溶于水的物質,兩種元素的質量比為7:4;B是強酸;C的摩爾質量為34g·mol-1; F是最常見的無色液體;無色氣體G能使品紅溶液褪色;向含有I的溶液中滴加KSCN溶液,溶液出現血紅色。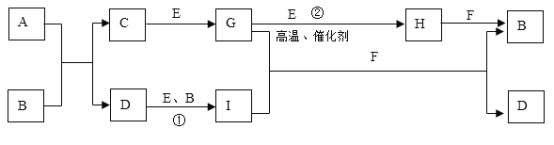
請回答下列問題:
(1)A的化學式____________________________。
(2)C的電子式____________________________。
(3)反應①的離子方程式_______________________________________________________。
(4)反應②的化學方程式_______________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用化學用語解釋相關現象正確的是( )
A. BaSO4的水溶液導電性極弱:BaSO4![]() Ba2++SO42-
Ba2++SO42-
B. 常溫下,0.1mol/L的HF溶液的pH>1:HF+H2O![]() H3O++F-
H3O++F-
C. KHSO4在熔融狀態下可導電:KHSO4=K++H++SO42-
D. 向KI-淀粉溶液中滴加稀硫酸,溶液變藍色:4I-+O2+2H2O=2I2+4OH-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向NaOH和Na2CO3混合溶液中滴加0.1mol/L稀鹽酸,CO2的生成量與加入鹽酸的體積(V)的關系如圖所示。下列判斷正確的是( )

A. 在0-a范圍內,只發生中和反應
B. ab段發生反應的離子方程式為:CO32-+2H+=H2O+CO2↑
C. a=0.3
D. 原混合溶液中NaOH與Na2CO3的物質的量之比為1:2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】R2O8n-在一定條件下可以把 Mn2+氧化為 MnO4-,若反應后 R2O8n-變成 RO42-,又知反應中氧化劑與還原劑的物質的量之比為 5:2,則 R2O8n-中 R 元素的化合價為( )
A. +7 B. +6 C. +3 D. +5
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室用如下裝置制取氯氣,并用氯氣進行實驗。回答下列問題:
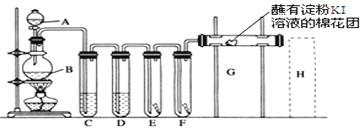
(1)A中盛有濃鹽酸,B中盛有MnO2,寫出反應的離子方程式___________________。
(2)D中放入濃H2SO4其目的是_____________________________。
(3)E中為紅色干布條,F中為紅色濕布條,可觀察到的現象是___________,對比E和F中現象的差異可得出的結論是________________________________。
(4)G處的現象是____________________________________。
(5)用化學方程式寫出H處尾氣吸收裝置中的反應原理____________。
(6)家庭中常用消毒液(主要成分NaClO)與潔廁靈(主要成分鹽酸)清潔衛生。某品牌消毒液包裝上說明如下圖。

①消毒液與潔廁靈不能同時使用,原因是(用離子方程式表示)____________。
②需“密閉保存”的原因____________________________________________。
(7)工業上用亞氯酸鈉和稀鹽酸為原料制備 ClO2 ,寫出反應的化學方程式____________。Cl2和ClO2都是強氧化劑,能殺死水中的病菌。等質量的ClO2的氧化能力是Cl2的_______倍。
(8)氰(CN)2、硫氰(SCN)2的化學性質和鹵素(X2)很相似,化學上稱為擬鹵素,如:[(SCN)2+H2O = HSCN+HSCNO]。它們陰離子的還原性強弱為 Cl-<Br-<CN-<SCN-<I-。試寫出:KBr和KSCN的混合溶液中加入(CN)2,反應的化學方程式為_________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】成環反應在有機合成中具有重要應用,某環狀化合物G的合成過程如下:

(1)A→B為加成反應,則B的結構簡式是______;B→C的反應類型是______.
(2)G中含有的官能團名稱是______;F的化學式為______.
(3)D→E的化學方程式是___________________________________________.
(4)H是F的同分異構體,具有下列結構特征:①核磁共振氫譜除苯環吸收峰外僅有1個吸收峰;②存在甲氧基(CH3O—).H的結構簡式是________________.
(5)由C通過加聚反應合成的高分子化合物M的化學方程式為______.
(6)下列說法正確的是______.
a.A能和HCl反應得到聚氯乙烯的單體
b.D和F中均含有2個π鍵
c.1mol G完全燃燒生成8mol H2O
d.F能發生加成反應、取代反應、氧化反應.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應的離子方程式書寫正確的是( )
A. 碳酸鈣與鹽酸反應:CO32-+2H+=H2O+CO2↑
B. 將氯氣溶于水制備次氯酸:Cl2+H2O =2H++Cl-+ClO-
C. 氫氧化鋇溶液與稀H2SO4 反應:Ba2++SO42-=BaSO4↓
D. 氯化銅溶液與鐵粉反應:Cu2++Fe=Fe2++Cu
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com