
【題目】(1)X、Y兩種主族元素能形成XY2型化合物,已知XY2中共有38個電子,且XY2為常見元素形成的離子化合物,則X、Y在元素周期表中的位置分別為______、_________,用電子式表示該化合物形成過程_____________。
(2)現有a~g 7種短周期元素,它們在周期表中的位置如下,請據此回答下列問題: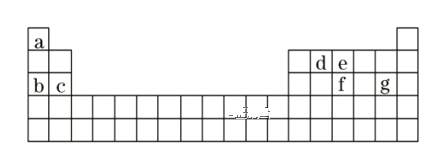
①元素的原子間反應最容易形成離子鍵的是____。
A.c和f B.b和g C.d和g D.b和e
②d與g元素形成的分子中所有原子_____(填“是”或“不是”)都滿足最外層為8電子結構。
(3)X、Y、Z和W代表原子序數依次增大的四種短周期元素,它們滿足以下條件:①元素周期表中,Z與Y相鄰,Z與W也相鄰;②Y、Z和W三種元素的原子最外層電子數之和為17。請填空:
①Y、Z和W三種元素是否位于同一周期(填“是”或“否”):________,理由是________
②X、Y、Z和W可組成一化合物,其原子個數之比為8:2:4:1。寫出該化合物的化學式_______。
【答案】第四周期第ⅡA族 第二周期第ⅦA族 ![]() B 是 否 若三者處于同一周期,則最外層電子數之和不可能為17 (NH4)2SO4
B 是 否 若三者處于同一周期,則最外層電子數之和不可能為17 (NH4)2SO4
【解析】
(1)若XY2為常見元素形成的離子化合物,X為第IIA族元素、Y為第VIIA族元素,其電子數是38,則為CaF2;
(2)根據元素所在周期表中的位置可知,a為H元素、b為Na元素、c為Mg元素,、d為C元素、e為N元素、f為P元素、g為Cl元素;
(3)若Y、Z、W三者處于同一周期或同一主族,最外層電子數之和不可能為17,處于不同周期的Y、Z、W兩兩相鄰,可能出現的位置關系有: 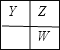 ,
,![]() ,設Y的最外層電子數為x,若為第一種情況,則有x+x+1+x+1=17,解得x=5,Y、Z、W對應的三種元素分別為N、O、S;若為第二種情況,則有x+x+x+1=17,x為分數,不合理,由于Y是N元素,那么X只能是位于其前面的H、He、Li、Be、B五種元素。
,設Y的最外層電子數為x,若為第一種情況,則有x+x+1+x+1=17,解得x=5,Y、Z、W對應的三種元素分別為N、O、S;若為第二種情況,則有x+x+x+1=17,x為分數,不合理,由于Y是N元素,那么X只能是位于其前面的H、He、Li、Be、B五種元素。
(1)若XY2為常見元素形成的離子化合物,X為第IIA族元素、Y為第VIIA族元素,其電子數是38,則XY2為CaF2,用電子式表示CaF2形成過程為![]() ,故答案為:第四周期ⅡA族;第二周期ⅦA族;
,故答案為:第四周期ⅡA族;第二周期ⅦA族;![]() ;
;
(2)①金屬性最強的鈉元素和非金屬性最強的Cl元素最易形成離子鍵,B正確,故答案為:B;
②d與g元素形成的分子為CCl4,CCl4中C元素化合價為+4,C原子最外層電子數為4,所以4+4=8,分子中C原子滿足8電子結構;Cl元素化合價為-1,Cl原子最外層電子數為7,所以|-1|+7=8,分子中Cl原子滿足8電子結構,則CCl4分子中所有原子都滿足最外層為8電子結構,故答案為:是;
(3)①假設Y、Z、W處于同一周期,根據它們的原子序數依次增大,其最外層電子數分別設為x-1、x、x+1,則x-1+x+x+1=17,x為分數,故答案為:否;若三者處于同一周期,則最外層電子數之和不可能為17;
②化合物中硫原子與氧原子個數之比為1:4,為硫酸根,化合物中x原子與氮原子個數之比為4:1,且x的原子序數比氮原子小,可為銨根離子,所以該化合物為硫酸銨,故答案為:(NH4)2SO4。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】容積固定為3 L的某密閉容器中加入1 mol A、2 mol B,一定溫度下發生如下反應:A(s)+2B(g)![]() C(g)+D(g),經反應5 min后,測得C的濃度為0.3 mol·L-1。則下列說法中正確的是
C(g)+D(g),經反應5 min后,測得C的濃度為0.3 mol·L-1。則下列說法中正確的是
A. 5 min內D的平均反應速率為0.02 mol·L-1·min-1
B. 5 min內A的平均反應速率為0.06 mol·L-1·min-1
C. 經5 min后,向容器內再加入C,正反應速率變小
D. 平衡狀態時,生成1 mol D時同時生成1 mol A
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】青蒿素是一種用于治療瘧疾的藥物,挽救了全球特別是發展中國家數百萬人的生命,它的分子式為C15H22O5。NA表示阿伏伽德羅常數,下列關于青蒿素的說法不正確的是( )
A.青蒿素的摩爾質量等于282![]() B.14.1g青蒿素中含氧原子數目為0.05NA
B.14.1g青蒿素中含氧原子數目為0.05NA
C.1mol青蒿素完全燃燒,生成11NA個H2OD.10g青蒿素中![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有1L未知成分的混合溶液,其中除了含有0.2mol/L的Na+外,還可能含有下列離子中的一種或幾種:
![]()
現進行如下實驗操作(每次實驗所加試劑均過量):
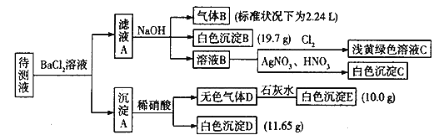
已知:①![]() ,②
,②![]() ,Cl2在常溫下為黃綠色氣體,可溶于水,其水溶液為淺黃綠色;Br2在常溫下是深紅棕色液體,微溶于水,其水溶液為黃色。
,Cl2在常溫下為黃綠色氣體,可溶于水,其水溶液為淺黃綠色;Br2在常溫下是深紅棕色液體,微溶于水,其水溶液為黃色。
(1)由氣體B可確定待測液中含有的離子是____________。
(2)由沉淀D和沉淀E可以判斷待測液中一定含有_____離子,據此可以排除的離子是_____。
(3)由白色沉淀B可確定待測液中含有的離子是____,寫出產生沉淀B的離子方程式_______。
(4)某同學讀圖后,認為待測液中一定不含Br—,他的判斷依據是______。
(5)綜合分析,待測液中![]() 的物質的量濃度的取值范圍為________。
的物質的量濃度的取值范圍為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
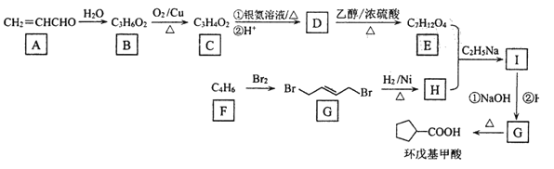
【題目】某研究小組以鏈燒烴 (C4H6) 和丙烯醛( CH2= CHCHO) 為原料合成某藥物中間體環戊基甲酸(部分反應條件、產物已省略),其流程如下:
已知:i.![]() +2RBr
+2RBr 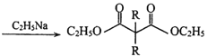 +2HBr
+2HBr
ii. ![]() +2CO2
+2CO2
請回答下列問題:
(1) B中的官能團名稱為________,D→E的反應類型是 ____________ .
(2)寫出C與銀氨溶液反應的化學方程式①:_____________ 。
(3)一定條件下,H可制取F, 則所需試劑和反應條件是____________________ 。
(4) I的結構簡式為______________。
(5)環戊基甲酸與苯酚反應生成一種酯X,寫出一種同時符合以下條件的 X 的同分異構體的結構簡式:________(不考慮立體異構)。
①核磁共振氫譜有四組峰,峰面積比為9:2:2:l
②能與FeCl3發生顯色反應
③與濃溴水反應時,l molX可消耗4mol Br2
(6)參照上述合成路線,設計以乙醇和化合物E為原料制備2.2-二乙基丙二酸(結構簡式: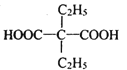 )的合成路線(無機試劑任選):___________________。
)的合成路線(無機試劑任選):___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表為元素周期表的一部分,請參照元素①~⑨在表中的位置,用化學用語回答下列問題:
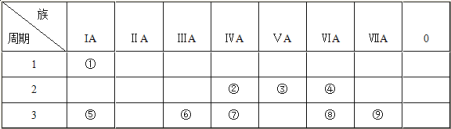
(1)④、⑤、⑧三種元素中,離子半徑由大到小的順序為____(填離子符號)。
(2)②、⑦、⑧的最高價含氧酸的酸性由強到弱的順序是_______ (填化學式)。⑧和⑨元素的氣態氫化物穩定性順序為__________。
(3)⑥單質與⑤的最高價氧化物的水化物反應的離子方程式為____。
(4)①、④、⑤、⑨四種元素中,某些元素間可形成既含離子鍵又含極性共價鍵的化合物,寫出其中一種化合物的電子式________。
(5)元素⑤與元素④能形成原子個數比為1:1的化合物Y,Y在常溫下為固態,焰色反應為黃色,Y與②的最高價氧化物反應的化學方程式為_________。
(6)能說明⑧的非金屬性比⑨的非金屬性______(填“強”或“弱”)的事實是__________(用離子方程式說明)。
(7)①和③形成的18電子的化合物甲是一種應用廣泛的化工原料,寫出甲的電子式____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有下列三個反應:
①Cl2+FeI2=FeCl2+I2
②2Fe2++Br2=2Fe3++2Br-
③Co2O3+6HCl=2CoCl2+Cl2↑+3H2O
下列說法正確的是( )
A. 反應①②③中的氧化產物分別是I2、Fe3+、CoCl2
B. 根據以上方程式可以得到氧化性:Cl2>Fe3+>Co2O3
C. 在反應③中當1 mol Co2O3參加反應時,2 mol HCl被氧化
D. 可以推理得到Cl2+FeBr2 =FeCl2+Br2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】治理大氣和水體污染對建設美麗家鄉,打造宜居環境具有重要意義。
(1)![]() 泄漏會導致人體中毒,用于檢測
泄漏會導致人體中毒,用于檢測![]() 的傳感器的工作原理如圖所示:
的傳感器的工作原理如圖所示:

①寫出電極Ⅰ上發生的反應式:__________
②工作一段時間后溶液中![]() 的濃度__________(填“變大”、“變小”或“不變”)
的濃度__________(填“變大”、“變小”或“不變”)
(2)用![]() 氧化
氧化![]() 制取
制取![]() ,可提高效益,減少污染。反應為:
,可提高效益,減少污染。反應為:![]() ,通過控制條件,分兩步循環進行,可使
,通過控制條件,分兩步循環進行,可使![]() 轉化率接近100%,其原理如圖所示:
轉化率接近100%,其原理如圖所示:

過程Ⅰ的反應為:![]()
過程Ⅱ反應的熱化學方程式(![]() 用含有
用含有![]() 和
和![]() 的代數式表示)__________。
的代數式表示)__________。
(3)在溫度![]() ,容積為
,容積為![]() 的絕熱容器中,充入
的絕熱容器中,充入![]() ,發生反應:
,發生反應:![]() ,容器中
,容器中![]() 的相關量隨時間變化如圖所示。
的相關量隨時間變化如圖所示。

①反應到![]() 時,
時,![]() 的轉化率是__________。
的轉化率是__________。
②根據圖示,以下各點表示反應達到平衡狀態的是________。
a.![]() b.
b.![]() c.
c.![]() d.
d.![]()
③![]() 內容器中
內容器中![]() 的反應速率增大,而
的反應速率增大,而![]() 后容器中
后容器中![]() 的反應速率減小了,原因是_______。
的反應速率減小了,原因是_______。
④此容器中反應達平衡時,溫度若為![]() ,此溫度下的平衡常數
,此溫度下的平衡常數![]() =__________。
=__________。
(4)工業上可用![]() 溶液吸收法處理
溶液吸收法處理![]() ,25℃時用
,25℃時用![]() 的
的![]() 溶液吸收
溶液吸收![]() ,當溶液
,當溶液![]() 時,溶液中各離子濃度的大小關系為:
時,溶液中各離子濃度的大小關系為:![]() 。(已知25℃時:
。(已知25℃時:![]() 的電離常數
的電離常數![]() ,
,![]() )請結合所學理論通過計算說明
)請結合所學理論通過計算說明![]() 的原因__________。
的原因__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學研究性學習小組的同學根據理論分析后認為,NO2可能會氧化單質銅,他們設想利用下圖所示裝置驗證NO2的氧化性(夾持裝置已省略)。

(1)裝置A~C中有一處錯誤,改正的方法是________,A中發生反應的兩種試劑通常是_____。
(2)點燃C處酒精燈比較合適的時機是_________。若C中固體全部變成黑色,同時生成對環境無污染的氣體,寫出C中反應的化學方程式:_____。裝置D的用途是__________。
(3)開關K的設計是以實現綠色化學實驗為目的,請說明K的使用方法:_______(包括使用時段與內容)。
(4)實驗結束后發現C中的固體混有少量的紅色粉末,經過分析,甲同學認為該紅色粉末是Cu2O,乙同學認為該紅色粉末是Cu,丙同學認為該紅色粉末是Cu和Cu2O的混合物。查閱資料,Cu、Cu2O和CuO的部分性質如下:

請設計一個簡單的實驗證明甲同學的看法是否正確:__________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com