
【題目】(1)實驗室用濃鹽酸和二氧化錳反應制取氯氣時,反應為4HCl(濃)+MnO2![]() MnCl2+Cl2↑+2H2O收集到7.1g氯氣,求:
MnCl2+Cl2↑+2H2O收集到7.1g氯氣,求:
①發生反應的二氧化錳的物質的量是多少?
②被氧化的氯化氫的物質的量是多少?
(2)把5.1g鎂鋁合金粉末放入500mL 1mol/L鹽酸中,恰好完全反應。試計算:
①該合金中鎂和鋁的物質的量各為多少mol。
②將等質量的該合金投入足量的氫氧化鈉溶液中,求標況下放出氣體的體積。
【答案】
(1)①0.1mol;②0.2mol;
(2)①0.1 mol;0.1 mol;②3.36L
【解析】
試題分析:
(1)① MnO2+4HCl(濃)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
1 mol 71 g
n(MnO2) 7.1 g
n(MnO2)=![]() =0.1 mol
=0.1 mol
②被氧化的HCl的物質的量等于被氧化的Cl-的物質的量。
MnO2+2Cl-+4H+![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
2mol 71 g
n(Cl-) 7.1 g
n(Cl-)=![]() =0.2 mol,所以被氧化的HCl的物質的量為0.2mol。
=0.2 mol,所以被氧化的HCl的物質的量為0.2mol。
(2)① 設此合金中含![]() 的物質的量為
的物質的量為![]() ,
,![]() 的物質的量為
的物質的量為![]() ,則有
,則有![]() ①
①
500mL1mol·L-1鹽酸中含![]() 的物質的量為
的物質的量為![]() ,又由下列反應的方程式得
,又由下列反應的方程式得
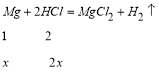
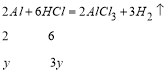
與此合金恰好反應的![]() 的量為
的量為![]() ②
②
由①②得![]()
即該合金中含有鎂和鋁的物質的量均為![]()
②合金中的![]() 不與
不與![]() 反應,
反應,![]() 與
與![]() 的反應方程式如下:
的反應方程式如下:

則有![]() ,解得
,解得![]() ,標準狀況下其體積為
,標準狀況下其體積為![]() 。
。


 全能練考卷系列答案
全能練考卷系列答案科目:高中化學 來源: 題型:
【題目】物質的量是高中化學中常用的物理量,請完成以下有關其內容的計算:
(1)標準狀況下,含有相同氧原子數的CO與CO2的體積之比為____________。
(2)等溫等壓下,等體積的O2和O3所含分子個數比為______________,原子個數比為______________,質量比為___________。
(3)設NA為阿伏加德羅常數的數值,如果a g某氣中含有的分子數為b,則c g某氣在標準狀況下的體積約是___________。 (用含NA的式子表示).
(4)配制100mL 1molL-1的稀H2SO4溶液,需要用量筒量取濃H2SO4(密度為1.84gmL-1,質量分數為98%)的體積為__________ mL.
(5)100 mL 某Al2(SO4)3溶液中,n(Al3+)=0.20 mol,則其中c(SO42-)= _________mol/L。
(6)某氯化鎂溶液的密度為1.18g/cm3,其中鎂離子的質量分數5.6%,300mL該溶液中Cl-的物質的量等于_________ .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】同溫同壓下,分子數相同的CO和CO2 , 下列說法正確的是( )
A.密度之比為7:11
B.體積之比為11:7
C.物質的量之比為7:11
D.質量之比為11:7
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A.在標準狀況下,1mol水和1molH2的體積都約是22.4L
B.2gH2和44gCO2的體積相等
C.1mol某氣體的體積為22.4L,則該氣體一定處于標準狀況
D.在標準狀況下,1gH2和11.2LO2的物質的量相等
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列除去雜質的方法正確的是
①除去乙烷中少量的乙烯:光照條件下通入Cl2,氣液分離
②除去乙炔中少量的H2S:氣體通過盛有硫酸銅溶液的洗氣瓶
③除去C2H6中少量的C2H4:氣體通過盛有酸性高錳酸鉀溶液的洗氣瓶
④除去乙醇中少量的乙酸:加足量新制生石灰,蒸餾
A. ②④ B. ①② C. ③④ D. ②③
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】關于粗鹽提純的下列說法正確的是
A.溶解粗鹽時,應多加水盡量使溶液稀些,防止食鹽溶解不完全
B.濾去不溶性雜質以后,將濾液移至坩堝內加熱濃縮
C.當蒸發到剩有少量溶液時,停止加熱,利用余熱將液體蒸干
D.當制得的晶體轉移到新制過濾器中用大量水進行洗滌
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列表格中各項分類都正確的一組是( )
純凈物 | 混合物 | 電解質 | 非電解質 | |
A | 冰水混合物 | CuSO45H2O | 液態KNO3 | 蔗糖 |
B | CaO | 海水 | 銅 | 酒精 |
C | 液氯 | 鋁合金 | AgCl | CO2 |
D | 氫氧化鈉 | 空氣 | Na2SO4溶液 | 食醋 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】從海水中提取蒸餾水、溴、食鹽過程過如下:
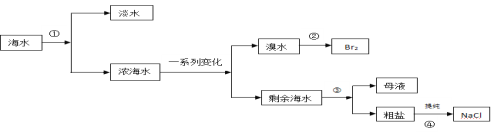
(1)從海水中獲取淡水的方法實驗操作是 ,需要的玻璃儀器有:酒精燈、溫度計、牛角管、冷凝管、 。
(2)從溴水中獲得單質溴時,采用的方法是萃取、 、蒸餾。操作是 、過濾。
下列可選作萃取劑的是
A.酒精 B.苯 C.CCl4
(3)粗鹽含有Ca2+、Mg2+、SO42-等離子,為除去以上雜質離子,可加入①Na2CO3溶液②BaCl2溶液NaOH溶液④過濾⑤稀鹽酸。錯誤的操作順序是
A.①②③④⑤ B. ②①③④⑤ C.③②①④⑤ D. ②③①④⑤
(4)實驗室用上述方法制得的NaCl配制240ml 0.1mol/LNaCl溶液。需要用托盤天平稱量NaCl固體 g。配制時,一般可分為以下幾個步驟:①稱量②計算③溶解④搖勻⑤轉移⑥洗滌⑦定容⑧冷卻。其正確的操作順序為 。
配制過程中,下列情況會使配制結果偏高的是(填序號)
①定容時俯視刻度線觀察液面
②容量瓶使用時未干燥
③定容后經振蕩、搖勻、靜置,發現液面低于刻度線,再加蒸餾水補至刻度線
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com