
 C(g) +3D(g) △H<0。該可逆反應的反應速率—時間、轉化率—時間關系圖如下,下列分析中錯誤的是( )
C(g) +3D(g) △H<0。該可逆反應的反應速率—時間、轉化率—時間關系圖如下,下列分析中錯誤的是( )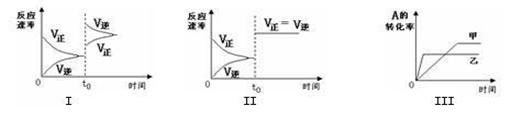
| A.圖I可體現t0時升高溫度對反應速率的影響 |
| B.圖II可體現t0時增大壓強(縮小體積)或使用催化劑對反應速率的影響 |
| C.圖III可體現溫度對化學平衡的影響,且乙的溫度較高 |
| D.圖III可體現催化劑對化學平衡的影響,且甲使用了催化劑 |
科目:高中化學 來源:不詳 題型:填空題
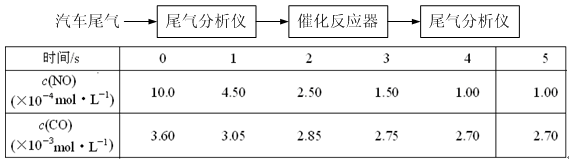
 CO2 (g) 十 H2 (g) ; △H<0
CO2 (g) 十 H2 (g) ; △H<0
 CO2 (g) + H2 (g)的平衡濃度符合c(CO2)·c(H2)=2 c(CO)·c(H2O),則t2℃ 850℃,判斷依據是:
CO2 (g) + H2 (g)的平衡濃度符合c(CO2)·c(H2)=2 c(CO)·c(H2O),則t2℃ 850℃,判斷依據是: 查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題

查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
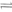 2c(g),△H<0;達到平衡后,改變一個條件(X),下列量(Y)的變化一定符合圖中曲線的是
2c(g),△H<0;達到平衡后,改變一個條件(X),下列量(Y)的變化一定符合圖中曲線的是| | X | Y |
| A | 再加入B | B的轉化率 |
| B | 再加入C | A的體積分數 |
| C | 增大壓強 | A的轉化率 |
| D | 升高溫度 | 混合氣體平均摩爾質量 |

查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題

 Fe(SCN)2+ 來檢驗反應是否產生鐵離子。已知在一定溫度下該反應達到平衡時c(Fe3+)="0.04" mol/L,c(SCN—)=0.1mol/L,c[Fe(SCN)2+]=0.68mol/L,則此溫度下該反應的平衡常數K= 。
Fe(SCN)2+ 來檢驗反應是否產生鐵離子。已知在一定溫度下該反應達到平衡時c(Fe3+)="0.04" mol/L,c(SCN—)=0.1mol/L,c[Fe(SCN)2+]=0.68mol/L,則此溫度下該反應的平衡常數K= 。查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
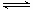 2C(g)。若經2 s后測得C的濃度為0.6 mol·L-1,現有下列幾種說法:
2C(g)。若經2 s后測得C的濃度為0.6 mol·L-1,現有下列幾種說法:| A.①③ | B.①④ | C.②③ | D.③④ |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
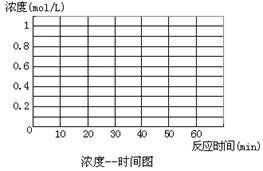
 B + D在不同條件下進行,B、D的起始濃度為0,把反應物A的濃度(mol/L)隨反應時間(min)的變化情況如下表所示。
B + D在不同條件下進行,B、D的起始濃度為0,把反應物A的濃度(mol/L)隨反應時間(min)的變化情況如下表所示。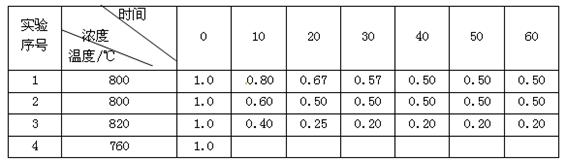
 www.k@s@5
www.k@s@5 @u.com
@u.com 查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.實驗室用排水法收集氯氣時用飽和食鹽水代替水以減少氯氣的溶解 |
| B.氫氣、碘蒸氣、碘化氫氣體組成的平衡體系加壓后顏色變深 |
| C.實驗室保存硫酸亞鐵溶液時加入幾枚鐵釘以防止試劑變質 |
| D.在二氧化硫的催化氧化反應中,通入過量的空氣以提高二氧化硫的轉化率 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com