
已知可逆反應:CO(g)+H2O(g)![]() CO2(g)+H2(g)(正反應為放熱反應),在850℃時,其化學平衡常數K=1.
CO2(g)+H2(g)(正反應為放熱反應),在850℃時,其化學平衡常數K=1.
(1)若升高溫度到950℃時,達到平衡時K________1(填“大于”、“小于”或“等于”).
(2)850℃時,若向一容積可變的密閉容器中同時充入1.0mol CO,3.0mol H2O,1.0mol CO2和x mol H2,則:①當x=5.0時,上述平衡向________(填“正反應”或“逆反應”)方向進行.
②若要使上述反應開始時向正反應方向進行,則x應滿足的條件是________.
(3)在850℃時,若設x=5.0和x=6.0,其他物質的投料不變,當上述反應達到平衡后,測得H2的體積分數分別為a%和b%,則a________b(填“大于”、“小于”或“等于”).
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| X | ||
| Y | Z |
| 溫度/℃ | 500 | 700 | 850 | 1 000 |
| 平衡常數 | 2.5 | 1.7 | 1.0 | 0.6 |
查看答案和解析>>
科目:高中化學 來源:101網校同步練習 高二化學 山東科學技術出版社 魯教版 題型:038
已知可逆反應:CO+H2O![]() CO2+H2,達到平衡時,K=[CO2][H2]/[CO][H2O],K是常數,只與溫度有關,與濃度無關.
CO2+H2,達到平衡時,K=[CO2][H2]/[CO][H2O],K是常數,只與溫度有關,與濃度無關.
(1)830 K時,若起始時,CO為2 mol·L-1,H2O為3 mol·L-1,平衡時CO的轉化率為60%,計算水蒸氣的轉化率及K值.
(2)830 K,若只將起始時H2O改為6 mol·L-1,計算水蒸氣的轉化率.
(3)若830 K時,CO起始濃度為a mol·L-1,H2O起始濃度為b mol·L-1,H2濃度為c mol·L-1:
計算:①a、b、c的關系式
②當a=b時,a=________c
查看答案和解析>>
科目:高中化學 來源: 題型:
 CO2(g)+H2(g),達到平衡時,K=
CO2(g)+H2(g),達到平衡時,K=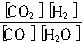 ,K是常數,只與溫度有關,與濃度無關。
,K是常數,只與溫度有關,與濃度無關。查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com