
【題目】在25’C時,密閉容器中X、Y、Z三種氣體的初始濃度和平衡濃度如下表:
物質 | X | Y | Z |
初始濃度/mol/L | 0.1 | 0.2 | 0 |
平衡濃度/mol/L | 0. 05 | 0. 05 | 0.1 |
下列說法錯誤的是
A. 反應達衡時,X的轉化率為50%
B. 反應可表示為X+3Y![]() 2Z,其平衡常數為1600
2Z,其平衡常數為1600
C. 增大壓強使平衡向生成Z的方向移動,平衡常數增大
D. 改變溫度可以改變此反應的平衡常數
科目:高中化學 來源: 題型:
【題目】在一定溫度下的定容容器中,發生反應:3B(s)![]() 2C(g)+D(g),下列描述中能表明反應已達到平衡狀態的是
2C(g)+D(g),下列描述中能表明反應已達到平衡狀態的是
①混合氣體的壓強不變②混合氣體的密度不變③C(g)的物質的量濃度不變④容器內C、D三種氣體的濃度之比為2:1⑤單位時間內生成n molD,同時生成2n mol C.⑥單位時間內生成2n molC,同時消耗n mol D.⑦混合氣體中C的體積分數不變
A. ①②③ B. ③④⑥ C. ①②③⑥⑦ D. ①②③⑥
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】 38.4g銅跟適量的濃硝酸反應,銅完全作用后,共收集到氣體22.4L(標準狀況),反應消耗的HNO3的物質的量可能是
A.1.0molB.1.6 molC.2.2 mol D.2.4 mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】從經濟效益和環境保護的角度考慮,大量制取硝酸銅最宜采用的方法是( )
A.Cu+HNO3(濃)→Cu(NO3)2
B.Cu+HNO3(稀)→Cu(NO3)2
C.Cu ![]() CuO
CuO ![]() Cu(NO3)2
Cu(NO3)2
D.Cu ![]() CuSO4
CuSO4 ![]() Cu(NO3)2
Cu(NO3)2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對增生性瘢痕早期進行 ![]() Sr(鍶)干預可取得較好效果.下列說法正確的是( )
Sr(鍶)干預可取得較好效果.下列說法正確的是( )
A.Sr為于第4周期ⅡA 族
B.![]() Sr核內中子數與質子數之差為14
Sr核內中子數與質子數之差為14
C.![]() Sr與
Sr與 ![]() Y互為同位素
Y互為同位素
D.![]() Sr的核內質子數為38,Sr元素的相對原子質量為90
Sr的核內質子數為38,Sr元素的相對原子質量為90
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】可逆反應aA(g)+bB(s)![]() cC(g)+dD(g),其他條件不變,C的物質的量分數和溫度(T)或壓強(P)關系如圖,其中正確的是( )
cC(g)+dD(g),其他條件不變,C的物質的量分數和溫度(T)或壓強(P)關系如圖,其中正確的是( )

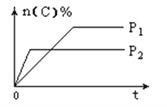
A. 升高溫度,平衡向正反應方向移動 B. 使用催化劑,C的物質的量分數增加
C. 化學方程式系數a<c+d D. 根據圖象無法確定改變溫度后平衡移動方向
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關金屬腐蝕的認識中正確的是
A.金屬被腐蝕時發生的全部是氧化還原反應
B.金屬腐蝕可以分為化學腐蝕和電化腐蝕,只有化學腐蝕是氧化還原反應
C.防止鋼鐵被腐蝕不需要避免它受潮
D.鋼鐵發生腐蝕時以發生化學腐蝕為主
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為了防止槍支生銹,常將槍支的鋼鐵零件放在NaNO2和NaOH的混合溶液中進行化學處理使鋼鐵零件表面生成Fe3O4的致密的保護層——“發藍”。其過程可用下列化學方程式表示:
①3Fe+NaNO2+5NaOH===3Na2FeO2+H2O+NH3↑
②![]() Na2FeO2+
Na2FeO2+![]() NaNO2+
NaNO2+![]() H2O―→
H2O―→![]() Na2Fe2O4+
Na2Fe2O4+![]() NH3↑+
NH3↑+![]() NaOH
NaOH
③Na2FeO2+Na2Fe2O4+2H2O![]() Fe3O4+4NaOH
Fe3O4+4NaOH
請回答下列問題:
(1)配平化學方程式②,各物質前的化學計量數依次為_____________。
(2)上述反應①中氧化劑為______,被氧化的物質是______。若有2 mol Na2FeO2生成,則反應①中有________mol電子發生轉移。
(3)關于“發藍”的過程,下列說法不正確的是________(填字母)。
A.該過程不會產生污染
B.反應③生成的四氧化三鐵具有抗腐蝕作用
C.反應①②③均是氧化還原反應
D.反應①②中的氧化劑均為NaNO2
(4)當混合溶液中NaOH濃度過大,“發藍”的厚度會變小,其原因是________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com