
【題目】華為研發人員利用鋰離子能在石墨烯表面和電極之間快速大量穿梭運動的特性,開發出石墨烯電池,電池反應式為LixC6+Li1﹣xCoO2C6+LiCoO2,其主要優勢在于使用壽命長和充電速度快,其工作原理如圖所示。下列關于該電池的說法錯誤的是( )

A.該電池若用隔膜,可選用陽離子交換膜
B.充電時,陰極反應為C6+xLi++xe﹣=LixC6
C.放電時,LiCoO2極發生的電極反應為:LiCoO2﹣xe﹣=Li1﹣xCoO2+xLi+
D.廢舊的該電池進行“放電處理”,讓Li+嵌入 LiCoO2中有利于回收石墨烯
【答案】C
【解析】
根據電池反應式及圖示可知,負極反應為:LixC6 - xe﹣=C6+xLi+,正極反應為:Li1﹣xCoO2+xLi++ xe﹣=LiCoO2,充電時,陰陽極電極反應與負極正極反應式正好相反,據此分子判斷。
A.根據圖知,鋰離子需要自由移動,所以需要陽離子交換膜,A項正確,不符合題意;
B.充電時,陰極上得電子發生還原反應,電極反應式為C6+xLi++xe﹣=LixC6,B項正確,不符合題意;
C.放電時,LiCoO2極得電子發生還原反應,發生的電極反應為:Li1﹣xCoO2+xLi++xe﹣=LiCoO2,C項錯誤,符合題意;
D.放電石墨烯為負極反應式為LixC6﹣xe﹣=C6+xLi+,所以放電處理讓 Li+從石墨烯中脫出而有利于回收,D項正確,不符合題意;
答案選C。


 孟建平小學滾動測試系列答案
孟建平小學滾動測試系列答案 黃岡天天練口算題卡系列答案
黃岡天天練口算題卡系列答案科目:高中化學 來源: 題型:
【題目】在一定溫度下的定容密閉容器中,發生反應:![]() 。當下列所給有關量不再變化時,不能表明該反應已達平衡狀態的是
。當下列所給有關量不再變化時,不能表明該反應已達平衡狀態的是![]()
![]()
A.混合氣體的壓強B.混合氣體的密度
C.混合氣體的平均相對分子質量D.![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】反應CO(g)+2H2(g)![]() 2CH3OH(g)在恒容密閉容器中進行。為探究溫度、CO2等因素對該反應的影響,進行了4組實驗,結果如右下表。下列說法不正確的是
2CH3OH(g)在恒容密閉容器中進行。為探究溫度、CO2等因素對該反應的影響,進行了4組實驗,結果如右下表。下列說法不正確的是
組序號 | 1 | 2 | 3 | 4 | |
反應溫度/℃ | 225 | 235 | 225 | 235 | |
反應前氣體的物質的量/mol | CO2 | 0 | 0 | 0.2 | 0.2 |
CO | 3.0 | 3.0 | 2.8 | 2.8 | |
H2 | 7.0 | 7.0 | 7.0 | 7.0 | |
平衡時CH3OH的體積分數/% | 4.9 | 8.8 | 36.5 | 50.7 | |
A.該反應的△H>0
B.當容器中壓強不變時,反應達到平衡
C.CH3OH含量增大的原因是CO2
D.少量CO2能提高平衡時CH3OH的體積分數
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】過碳酸鈉(Na2CO4)是一種很好的供氧劑,其與稀鹽酸發生反應的化學方程式為2Na2CO4+4HCl=4NaCl+2CO2↑+O2↑+2H2O。市售過碳酸鈉一般都含有碳酸鈉,為測定某過碳酸鈉樣品(只含Na2CO4和Na2CO3)的純度,某化學興趣小組采用以下方案實施:
按如圖組裝好實驗裝置,Q為一可鼓脹收縮的塑料氣袋,取適量樣品于其中,打開分液漏斗活塞,將稀鹽酸滴人氣袋中至充分反應。

(1)為測定反應生成氣體的總體積滴稀鹽酸前必須關閉______打開____(均填“K1”、“K2”或“K3”),導管A的作用是________。
(2)當上述反應停止后,使K1、K3處于關閉狀態,K2處于打開狀態,再緩緩打開K1。B中裝的固體試劑是_________,為什么要緩緩打開K1?________。
(3)實驗結束時,裝置內的氣體同溫同壓,測得量筒I中有x mL水,量筒Ⅱ中收集到了y mL氣體,則樣品中過碳酸鈉的質量分數是_______(用含有x、y的代數式表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】病人輸液用的葡萄糖注射液是葡萄糖(C6H12O6)的水溶液,其標簽上的部分內容如圖所示,下列說法錯誤的是( )

A.配制400mL上述溶液可選用500mL容量瓶
B.該注射液中葡萄糖的物質的量濃度為0.01molL﹣1
C.該注射液為一種分散系,但不能產生丁達爾現象
D.可用新制氫氧化銅懸濁液檢驗人體尿液中是否含有葡萄糖
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)現有下列7種有機物:
①CH4 ②CH3C≡CCH3 ③ ④
④ ⑤
⑤ ⑥
⑥![]() ⑦
⑦
請回答:
其中屬于醇類的是___(填序號,下同),互為同系物的是___,能與金屬鈉反應的有___,互為同分異構體的是___。
(2)肉桂酸甲酯由C、H、O三種元素組成,已知其相對分子質量為162,核磁共振氫譜顯示有6個峰,其面積之比為1︰2︰2︰1︰1︰3,利用紅外光譜儀檢測其中的某些基團,測得紅外光譜如圖,則肉桂酸甲酯的結構簡式是___(不考慮立體異構)。

(3)碳原子數不大于10的烷烴中一氯代物只有一種結構的物質有___種。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】儲氫納米碳管的研制成功體現了科技的進步。用電弧法合成的納米碳管常伴有大量的雜質碳納米顆粒,這種碳納米顆粒可用氧化氣化法提純,此反應中的反應物和生成物有C、CO2、H2SO4、K2Cr2O7、Cr2(SO4)3、K2SO4、H2O七種物質。
(1)若將碳納米顆粒分散到一定溶劑中,形成穩定的分散系,其所具有的性質是__________。
①丁達爾效應 ②加入飽和(NH4)2SO4溶液產生聚沉 ③可通過半透膜
(2)請用上述物質填空,并配平化學方程式:____C+____+____H2SO4→____K2SO4+________+____Cr2(SO4)3+____H2O。
(3)H2SO4在上述反應中表現出來的性質是________(填選項編號)。
A.氧化性 B.氧化性和酸性
C.酸性 D.還原性和酸性
(4)若反應中電子轉移了0.8 mol,則產生的氣體在標準狀況下的體積為____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某烴A蒸汽的密度是相同狀況下氫氣密度的36倍,已知該烴中碳、氫元素的質量比為5:1,回答下列問題:
(1)該烴的相對分子質量為__________________。
(2)該烴的分子式為__________________。
(3)該烴有____________種結構。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】決定物質性質的重要因素是物質結構。請回答下列問題:
(1)已知元素M是組成物質Ca5(PO4)3F的一種元素。元素M的氣態原子逐個失去第1個至第5個電子所需能量(即電離能,用符號I1至I5表示)如表所示:
I1 | I2 | I3 | I4 | I5 | |
電離能 | 589.8 | 1145.4 | 4912.4 | 6491 | 8153 |
元素M化合態常見化合價是_________價,其基態原子電子排布式為_________。
(2)Ca3(PO4)3F中非金屬元素電負性由大到小的順序為_________。
(3)PO43-的中心原子的雜化方式為_________,該離子的空間構型為_________,鍵角為________,其等電子體有_________ (請寫出兩種)。
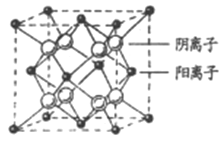
(4)CaF2晶胞結構如圖所示,則CaF2晶體中與Ca2+最近且等距離的Ca2+數目為_________;已知Ca2+和F半徑分別為a cm、b cm,阿伏加德羅常數為NA,M為摩爾質量,則晶體密度為________g·cm3(不必化簡)。
(5)已知MgO與CaO的晶體結構相似,其摩氏硬度的大小關系為_________,原因為___________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com