
| A. | Ca2+、Al3+、HCO3-、Cl- | B. | K+、Ba2+、Cl-、NO3- | ||
| C. | Na+、AlO2-、OH-、SO42- | D. | Na+、NH4+、Cl-、K+ |
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | AgCl在飽和NaCl溶液中的Ksp比在純水中的Ksp小 | |
| B. | 向AgCl的懸濁液中滴加濃氨水,沉淀溶解,說明AgCl的溶解平衡向右移動 | |
| C. | 將0.001 mol•L-1AgNO3溶液滴入0.001 mol•L-1的KCl和0.001 mol•L-1的K2CrO4溶液中先產生Ag2CrO4沉淀 | |
| D. | 向AgCl的懸濁液中加入NaBr溶液,白色沉淀轉化為淡黃色,說明Ksp(AgCl)<Ksp(AgBr) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③④ | B. | ①②④ | C. | ①②③④ | D. | ①②③⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
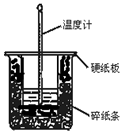 50mL 0.50mol•L-1鹽酸與50mL 0.55mol•L-1NaOH溶液在圖示的裝置中進行中和反應.通過測定反應過程中所放出的熱量可計算中和熱.回答下列題:
50mL 0.50mol•L-1鹽酸與50mL 0.55mol•L-1NaOH溶液在圖示的裝置中進行中和反應.通過測定反應過程中所放出的熱量可計算中和熱.回答下列題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 3個 | B. | 4個 | C. | 5個 | D. | 6個 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
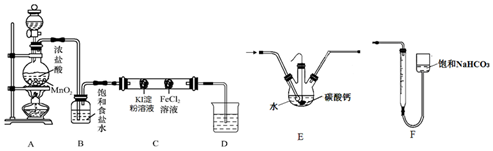
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com