
【題目】溴乙烷在不同溶劑中與NaOH發生不同類型的反應,生成不同的反應產物。
某同學依據溴乙烷的性質,用如圖實驗裝置(鐵架臺、酒精燈略)驗證取代反應和消去反應的產物,請你一起參與探究。
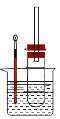
實驗操作Ⅰ:在試管中加入5 mL 1 mol/L NaOH溶液和5 mL 溴乙烷,振蕩。
實驗操作II:將試管如圖固定后,水浴加熱。
(1)用水浴加熱而不直接用酒精燈加熱的原因是_______________________________。
(2)觀察到_________________________現象時,表明溴乙烷與NaOH溶液已完全反應。
(3)鑒定生成物中乙醇的結構,可用的波譜是_________________________________。
(4)為證明溴乙烷在NaOH乙醇溶液中發生的是消去反應,在你設計的實驗方案中,需要檢驗的是______________________,檢驗的方法是_____________(需說明:所用的試劑、簡單的實驗操作及預測產生的實驗現象)。
【答案】溴乙烷沸點低,減少溴乙烷的損失 試管內溶液靜置后不分層 紅外光譜、核磁共振氫譜 生成的氣體 將生成的氣體先通過盛有水的試管,再通入盛有KMnO4溶液的試管,KMnO4溶液褪色(或直接通入溴的四氯化碳溶液)
【解析】
溴乙烷與氫氧化鈉反應生成乙醇與溴化鈉,反應方程式為CH3CH2Br+NaOH![]() CH3CH2OH+NaBr。
CH3CH2OH+NaBr。
(1)溴乙烷沸點低,溴乙烷易揮發,用水浴加熱熱均勻,減少溴乙烷的損失,故答案為溴乙烷沸點低,減少溴乙烷的損失;
(2)溴乙烷不溶于水,開始溶液分層,生成的產物乙醇、溴化鈉都易溶于水,當溶液分層消失,表明溴乙烷與NaOH溶液已完全反應,故答案為試管內溶液靜置后不分層;
(3)乙醇分子結構中有三種氫原子,它們的比為3:2:1,利用紅外光譜、核磁共振氫譜可檢測,故答案為紅外光譜、核磁共振氫譜;
(4)無論發生取代反應還是消去反應,溶液中都會產生Br-,但生成的有機物不同,溴乙烷發生消去反應生成乙烯,所以應檢驗生成的有機物乙烯;檢驗乙烯可根據其能使酸性KMnO4溶液或溴水褪色的原理來進行,可以采用洗氣的裝置,觀察到酸性KMnO4溶液褪色且有氣泡產生,溴水或溴的四氯化碳溶液褪色即可,
故答案為生成氣體;將生成的氣體先通過盛有水的試管,再通入盛有KMnO4溶液的試管,KMnO4溶液褪色(或直接通入溴的四氯化碳溶液,溴水褪色)。


科目:高中化學 來源: 題型:
【題目】鉬是一種過渡金屬元素,通常用作合金及不銹鋼的添加劑,這種元素可增強合金的強度、硬度、可焊接性及韌性,還可增強其耐高溫及耐腐蝕性能。如圖是化工生產中制備金屬鉬的主要流程圖。
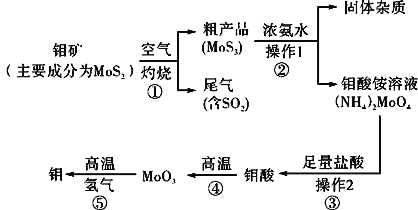
(1)反應①的尾氣可以再利用,寫出應用該尾氣制得的兩種重要化學試劑:___。
(2)如果在實驗室模擬操作1和操作2,則需要使用的主要玻璃儀器有:___。
(3)鉬在空氣中灼燒生成三氧化鉬,三氧化鉬溶于氫氧化鈉溶液生成鉬酸鈉;三氧化鉬不溶于鹽酸或稀硫酸。鉬酸鈉的化學式為___。
(4)工業上制備還原性氣體CO和H2的反應原理為CO2+CH4![]() 2CO+2H2,CH4+H2O
2CO+2H2,CH4+H2O![]() CO+3H2。含甲烷體積分數為80%的a L(標準狀況)天然氣與足量二氧化碳和水蒸氣的混合物在高溫下反應,甲烷轉化率為90%,用產生的還原性氣體(CO和H2)還原MoO3制鉬,理論上能生產鉬的質量為___。
CO+3H2。含甲烷體積分數為80%的a L(標準狀況)天然氣與足量二氧化碳和水蒸氣的混合物在高溫下反應,甲烷轉化率為90%,用產生的還原性氣體(CO和H2)還原MoO3制鉬,理論上能生產鉬的質量為___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗小組制備高鐵酸鉀(K2FeO4) 并探究其性質。資料: K2FeO4 為紫色固體,微溶于KOH溶液;具有強氧化性,在酸性或中性溶液中快速產生O2,在堿性溶液中較穩定。制備K2FeO4 (夾持裝置略)
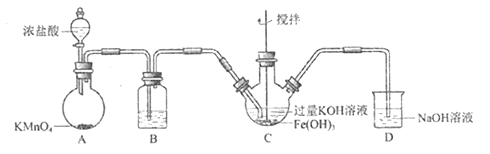
(1)簡述檢驗該裝置氣密性的方法:________________________________________。
(2)A為氯氣發生裝置。A中化學反應的被還原的元素是____________________________。
(3)裝置B的作用是除雜,所用試劑為_____________________________________。
(4)C中得到紫色固體和溶液。請寫出C中發生的化學反應并標出電子轉移的方向和數目:_________。 此反應表明:氧化性Cl2______FeO42-(填“>”或“<”)。
(5) C中除了發生③中的反應,還發生化學反應的離子方程式是:______________________。
(6)用KOH溶液充分洗滌C中所得固體,再用KOH溶液將K2FeO4溶出,得到紫色溶液a。取少量a,滴加鹽酸,有Cl2產生。此實驗得出Cl2和FeO42-的氧化性強弱關系與制備實驗時得出的結論相反,原因是__________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有下列幾組物質,請將序號填入下列空格內:
A、CH2=CH﹣COOH和油酸(C17H33COOH)
B、12C60和石墨
C、![]() 和
和![]()
D、35Cl和37Cl
E、乙醇和乙二醇
(1)互為同位素的是 ;
(2)互為同系物的是 ;
(3)互為同素異形體的是 ;
(4)互為同分異構體的是 ;
(5)既不是同系物,又不是同分異體,也不是同素異形體,但可看成是同一類物質的是 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溶液中可能含有H+、NH![]() 、Mg2+、Al3+、Fe3+、CO
、Mg2+、Al3+、Fe3+、CO![]() 、SO
、SO![]() 、NO
、NO![]() 中的幾種。①若加入鋅粒,產生無色無味的氣體;②若加入NaOH溶液,產生白色沉淀,且產生的沉淀量與加入NaOH的物質的量之間的關系如圖所示。則下列說法不正確的是( )
中的幾種。①若加入鋅粒,產生無色無味的氣體;②若加入NaOH溶液,產生白色沉淀,且產生的沉淀量與加入NaOH的物質的量之間的關系如圖所示。則下列說法不正確的是( )
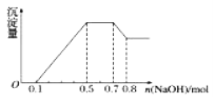
A.溶液中一定含有NH![]() B.溶液中一定含有Al3+
B.溶液中一定含有Al3+
C.溶液中一定含有NO![]() D.溶液中一定含有SO
D.溶液中一定含有SO![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】乙醇是制取飲料、香精、染料、涂料、洗滌劑等產品的原料。
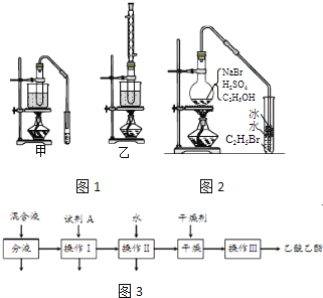
完成下列填空:
(1)實驗室用乙醇制取乙烯時,濃硫酸的用量遠遠超過作為催化劑的正常用量,原因是______。
(2)驗證乙烯加成反應性質時,需對乙烯氣體中的干擾物質進行處理,可選用的試劑是_____(填寫化學式);能確定乙烯通入溴水中發生了加成反應的事實是______。(選填編號)
a.溴水褪色 b.有油狀物質生成
c.反應后水溶液酸性增強 d.反應后水溶液接近中性
(3)實驗室用乙醇和乙酸制備乙酸乙酯時,甲、乙兩套裝置如圖1都可以選用。關于這兩套裝置的說法正確的是______。(選填編號)

a.甲裝置乙酸轉化率高 b.乙裝置乙酸轉化率高
c.甲裝置有冷凝回流措施 d.乙裝置有冷凝回流措施
(4)用乙裝置實驗時,提純乙中乙酸乙酯的流程如圖3以上流程中試劑A的化學式是______;操作Ⅱ的名稱是______;操作Ⅲ一般適用于分離______混合物。
(5)如圖2是用乙醇制備溴乙烷的裝置,實驗中有兩種加料方案:
①先加溴化鈉→再加乙醇→最后加1:1濃硫酸;
②先加溴化鈉→再加1:1濃硫酸→最后加乙醇。
按方案①和②實驗時,產物都有明顯顏色,若在試管中加入______,產物可變為無色。與方案①相比較,方案②的明顯缺點是______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、Z、W均為短周期元素,它們在元素周期表中相對位置如圖所示,若Z原子的最外層電子數是第一層電子數的3倍,下列說法正確的是( )
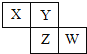
A.Z單質與氫氣反應較Y劇烈
B.X與W的原子核外電子數相差9
C.X單質氧化性強于Y單質
D.最高價氧化物對應水化物酸性W比Z強
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將a g二氧化錳粉末加入b mol/L的濃鹽酸c L中加熱完全溶解,反應中轉移電子d個,設NA為阿伏加德羅常數的值,下列敘述正確的是
A.可以收集到氯氣![]() L
L
B.NA可表示為:![]()
C.反應后溶液中的Cl―數目為:![]()
D.反應后溶液中的H+數目為:![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以CH4和H2O為原料,通過下列反應來制備甲醇。
I:CH4(g) + H2O(g) ![]() CO(g) + 3H2(g) △H=+206.0kJ·mol-1
CO(g) + 3H2(g) △H=+206.0kJ·mol-1
II:CO(g) + 2H2(g) ![]() CH3OH(g) △H=-129.0kJ·mol-1
CH3OH(g) △H=-129.0kJ·mol-1
(1)一定溫度下,在容積2L且固定的兩個密閉容器中,按如下方式加入反應物發生反應I,一段時間后達到平衡。
容 器 | 甲 | 乙 |
反應物投入量 | 1molCH4、1molH2O | a molCH4、a molH2O、b molCO、c molH2 |
經測定甲容器經過5min達到平衡,平衡后甲中氣體的壓強為開始的1.2倍,若要使平衡后乙與甲中相同組分的體積分數相等,且起始時維持化學反應向逆反應方向進行,則b的取值范圍為__________。
(2)將1.0molCH4和2.0molH2O(g)通入容積為10L的反應室,在一定條件下發生反應I,測得在一定的壓強下CH4的轉化率與溫度的關系如圖。
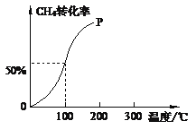
①假設100 ℃時達到平衡所需的時間為5min,則用H2表示該反應的反應速率為______。
②100℃時反應I的平衡常數為____________。
(3)若在恒溫恒壓容器內進行反應II,下列能說明該反應達到平衡狀態的有________(填序號)。
A.有2個H—H鍵生成的同時有 3個C—H鍵斷裂
B.CO百分含量保持不變
C.容器中混合氣體的壓強保持不變
D.容器中混合氣體的密度保持不變
(4)在壓強為0.1MPa、溫度為300℃條件下,將amol CO與3amol H2的混合氣體在催化劑作用下發生反應II生成甲醇,平衡后將容器的容積壓縮到原來的l/2,其他條件不變,對平衡體系產生的影響是__________(填序號)。
A.c(H2) 減少 B.正反應速率加快,逆反應速率減慢
C.n(CH3OH) 增加 D.![]() 減小 E.平衡常數K增大
減小 E.平衡常數K增大
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com