

分析 如先加入AgNO3,則會同時生成Ag2SO4和AgCl沉淀,則應先加入過量的BaCl2[或Ba(NO3)2],生成BaSO4沉淀,然后在濾液中加入過量的AgNO3,使Cl-全部轉化為AgCl沉淀,在所得濾液中加入過量的Na2CO3,使溶液中的Ag+、Ba2+完全沉淀,最后所得溶液為NaNO3和Na2CO3的混合物,加入稀HNO3,最后進行蒸發操作可得固體NaNO3,以此解答該題.
解答 解:(1)如先加入AgNO3,則會同時生成Ag2SO4和AgCl沉淀,則應先加入過量的BaCl2[或Ba(NO3)2],生成BaSO4沉淀,然后在濾液中加入過量的AgNO3,使Cl-全部轉化為AgCl沉淀,則試劑X為BaCl2[或Ba(NO3)2],沉淀A為BaSO4,沉淀B為AgCl,
故答案為:Ba(NO3)2;
(2)加入過量的BaCl2[或Ba(NO3)2],然后在濾液中加入過量的AgNO3,使Cl-全部轉化為AgCl沉淀,在所得濾液中含有Ag+、Ba2+,步驟③在所得濾液中加入過量的Na2CO3,使溶液中的Ag+、Ba2+完全沉淀,反應的離子方程式為Ba2++CO32-═BaCO3↓、2Ag++CO32-═Ag2CO3↓,
故答案為:Ba2++CO32-═BaCO3↓;2Ag++CO32-═Ag2CO3↓;
(3)溶液3為NaNO3和Na2CO3的混合物,加入稀HNO3,可除去Na2CO3,最后加熱蒸發、冷卻結晶、過濾得到硝酸鈉,
故答案為:HNO3;蒸發結晶.
點評 本題考查物質的分離提純操作,題目難度中等,本題注意Cl-、SO42-的性質,把握除雜原則,提純時不能引入新的雜質,注意把握實驗的先后順序.


 津橋教育計算小狀元系列答案
津橋教育計算小狀元系列答案科目:高中化學 來源: 題型:填空題
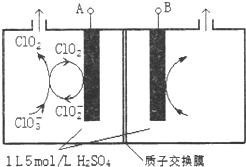 二氧化氯(ClO2)是國內外公認的高效、廣譜、快速、安全無毒的殺菌消毒劑,被稱為“第4代消毒劑”.工業上可采用氯酸鈉(NaClO3)或亞氯酸鈉(NaClO2)為原料制備ClO2.
二氧化氯(ClO2)是國內外公認的高效、廣譜、快速、安全無毒的殺菌消毒劑,被稱為“第4代消毒劑”.工業上可采用氯酸鈉(NaClO3)或亞氯酸鈉(NaClO2)為原料制備ClO2.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 已知某可逆反應:mA(氣)+nB(氣)?xC(氣)△H=QkJ•mol-1,在密閉容器中進行,如圖表示反應在不同時間t,溫度T和壓強P與C在混合氣體中的百分含量(C%)的關系曲線,則( )
已知某可逆反應:mA(氣)+nB(氣)?xC(氣)△H=QkJ•mol-1,在密閉容器中進行,如圖表示反應在不同時間t,溫度T和壓強P與C在混合氣體中的百分含量(C%)的關系曲線,則( )| A. | T1>T2,P1>P2,m+n>x,Q>0 | B. | T1>T2,P1<P2,m+n<x,Q<0 | ||
| C. | T1>T2,P1<P2,m+n<x,Q>0 | D. | T1<T2,P1>P2,m+n>x,Q<0 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | HCl的電子式: | B. | 氯離子(Cl-)的結構示意圖: | ||
| C. | 乙酸的結構簡式:C2H4O2 | D. | 質子數為17、中子數為20的氯原子: |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,Cl2的摩爾質量為71g | |
| B. | 氧化還原反應一定有氧元素參加 | |
| C. | 國際上規定,0.012kg 12C所含有的碳原子數約為1mol | |
| D. | Na2CO3屬于鈉鹽,又屬于碳酸鹽是用交叉分類法分類的 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 綠色食品是指不含任何化學物質的食品 | |
| B. | 苯主要是從石油分餾而獲得的一種重要化工原料 | |
| C. | 煤經氣化和液化兩個化學變化過程可以轉變為清潔能源 | |
| D. | 乙烯和苯均能發生氧化反應,說明兩者都有碳碳雙鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com