
2015年斯坦福大學研究人員研制出一種可在一分鐘內完成充放電的超常性能鋁離子電池,內部用AlCl4-和有機陽離子構成電解質溶液,其放電工作原理如圖所示。下列說法不正確的是
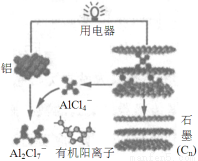
A.放電時,鋁為負極、石墨為正極
B.放電時,有機陽離子向鋁電極方向移動
C.放電時的負極反應為:Al –3e-+ 7AlCl4-= 4Al2Cl7-
D.充電時,AlCl4-向石墨電極方向移動
 暑假銜接教材期末暑假預習武漢出版社系列答案
暑假銜接教材期末暑假預習武漢出版社系列答案 假期作業暑假成長樂園新疆青少年出版社系列答案
假期作業暑假成長樂園新疆青少年出版社系列答案科目:高中化學 來源:2017屆福建省高三上聯考二化學卷(解析版) 題型:選擇題
環保、安全的鋁--空氣電池的工作原理如圖所示,下列有關敘述錯誤的是
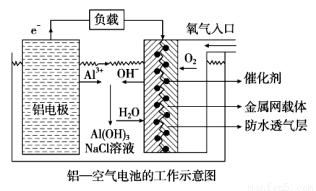
A.電池工作過程中,電解質溶液的pH不斷增大
B.正極的電極反應式為O2 + 4e-+ 2H2O =4OH-
C.NaCl的作用是增強溶液的導電性
D.用該電池做電 源電解KI溶液制取1 mol KIO3,消耗鋁電極的質量為54 g
源電解KI溶液制取1 mol KIO3,消耗鋁電極的質量為54 g
查看答案和解析>>
科目:高中化學 來源:2017屆廣東省肇慶市高三上學期二模化學試卷(解析版) 題型:選擇題
某有機化合物的結構簡式如圖所示,下列說法正確的是( )
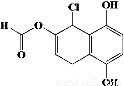
A.不能發生銀鏡發應
B.1mol 該物質最多可與2molBr2反應
C.1mol 該物質最多可與4mol NaOH反應
D.與NaHCO3、Na2CO3均能發生反應
查看答案和解析>>
科目:高中化學 來源:2017屆廣東省深圳市三校高三上學期第一次聯考化學卷(解析版) 題型:選擇題
已知A是一種金屬單質,B顯淡黃色,其轉化關系如圖所示,則C的以下性質錯誤的是 ( )
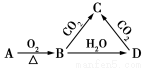
A.溶液呈堿性
B.與澄清石灰水反應產生白色沉淀
C.與足量鹽酸反應放出氣 體
體
D.受熱易分解
查看答案和解析>>
科目:高中化學 來源:2017屆廣東省韶關市高三上高考調研理綜化學試卷(解析版) 題型:推斷題
【化學—選修3:物質結構與性質】
硒(Se)是一種有抗癌、抗氧化作用的元素,可以形成多種化合物。
(1)基態硒原子的價層電子排布式為 。
(2)鍺、砷、硒的第一電離能大小排序為 。H2SeO4的酸性比H2SeO3的強,其原因是 。
(3)H2SeO3的中心原子雜化類型是 ;SeO32- 的立體構型是 。與SeO32- 互為等電體的分子有(寫一種物質的化學式即可) 。
(4)H2Se屬于 (填“極性”或“非極性”)分子;單質硒的熔點為217℃,它屬于 晶體。
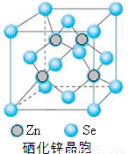
(5)硒化鋅(SnSe)是一種重要的半導體材料,其晶胞結構如圖所示,該晶胞中硒原子的配位數為 ;若該晶胞密度為ρg•cm-3,硒化鋅的摩爾質量為M g/mol。NA代表阿伏加德羅常數,則晶胞參數a為 pm。
查看答案和解析>>
科目:高中化學 來源:2017屆廣東省韶關市高三上高考調研理綜化學試卷(解析版) 題型:選擇題
化學與社會、科學、技術、環境等有密切聯系。下列有關說法正確的是
A.用浸泡過酸性高錳酸鉀溶液的硅藻土吸收水果產生的乙烯以達到保鮮目的
B.PM 2.5是指氮、硫的氧化物溶于水形成的酸性液體造成的空氣污染
C.新型材料聚酯纖維、光導纖維都屬于有機高分子
D.在食品袋中放入盛有硅膠的透氣袋,可防止食物氧化變質
查看答案和解析>>
科目:高中化學 來源:2017屆廣東省汕頭市高三上學期期末化學試卷(解析版) 題型:選擇題
下列關于電解質溶液的敘述正確的是
A.常溫下,pH=7的NH4Cl與氨水的混合溶液中:c(Cl-)>c(NH4+)>c(H+)=c(OH-)
B.在pH=3的溶液中,Na+、Cl-、Fe2+、ClO-可大量共存
C.常溫下,pH=11的NaOH溶液與pH=3的醋酸溶液等體積混合,滴入石蕊溶液呈紅色
D.向0.1mol·L-1的氨水中加入少量硫酸銨固體,則溶液中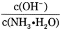 增大
增大
查看答案和解析>>
科目:高中化學 來源:2017屆廣東省清遠市清城區高三上期末B卷化學試卷(解析版) 題型:選擇題
X、Y、Z都是氣體,反應前X、Y的物質的量之比是1:2,在一定條件下可逆反應X+2Y?2Z達到平衡時,測得反應物總的物質的量等于生成物總的物質的量,則平衡時X的轉化率是( )
A.80% B.20% C.40% D.60%
查看答案和解析>>
科目:高中化學 來源:2017屆湖南省株洲市高三上教學質檢一化學試卷(解析版) 題型:填空題
氮的固定對工農業及人類生存具有重大意義。
Ⅰ.合成氨是最重要的人工固氮:N2(g)+3H2(g) 2NH3(g)。
2NH3(g)。
(1)下列關于該反應的說法中,正確的是 。
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S>0 D.△H<0,△S<0
(2) —定溫度下,在容積為1L的密閉容器中,加入ImolN2和3molH2,反應達到平衡時H2的轉化率為60%,則此條件下反應的平衡常數K= (此處不要求寫單位);保持容器體積不變,再向容器中加入lmolN2,3molH2反應達到平衡時,氫氣的轉化率將 (填“增大”、“減小”或“不變”)
(3)標準狀況下,若將22.4mL的氨氣通入100mLpH為2的鹽酸中.則溶液中各離子濃度的順序由大到小為 。
(4)將氨氣通入盛有CaSO4懸濁液的沉淀池中,再通入適量的CO2氣體,充分反應后,過濾所得濾液為(NH4)2SO4溶液,該過程的化學方程式為 。
II.隨著研究的不斷深入,科學家發明了越來越多有關氮的固定方法。
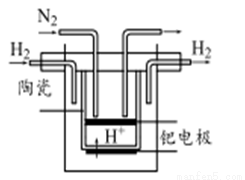
(5)20世紀末,科學家采用高質子導電性的SCY陶瓷(能傳遞H+)為介質,用吸附在它內外表面上的金屬鈀多晶薄膜做電極,實現常壓、570℃高溫的電解法合成氨,提高了反應物的轉化率,其實驗簡圖如下,陰極的電極反應式為 。
(6)近年,又有科學家提出在常溫、常壓、催化劑等條件下合成氨氣的新思路,反應原理為:
2N2(g)+6H2O(I)  4NH3(g)+3O2(g),則其反應熱△H= 。(已知:N2(g)+3H2(g)
4NH3(g)+3O2(g),則其反應熱△H= 。(已知:N2(g)+3H2(g)  2NH3(g) △H=-92.4kJ·mol-1;2H2(g)+O2(g)
2NH3(g) △H=-92.4kJ·mol-1;2H2(g)+O2(g)  2H2O(I) △H=-571.6kJ·mol-1)
2H2O(I) △H=-571.6kJ·mol-1)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com