
分析 (1)依據溶液稀釋過程中所含溶質的物質的量不變計算需要溶液的體積;
(2)依據配制一定物質的量濃度溶液的一般步驟選則需要的儀器;
(3)依據容量瓶構造解答;
(4)依據配制一定物質的量濃度溶液的正確操作步驟結合容量瓶、量筒使用方法解答;
(5)分析操作對溶質的物質的量和溶液體積的影響,依據C=$\frac{n}{V}$進行誤差分析.
解答 解:(1)依據溶液稀釋過程中所含溶質的物質的量不變得V×18.4mol/L=0.4mol/L×250mL,解得V=5.4mL;
故答案為:5.4;
(2)配制一定物質的量濃度溶液的一般步驟:計算、量取、稀釋、冷卻、移液、洗滌、定容、搖勻,用到的儀器:燒杯、玻璃棒、10ml 量筒、250ml 容量瓶;還缺少的儀器:膠頭滴管;
故答案為:①②③⑥;膠頭滴管;
(3)容量瓶上需標有:溫度、容積、刻度線;
故答案為:B;
(4)①用量筒量取V ml 濃硫酸,故正確;
②量筒為精密儀器,不能用來溶解固體、稀釋濃溶液,故錯誤;
③立即將稀釋后的溶液轉入容量瓶中,冷卻后溶液體積偏小,溶液濃度偏高,故錯誤;
④定容時,小心地往容量瓶中加水至刻度1-2cm處,改用膠頭滴管,故正確;
⑤平視凹液面定容,故正確;
⑥搖勻時把容量瓶瓶塞塞緊,再振蕩,上下顛倒搖勻,故正確;
故選:②③;
(5)①將稀釋后的硫酸轉移至容量瓶中后,未洗滌燒杯和玻璃棒,導致溶質的物質的量偏小,溶液濃度偏低,故選;
②將燒杯內的稀硫酸向容量瓶中轉移時,因操作不當使部分稀硫酸濺出瓶外,導致溶質的物質的量偏小,溶液濃度偏低,故選;
③定容操作不慎使溶液凹液面高于容量瓶刻度線,此時立即將多余的液體吸出,使溶液凹液面與容量瓶刻度線相切,導致溶質的物質的量偏小,溶液濃度偏低,故選;
④定容時仰視容量瓶刻度線,導致溶液的體積偏大,溶液濃度偏低,故選;
故選:①②③④.
點評 本題考查了一定物質的量濃度溶液的配制,明確配制原理及操作步驟是解題關鍵,注意誤差分析的方法和技巧,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| 序號 | 甲 | 乙 |
| ① | SO2 | 石灰水 |
| ② | CO2 | 石灰水 |
| ③ | SO2 | Ba(NO3)2 |
| ④ | NO2 | CaCl2 |
| A. | ②③④ | B. | ②③ | C. | ①③④ | D. | ①②③ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
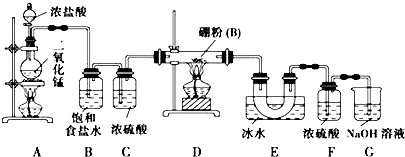
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
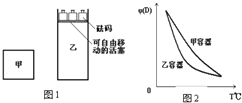 一定溫度下,有可逆反應:2A(g)+2B(g)?C(g)+3D(g);△H<0.現將2molA和2mol B充入體積為V的甲容器,將2 mol C和6 mol D充入乙容器并使乙容器在反應開始前的體積為2V(如圖1).關于兩容器中反應的說法正確的是( )
一定溫度下,有可逆反應:2A(g)+2B(g)?C(g)+3D(g);△H<0.現將2molA和2mol B充入體積為V的甲容器,將2 mol C和6 mol D充入乙容器并使乙容器在反應開始前的體積為2V(如圖1).關于兩容器中反應的說法正確的是( )| A. | 甲容器中的反應先達到化學平衡狀態 | |
| B. | 兩容器中的反應均達平衡時,平衡混合物中各組份的體積百分組成相同,混合氣體的平均相對分子質量也相同 | |
| C. | 兩容器達平衡后升高相同的溫度,兩容器中物質D的體積分數隨溫度變化如圖2所示 | |
| D. | 在甲容器中再充入2 mol A和2 mol B,平衡后甲中物質C的濃度和乙中物質C的濃度相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 聯合制堿法中循環使用CO2和NH3,以提高原料利用率 | |
| B. | 硫酸工業中,SO2氧化為SO3時采用常壓,因為高壓會降低SO2轉化率 | |
| C. | 合成氨生產過程中將NH3液化分離,可加快正反應速率,提高N2、H2的轉化率 | |
| D. | 煉鋼是在高溫下利用氧化劑把生鐵中過多的碳和其他雜質氧化成氣體或爐渣除去 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 磷在氯氣中燃燒產生大量的白煙,并放出熱量 | |
| B. | 純凈的氫氣在氯氣中安靜燃燒,發出黃色火焰 | |
| C. | 光照新制氯水有氣泡逸出,該氣體是Cl2 | |
| D. | 實驗室制備氯氣可用排飽和食鹽水法收集 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
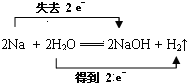 反應中,H2O是氧化劑.
反應中,H2O是氧化劑.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 不慎將酸濺到眼中,應立即用堿液沖洗,邊洗邊眨眼睛 | |
| B. | 酸式滴定管,堿式滴定管、移液管都是準確量取一定體積液體的儀器,它們在使用時都要進行檢查是否漏水、水洗、潤洗、注液、調整液面等幾個過程 | |
| C. | 除去硬脂酸鈉溶液中的甘油方法是:往溶液中加入食鹽,過濾 | |
| D. | 常溫下,準確稱取14.8g Ca(OH)2,配制100mL 2.0 mol/L的Ca(OH)2溶液 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com