
【題目】下列各組中的兩物質相互反應時,若改變反應條件(溫度、反應物用量比),化學反應的產物并不改變的是( )
A.Na和O2B.NaOH和CO2
C.Na2O2和CO2D.Na2CO3和鹽酸
科目:高中化學 來源: 題型:
【題目】假定把12C的相對原子質量定為24,把24g12C含有的原子個數定為阿伏加德羅常數,而物質的量的概念不變。則下列推斷不正確的是
A. 此時16O的相對原子質量為32
B. 40gNaOH溶于水配成1L溶液,其物質的量濃度為1 mol/L
C. 標況下44gCO2的體積為22.4L
D. NA個氧分子與NA個氫分子有相同數目的分子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】關于單質鐵的性質,下列說法中正確的是( )
A.鐵與高溫水蒸氣反應生成Fe2O3B.鐵與硫單質反應生成Fe2S3
C.生鐵是一種鐵-碳合金D.常溫下,冷的濃硫酸與鐵單質不反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】圖1是銅鋅原電池示意圖,圖2中軸表示實驗時流入正極的電子的物質的量, y軸表示

A. 銅棒的質量 B. c(H+) C. c(SO42-) D. c(Zn2+)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關實驗操作、現象、目的及結論都正確的是
選項 | 實驗 | 現象結論 |
A | 向濃度均為 0.1 molL1 NaCl 和 Na2CrO4混合溶液中滴加0.1 molL1 AgNO3 溶液,先生成白色的AgCl沉淀 | 能證明Ksp(AgCl)< Ksp(Ag2CrO4) |
B | 向植物油和礦物油中分別加入燒堿溶液,加熱,冷卻后觀察是否分層 | 不能區別植物油和礦物油 |
C | 其他條件相同,一只試管中加入5mL 0.2mol/LH2C2O4 (aq)和2.5L 0.1mol/L KMnO4(aq);另一支試管中加入7.5ml 0.2moI/L H2C2O4 (aq)和 2.5mL 0.2mol/L KMnO4(aq) 和5mlH2O | 可驗證相同條件下濃度對化學反應速率的影響 |
D | 常溫下,用pH計測定0.1moI/L NaA溶液的pH小于0.1moI/L Na2CO3溶液的pH | 能證明酸性:HA>H2CO3 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用右圖所示裝置進行下列實驗,能得出相應實驗結論的是( )
選項 | ① | ② | ③ | 實驗結論 | 實驗裝置 |
A | 稀硫酸 | Na2S | AgNO3與AgCl的溶液 | Ksp(AgCl)>Ksp(Ag2S) |
|
B | 濃硫酸 | 蔗糖 | 溴水 | 濃硫酸具有脫水性、氧化性 | |
C | 稀鹽酸 | Na2SO3 | Ba(NO3)2 溶液 | SO2與可溶性鋇鹽均可以生成白色沉淀 | |
D | 濃硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述正確的是
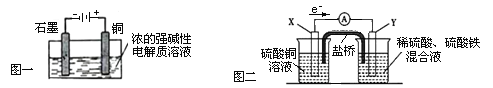
A.Cu2O是一種半導體材料,基于綠色化學理念設計的制取Cu2O的電解池示意圖如圖一所示,石墨電極上產生氫氣,銅電極發生氧化反應
B.圖一所示當有0.1mol電子轉移時,有0.1molCu2O生成
C.圖二裝置中發生:Cu+2Fe3+ = Cu2+ +2Fe2+ ,X極是負極,Y極材料可以是銅
D.如圖二,鹽橋的作用是傳遞電荷以維持電荷平衡,Fe3+ 經過鹽橋進入左側燒杯中
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向100 mL 0.1 mol·L-1硫酸鋁銨[NH4Al(SO4)2]溶液中逐滴滴入0.1 mol·L-1Ba(OH)2溶液。隨著Ba(OH)2溶液體積V的變化,沉淀總物質的量n的變化如圖所示。則下列說法中正確的是

A. a點的溶液呈中性
B. 從開始到b點發生反應的總的離子方程式是:Al3++2SO42-+2Ba2++3OH-= Al(OH)3↓+2BaSO4↓
C. c點加入Ba(OH)2溶液的體積為200 mL
D. c點溶液呈堿性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】與Al反應放出大量氫氣的溶液中,下列離子可能大量共存的是
A.Mg2+、Na+、Cl-、NO3-B.K+、Na+、Cl-、HCO3-
C.Na+、NH4+、Cl-、CH3COO-D.Fe2+、Ba2+、Cl-、I-
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com