
| A. | 在水中溶解性:Na2CO3>NaHCO3 | |
| B. | 熱穩定性:Na2CO3<NaHCO3 | |
| C. | 與酸反應的速度:Na2CO3>NaHCO3 | |
| D. | Na2CO3不能轉化成NaHCO3,而NaHCO3能轉化為Na2CO3 |
分析 A.相同條件下,碳酸鈉的溶解度大;
B.碳酸氫鈉受熱易分解;
C.碳酸氫鈉與鹽酸反應一步完成,而碳酸鈉與鹽酸反應兩步進行;
D.碳酸鈉溶液通入二氧化碳生成碳酸氫鈉,碳酸氫鈉加熱或與氫氧化鈉反應生成碳酸鈉.
解答 解:A.常溫下,向飽和碳酸鈉溶液中通入二氧化碳氣體,有碳酸氫鈉晶體析出,可知常溫時水溶解性:Na2CO3>NaHCO3,故A正確;
B.NaHCO3不穩定,加熱易分解:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,對熱穩定性:Na2CO3>NaHCO3,故B錯誤;
C.分別滴加HCl溶液,反應離子方程式為CO32-+2H+═CO2↑+H2O,HCO3-+H+═H2O+CO2↑,相同條件下NaHCO3比Na2CO3反應放出氣體劇烈,故C錯誤;
D.碳酸鈉和二氧化碳反應生成碳酸氫鈉,碳酸氫鈉也可以加熱分解生成碳酸鈉,反應的條件不同,不是可逆反應,故D錯誤;
故選A.
點評 本題考查Na2CO3和NaHCO3性質的異同,為高頻考點,題目難度不大,注意把握Na2CO3和NaHCO3性質,注重基礎知識的積累.


 課堂全解字詞句段篇章系列答案
課堂全解字詞句段篇章系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 不含其他雜質的天然油脂屬于純凈物 | |
| B. | 油脂在酸性條件下水解稱為皂化 | |
| C. | 油脂的烴基部分飽和程度越大,熔點越低 | |
| D. | 各種油脂水解后的產物中都有甘油 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 二氧化硅是酸性氧化物,它可以跟堿反應,不能和任何酸反應 | |
| B. | 水玻璃中通入過量的二氧化碳的離子方程式為:SiO32-+CO2+H2O═H2SiO3↓+CO32- | |
| C. | 石英可以用來生產玻璃 | |
| D. | 晶體硅常被用來制造光導纖維 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 編號 | 物質 | 雜質(少量) | 試 劑 | 除雜操作方法 |
| (1) | Na2CO3固體 | NaHCO3 | - | |
| (2) | Fe | Al | ||
| (3) | FeSO4 | CuSO4 | ||
| (4) | NaOH | Na2CO3 | ||
| (5) | KNO3 | NaCl | - |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
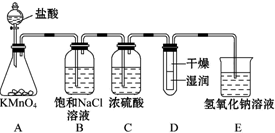
 肼是重要的化工原料,某探究小組利用下列反應制取水合肼(N2H4•H2O):
肼是重要的化工原料,某探究小組利用下列反應制取水合肼(N2H4•H2O):查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙烯可以與酸性高錳酸鉀溶液反應 因此可以用酸性高錳酸鉀溶液除去乙烷中的乙稀 | |
| B. | 溴乙烷可以通過乙稀與溴化氫加成得到 也可以通過乙烷與溴發生取代反應制備 | |
| C. | 區分甲苯和苯可以用酸性高錳酸鉀溶液也可以用溴水 | |
| D. | 鑒別己烯是否混有少量甲苯 正確的實驗方法是可以加足量溴水 然后再加入酸性高錳酸鉀溶液 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com