
A
 新課標同步訓練系列答案
新課標同步訓練系列答案 一線名師口算應用題天天練一本全系列答案
一線名師口算應用題天天練一本全系列答案科目:高中化學 來源: 題型:閱讀理解
| 乙炔水化法 | 乙烯氧化法 | |
| 原料 | 乙炔、水 | 乙烯、空氣 |
| 反應條件 | HgSO4、100~125℃ | PdCl2-CuCl2、100~125℃ |
| 平衡轉化率 | 乙炔平衡轉化率90%左右 | 乙烯平衡轉化率80%左右 |
| 日產量 | 2.5噸(某設備條件下) | 3.6噸(相同設備條件下) |
| 原料生產工藝過程 | ||||||||
| 乙炔 | CaCO3
| |||||||
| 乙烯 | 來源于石油裂解氣 |
查看答案和解析>>
科目:高中化學 來源: 題型:
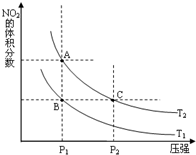 氮可形成多種氧化物,如NO、NO2、N2O4等,NO2和N2O4可以相互轉化.
氮可形成多種氧化物,如NO、NO2、N2O4等,NO2和N2O4可以相互轉化.| 時間(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
查看答案和解析>>
科目:高中化學 來源:2012-2013學年浙江省寧波市十校聯考理綜化學試卷(解析版) 題型:選擇題
Ⅰ.800℃時,向容積為2L的恒容密閉容器中充入一定量的CO和H2O維持恒溫,發生反應CO(g)+H2O(g) H2(g)+CO2(g),反應過程中測定的部分數據見下表:
H2(g)+CO2(g),反應過程中測定的部分數據見下表:
|
反應時間/min |
0 |
2 |
4 |
6 |
|
n(CO)/mol |
1.20 |
0.90 |
|
0.80 |
|
n(H2O)/ mol |
0.60 |
|
0.20 |
|
①反應在2 min內的平均速率為v(H2O)=___________;
②800℃時,化學平衡常數K的值為_______________;
③保持其他條件不變,向平衡體系中再通入0.20 mol H2O,與原平衡相比,達到新平衡時CO轉化率______(填“增大”或“減小”或“不變”)。
④在恒溫恒壓密閉容器中通入CO和H2O各1 mol發生該反應,當反應達到平衡后,維持溫度與壓強不變,t1時再通入各1 mol的CO和H2O的混合氣體,請在右圖中畫出正(v正)、逆(v逆)反應速率在t1后隨時間t變化的曲線圖。

Ⅱ.實驗室中利用復分解反應制取Mg(OH)2。實驗數據和現象如下表所示(溶液體積均取用1mL):
|
組別 |
藥品1 |
藥品2 |
實驗現象 |
|
I |
0.01 mol/L NaOH溶液 |
0.01 mol/L MgCl2溶液 |
生成白色沉淀 |
|
II |
0.01 mol/L氨水 |
0.01 mol/L MgCl2溶液 |
無現象 |
|
III |
0.1 mol/L氨水 |
0.1 mol/L MgCl2溶液 |
現象III |
|
IV |
0.1 mol/L氨水 |
0.01 mol/L MgCl2溶液 |
生成白色沉淀 |
|
V |
0.01 mol/L氨水 |
0.1 mol/L MgCl2溶液 |
無現象 |
①現象III是 ;
②如果向0.028 mol/L的MgCl2溶液中加入等體積的NaOH溶液,請計算NaOH溶液的濃度至少達到
mol/L時,溶液中開始出現白色沉淀(Ksp(Mg(OH)2)= 5.6×10-12)。
③MgCl2溶液和氨水混合后存在下列化學平衡:Mg2+(aq)
+ 2NH3·H2O(aq) 2NH4+(aq)
+ Mg(OH)2(s)該反應化學平衡常數的表達式為K=
,列出該反應平衡常數K與Kb(NH3·H2O)、Ksp(Mg(OH)2)的關系式
。
2NH4+(aq)
+ Mg(OH)2(s)該反應化學平衡常數的表達式為K=
,列出該反應平衡常數K與Kb(NH3·H2O)、Ksp(Mg(OH)2)的關系式
。
查看答案和解析>>
科目:高中化學 來源: 題型:
A.2a L B.2.5a L C.3a L D.3.5a L
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com