
| A、①② | B、③④⑤ |
| C、③⑤ | D、①③④ |


科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:

A、 、HCHO和 、HCHO和 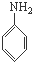 |
B、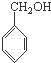 、CH3OH和 、CH3OH和 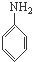 |
C、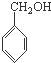 、HCHO和 、HCHO和 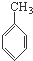 |
D、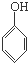 、CH3CHO和 、CH3CHO和 |
查看答案和解析>>
科目:高中化學 來源: 題型:
 硫鐵礦又稱黃鐵礦,是生產硫酸的原料,其主要成分為FeS2.850℃~950℃時,硫鐵礦在空氣中煅燒,可能發生下列反應(設空氣中N2與O2體積比為4:1):
硫鐵礦又稱黃鐵礦,是生產硫酸的原料,其主要成分為FeS2.850℃~950℃時,硫鐵礦在空氣中煅燒,可能發生下列反應(設空氣中N2與O2體積比為4:1):查看答案和解析>>
科目:高中化學 來源: 題型:
| Cl2的體積(標準狀況) | 5.6L | 11.2L | 22.4L |
| n (Cl-) | 2.5mol | 3.0mol | 4.0mol |
| n (Br-) | 3.0mol | 2.6mol | 1.6mol |
| n (I-) | x mol | 0 | 0 |
查看答案和解析>>
科目:高中化學 來源: 題型:
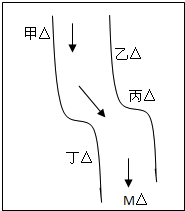 在一條魚、蝦絕跡的小河邊有四座工廠:甲、乙、丙、丁(如圖所示),它們排出的廢液里,每個工廠只含有Na2CO3、FeCl3、Ca(OH)2、HCl中的一種.某中學環保小組對河水檢測時發現:①甲處河水呈乳白色,②乙處河水呈紅褐色,③丙處河水由渾變清,④丁處產生氣泡,河水仍清,⑤M處水樣的pH小于7.請判斷:
在一條魚、蝦絕跡的小河邊有四座工廠:甲、乙、丙、丁(如圖所示),它們排出的廢液里,每個工廠只含有Na2CO3、FeCl3、Ca(OH)2、HCl中的一種.某中學環保小組對河水檢測時發現:①甲處河水呈乳白色,②乙處河水呈紅褐色,③丙處河水由渾變清,④丁處產生氣泡,河水仍清,⑤M處水樣的pH小于7.請判斷:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com