


 ,
,
| ||
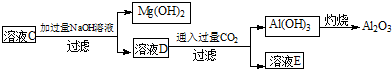
 ;Mg2++2OH-=Mg(OH)2↓,Al3++4OH-=AlO2-+2H2O,AlO2-+CO2+H2O=Al(OH)3↓+HCO3-,2Al(OH)3
;Mg2++2OH-=Mg(OH)2↓,Al3++4OH-=AlO2-+2H2O,AlO2-+CO2+H2O=Al(OH)3↓+HCO3-,2Al(OH)3
| ||
| 0.112g |
| 2.000g |


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
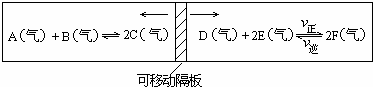
查看答案和解析>>
科目:高中化學 來源: 題型:
| 3 |
| 4 |
查看答案和解析>>
科目:高中化學 來源: 題型:
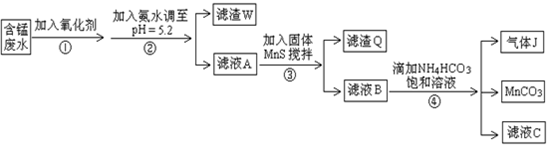
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Cu(OH)2 | Mn(OH)2 | CuS | MnS | MnCO3 |
| 沉淀完全時的PH | 3.7 | 5.2 | 6.4 | 9.8 | ≥0 | ≥7 | ≥7 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
A、 檢查裝置氣密性 |
B、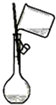 向容量瓶中轉移液體 |
C、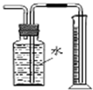 測量Cu與濃硝酸產生氣體體積 |
D、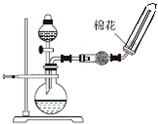 實驗室制取并收集NH3 |
查看答案和解析>>
科目:高中化學 來源: 題型:
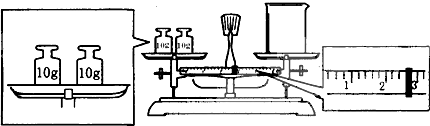
查看答案和解析>>
科目:高中化學 來源: 題型:
| 1 |
| 2 |
| 1 |
| 2 |
| A、5% | B、17% |
| C、25% | D、33% |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、金屬鈉著火燃燒時,用泡沫滅火器滅火 |
| B、硫酸亞鐵溶液存放在加有少量鐵粉的試劑瓶中 |
| C、在新制氯水中滴加少量紫色石蕊試液,充分振蕩后溶液最終呈紅色 |
| D、向Ba(OH)2溶液中慢慢滴加稀硫酸至過量,溶液的導電性變化是弱→強→弱 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com