
分析 根據n=$\frac{m}{M}$計算出10.6g Na2CO3的物質的量,然后可得出含有鈉原子、碳原子、氧原子的物質的量;碳酸鈉含有的電子數=質子數=52,根據N=nNA計算出含有的碳原子、氧原子、電子和質子數.
解答 解:10.6g Na2CO3的物質的量為:n(Na2CO3)=$\frac{10.6g}{106g/mol}$=0.1mol,0.1mol Na2CO3中含有鈉原子的物質的量為:n(Na)=0.1mol×2=0.2mol;含有碳原子的物質的量為:n(C)=n(Na2CO3)=0.1mol,數目為0.1NA;含有O原子的物質的量為:n(O)=0.1mol×3=0.3mol,數目為0.3NA;含有的電子、質子的物質的量相等,都為0.1mol×52=5.2mol,數目為5.2NA,
故答案為:0.2;0.1NA;0.3NA;5.2;5.2NA.
點評 本題考查了物質的量的計算,題目難度不大,明確物質的量與阿伏伽德羅常數、摩爾質量之間的關系即可解答,試題培養了學生的化學計算能力.


科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 化學鍵的斷裂和形成是化學反應中能量變化的主要原因 | |
| B. | 放熱反應和吸熱反應決定于反應物的總能量與生成物的總能量的相對大小 | |
| C. | 已知:S(s)+O2(g)=SO2(g)△H1;S(g)+O2(g)=SO2(g)△H2;則△H1>△H2 | |
| D. | 凡經加熱而發生的化學反應都是吸熱反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 硫酸溶液與氫氧化鋇溶液混合:Ba2++SO42-=BaSO⒋↓ | |
| B. | 稀硫酸中加入銅片:Cu+2H+=Cu2++H2↑ | |
| C. | 氧化銅溶于鹽酸:O2-+2H+=H2O | |
| D. | 二氧化碳通入足量澄清石灰水:Ca2++2OHˉ+CO2=CaCO3↓+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.1 mol/L稀硫酸中含有硫酸根數目為0.1NA | |
| B. | 9g H2O中含有H數目為1mol | |
| C. | 2.4g金屬鎂與足量的鹽酸反應,生成氫分子數目為2NA | |
| D. | 1mol NH4+中含有電子數為10NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
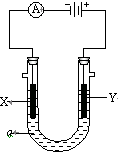 電解原理在化學工業中有廣泛應用.如圖表示一個電解池,裝有電解液a;X、Y是兩塊電極板,通過導線與直流電源相連.請回答以下問題:
電解原理在化學工業中有廣泛應用.如圖表示一個電解池,裝有電解液a;X、Y是兩塊電極板,通過導線與直流電源相連.請回答以下問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com