
| A.常溫下,將pH=3的醋酸溶液稀釋到原體積的10倍后,溶液的pH小于4 |
| B.為確定某酸H2A是強酸還是弱酸,可測NaHA溶液的pH.若pH>7,則H2A是弱酸;若pH<7,則H2A是強酸 |
| C.用0.200mol?L-1NaOH標準溶液滴定HCl與CH3COOH的混合液(混合液中兩種酸的濃度均約為0.1mol?L-1),至中性時,溶液中的酸未被完全中和 |
| D.相同溫度下,將足量氯化銀固體分別放入相同體積的①蒸餾水、②0.1mol?L-1鹽酸、③0.1mol?L-1氯化鎂溶液、④0.1mol?L-1硝酸銀溶液中,Ag+濃度:④>①>②>③ |
| 1 |
| 10 |


 期末寶典單元檢測分類復習卷系列答案
期末寶典單元檢測分類復習卷系列答案科目:高中化學 來源:不詳 題型:單選題
| A.降低溫度,溶液中c(NH4+)增大 | ||
| B.加入少量NaOH固體,平衡向逆反應方向移動,電離平衡常數減小 | ||
| C.加入少量0.1mol?L-1 HCl溶液,溶液中c(OH-)增大 | ||
D.加入水時,溶液中
|
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.①②③④ | B.②③④ | C.③④ | D.③④⑤ |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:問答題
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.溶于水的強電解質,在水溶液中全部電離成離子 |
| B.強電解質的水溶液導電能力一定比弱電解質水溶液的導電能力強 |
| C.某物質若不是電解質,就一定是非電解質 |
| D.難溶于水的電解質一定是弱電解質 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
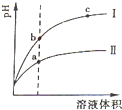
查看答案和解析>>
科目:高中化學 來源:不詳 題型:問答題
查看答案和解析>>
科目:高中化學 來源:不詳 題型:問答題
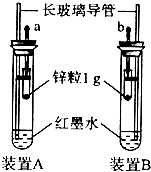
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com