
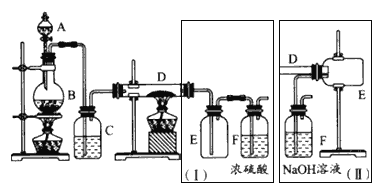
【題目】實驗室可用氯氣與金屬鐵反應制備無水三氯化鐵,該化合物呈棕紅色、易潮解,100℃左右時升華。下圖是兩個學生設計的實驗裝置,左邊的反應裝置相同,而右邊的產品收集裝置則不相同,分別如(I)和(Ⅱ)所示,
試回答:
(1)B中反應的化學方程式為___________________________。
(2)D中的反應開始前,需排除裝置中的空氣,應采取的方法是______________。
(3)D中反應的化學方程式為______________________________。
(4)裝置(I)的主要缺點是_______________________。
(5)裝置(Ⅱ)的主要缺點是______________________________,如果選用此裝置來完成實驗,則必須采取的改進措施是:___________________________。
【答案】4HCl(濃)+MnO2![]() MnCl2+2H2O+Cl2↑ B中的反應進行一段時間后,看到黃綠色氣體充滿裝置,再開始加熱D 2Fe +3Cl2
MnCl2+2H2O+Cl2↑ B中的反應進行一段時間后,看到黃綠色氣體充滿裝置,再開始加熱D 2Fe +3Cl2![]() 2FeCl3 導管易被產品堵塞,尾氣排入空氣,易造成環境污染 產品易潮解 在瓶E和F之間連接裝有干燥劑的裝置
2FeCl3 導管易被產品堵塞,尾氣排入空氣,易造成環境污染 產品易潮解 在瓶E和F之間連接裝有干燥劑的裝置
【解析】
(1)實驗室利用濃鹽酸和二氧化錳混合加熱制氯氣,發生反應的化學方程式為4HCl(濃)+MnO2![]() MnCl2+2H2O+Cl2↑;
MnCl2+2H2O+Cl2↑;
(2)D裝置反應前有空氣,空氣中的氧氣能在加熱條件下與鐵粉反應,需排除裝置中的空氣,當B中的反應進行一段時間后,看到黃綠色氣體充滿裝置,說明已經完全排除空氣,再開始加熱D;
(3)鐵在加熱條件下與氯氣反應生成氯化鐵,發生反應的化學方程式為2Fe +3Cl2![]() 2FeCl3;
2FeCl3;
(4)因FeCl3遇冷易凝華,另外沒有尾氣處理,則裝置(I)的主要缺點是導管易被產品堵塞,尾氣排入空氣,易造成環境污染;
(5)氯化鐵易潮解,而裝置(Ⅱ)中無干燥氯氣的裝置,改進措施是在瓶E和F之間連接裝有干燥劑的裝置。


 陽光課堂課時作業系列答案
陽光課堂課時作業系列答案科目:高中化學 來源: 題型:
【題目】沼氣(主要成分是甲烷)是一種廉價的能源,把農村中大量存在的農作物秸稈、雜草、人畜糞便等在沼氣池中發酵,便可產生沼氣,沼氣完全燃燒可以用來點燈、做飯。
(1)建立沼氣池可實現如圖能量轉化:___、___(在框內填寫能量的形式)。
![]()
(2)在101kPa時,32gCH4燃燒生成CO2和氣態H2O,放出1604kJ的熱量,寫出甲烷燃燒的熱化學方程式為___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】震驚全國的天津港“8.12”爆炸事故中,因爆炸沖擊導致氰化鈉泄漏而造成環境污染,可以通過噴灑雙氧水或硫代硫酸鈉溶液來處理。
資料:氰化鈉化學式NaCN(N元素-3價),白色結晶顆粒,劇毒,易溶于水
(1)NaCN用雙氧水處理后,產生一種酸式鹽和一種能使濕潤紅色石蕊試紙變藍的氣體,寫出該反應的化學方程式________________。
(2)某化學興趣小組實驗室制備硫代硫酸鈉(Na2S2O3),并檢測用硫代硫酸鈉溶液處理后的氰化鈉廢水能否達標排放。
【實驗一】實驗室通過下圖裝置制備Na2S2O3。
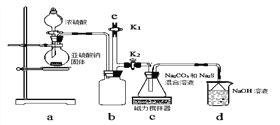
①a裝置中盛濃硫酸的儀器名稱是_______________;
b裝置的作用是________________。
②c裝置中的產物有Na2S2O3和CO2等,d裝置中的溶質有NaOH、Na2CO3,還可能有___________________。
③實驗結束后,在e處最好連接盛_________(選填“NaOH溶液”、“水”、“CCl4”中任一種)的注射器,再關閉K2打開K1,目的是__________________
【實驗二】測定用硫代硫酸鈉溶液處理后的廢水中氰化鈉的含量。
已知:
① 廢水中氰化鈉的最高排放標準為0.50 mg/L。
② Ag++2CN- = [ Ag (CN)2]-, Ag++I- = AgI↓, AgI呈黃色,且CN-優先與Ag+反應。
實驗如下:
取25.00 mL處理后的氰化鈉廢水于錐形瓶中,并滴加幾滴KI溶液作指示劑,用1.000 ×10-4 mol/L的標準AgNO3溶液滴定,消耗AgNO3溶液的體積為2.50 mL。
④滴定終點的判斷方法是____________________
⑤處理后的廢水中氰化鈉的含量為__________mg/L,_______(選填“能”、“不能”)排放
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】濃度相同的NaOH溶液各100mL倒入A、B、C三個燒杯中,分別向三份溶液中通入不等量的CO2,充分反應后,再向三份所得溶液中逐滴加入0.2mol/L的鹽酸,產生CO2的體積與所加鹽酸體積之間關系如圖所示。下列判斷正確的是( )
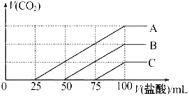
A.原NaOH溶液的濃度為0.2mol/L
B.B燒杯中通入的CO2體積為448mL
C.通入CO2后,不能確定A燒杯中的溶質
D.通入CO2后,C燒杯中溶質成分的物質的量之比為n(NaOH):n(Na2CO3)=2:1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下將NaOH溶液滴加到己二酸![]() 溶液中,混合溶液的pH與離子濃度變化的關系如圖所示。下列敘述錯誤的是
溶液中,混合溶液的pH與離子濃度變化的關系如圖所示。下列敘述錯誤的是![]()
![]()
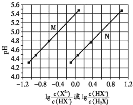
A.![]() 的數量級為
的數量級為![]()
B.曲線N表示pH與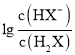 的變化關系
的變化關系
C.NaHX溶液中![]()
D.當混合溶液呈中性時,![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在25℃時,有pH為a的鹽酸和pH為b的NaOH溶液,取VaL該鹽酸,同該NaOH溶液中和,需VbLNaOH溶液,填空:
(1)若a+b=14,則Va:Vb=_________(填數字)。
(2)若a+b=13,則Va:Vb=_________(填數字)。
(3)若a+b>14,則Va:Vb=_________(填表達式),且Va__________Vb(填:>、<、=)(題中a≤6、b≥8)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】pH=2的A、B兩種一元酸溶液各1mL, 分別加水稀釋到1000mL,其溶液的pH與溶液體積(V)的關系如圖所示, 則下列說法正確的是

A. A、B兩種酸溶液物質的量濃度一定相等
B. 稀釋后A酸溶液的酸性比B酸溶液強
C. a = 5時, A是弱酸, B是強酸
D. 若A、B都是弱酸, 則5 > a > 2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】科學家合成出了一種新化合物(如圖所示),其中W、X、Y、Z為同一短周期元素,Z核外最外層電子數是X核外電子數的一半。下列敘述正確的是( )

A.WZ的水溶液呈堿性
B.元素非金屬性的順序為X>Y>Z
C.Y的最高價氧化物的水化物是強酸
D.該新化合物中Y滿足8電子穩定結構
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】含硫各微粒![]() 、
、![]() 和
和![]() 存在于
存在于![]() 與NaOH溶液反應后的溶液中,它們的物質的量分數
與NaOH溶液反應后的溶液中,它們的物質的量分數![]() 與溶液pH的關系如下圖所示.下列說法正確的是
與溶液pH的關系如下圖所示.下列說法正確的是
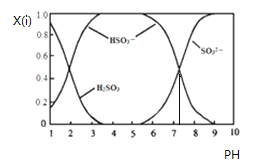
A.![]() 時,溶液中
時,溶液中![]()
B.![]() 時,溶液中
時,溶液中![]()
C.為獲得盡可能純的![]() ,可將溶液的pH控制在
,可將溶液的pH控制在![]() 左右
左右
D.由圖中數據可估算出![]() 為
為![]()
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com