
| A. | X的氣態氫化物的穩定性比甲烷強 | B. | X的最高價氧化物是XO2 | ||
| C. | X應為非金屬元素 | D. | X的最高價氧化物的水化物是強酸 |
分析 根據電子排布規律寫出該原子原子結構示意圖,根據電子層數判斷周期數,根據價電子判斷所屬族數,根據在周期表中的位置判斷判斷其化合物的性質.
解答 解:該原子的原子結構示意圖為: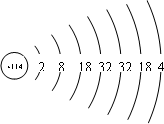 ,最外層有4個電子,屬于第IVA族元素,在鉛元素下方,金屬性比鉛強,
,最外層有4個電子,屬于第IVA族元素,在鉛元素下方,金屬性比鉛強,
A.同主族從上到下,氫化物的穩定性減弱,則X的氣態氫化物的穩定性比甲烷弱,故A錯誤;
B.X元素的原子最外層有4個電子,則最高價氧化物是XO2,故B正確;
C.屬于第IVA族元素,在鉛元素下方,金屬性比鉛強,屬于金屬元素,故C錯誤;
D.X在鉛元素下方,金屬性比鉛強,屬于金屬元素,則X的最高價氧化物的水化物顯堿性,故D錯誤.
故選B.
點評 本題考查根據原子結構示意圖、原子結構和性質,側重于同主族元素性質的變化規律的考查,注意判斷元素所屬周期和族,比較容易.


 每日10分鐘口算心算速算天天練系列答案
每日10分鐘口算心算速算天天練系列答案科目:高中化學 來源: 題型:選擇題
| A. | 2-甲基-1-丁烯 | B. | 2-甲基-2-丁烯 | ||
| C. | 3-甲基-1-丁炔 | D. | 3,3-二甲基-1-丁炔 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 實驗室用圖示裝置制取乙酸乙酯.
實驗室用圖示裝置制取乙酸乙酯.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 放熱91.5 kJ | B. | 放熱183 kJ | C. | 吸熱183 kJ | D. | 吸熱91.5 kJ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Te與H2的反應比S與H2反應困難 | B. | TeO3對應的水化物是一種酸 | ||
| C. | H2Te的還原性比H2S弱 | D. | 有-2、+4、+6三種化合價 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
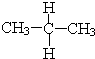 與
與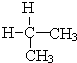 ⑦CH3CH3與
⑦CH3CH3與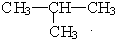
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Cl-、Br-、CrO42- | B. | CrO42-、Br-、Cl- | C. | Br-、Cl-、CrO42- | D. | Br-、CrO42-、Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 中國全運會期間,在濟南市等主要街道上,出現了一座座拔地而起的立體花壇,4000萬盆、上百種鮮花扮靚了濟南街頭.大量盆栽鮮花因施用了S-誘抗素制劑,得以保證鮮花盛開,S-誘抗素的分子結構如右圖,下列關于該分子的說法正確的是( )
中國全運會期間,在濟南市等主要街道上,出現了一座座拔地而起的立體花壇,4000萬盆、上百種鮮花扮靚了濟南街頭.大量盆栽鮮花因施用了S-誘抗素制劑,得以保證鮮花盛開,S-誘抗素的分子結構如右圖,下列關于該分子的說法正確的是( )| A. | 1mol該物質與足量的NaOH溶液反應最多消耗2mol NaOH | |
| B. | 該物質在Cu作催化劑條件下能被催化氧化 | |
| C. | 該物質能發生氧化、還原、取代反應 | |
| D. | 分別與足量的Na、NaHCO3 反應生成的氣體在相同狀況下體積比為2:1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com