
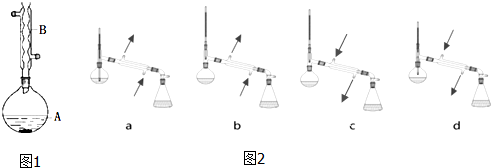
分析 在裝置A中加入反應混合物和2~3片碎瓷片,開始緩慢加熱A,利用冷凝管冷凝回流50分鐘,反應液冷至室溫后,倒入分液漏斗中,先用少量水洗掉大部分硫酸和醋酸,再用水洗滌碳酸氫鈉溶液,分出的產物加入少量無水硫酸鎂固體作干燥劑,靜置片刻,過濾除去硫酸鎂固體,進行蒸餾純化,收集140~143℃餾分,得乙酸異戊酯,還考查了反應物轉化率的提高方法,同時進行產率的計算有誤差分析.
(1)根據題中儀器B的構造判斷該儀器的名稱;
(2)酸脫羥基,醇脫氫,乙酸與乙醇在濃硫酸作用下加熱發生酯化反應生成乙酸乙酯和水,濃硫酸為催化劑和吸水劑;
(3)酯化反應的本質為酸脫羥基,醇脫氫,乙酸與乙醇在濃硫酸作用下加熱發生酯化反應生成乙酸乙酯和水;
(4)根據乙酸異戊酯的密度及正確的分液操作方法進行解答;
(5)少量無水硫酸鎂能夠吸收乙酸異戊酯中少量的水分,起到干燥作用;
(6)先根據溫度計在蒸餾操作中的作用排除ad,再根據球形冷凝管容易使產品滯留,不能全部收集到錐形瓶中,得出正確結論;
(7)先判斷過量情況,根據反應方程式及不足量計算出生成乙酸乙酯的質量,然后計算出乙酸乙酯的產率
解答 解:(1)由裝置中儀器B的構造可知,儀器B的名稱為球形冷凝管,
故答案為:球形冷凝管;
(2)酸脫羥基,醇脫氫,乙酸與乙醇在濃硫酸作用下加熱發生酯化反應生成乙酸乙酯和水,濃硫酸為催化劑和吸水劑;
(3)酯化反應的本質為酸脫羥基,醇脫氫,乙酸與乙醇在濃硫酸作用下加熱發生酯化反應生成乙酸乙酯和水,該反應為可逆反應為:CH3COOH+C2H5OH$?_{△}^{濃硫酸}$CH3COOC2H5+H2O,
故答案為:CH3COOH+C2H5OH$?_{△}^{濃硫酸}$CH3COOC2H5+H2O;
(4)由于酯的密度比水小,二者互不相溶,因此水在下層,酯在上層;分液時,要先將水層從分液漏斗的下口放出,待到兩層液體界面時關閉分液漏斗的活塞,再將乙酸異戊酯從上口放出,所以正確的為D,
故答案為:D;
(5)實驗中加入少量無水硫酸鎂的目的是吸收酯中少量的水分,對乙酸異戊酯進行干燥,
故答案為:干燥;
(6)在蒸餾操作中,溫度計的水銀球要放在蒸餾燒瓶的支管口處,所以ad錯誤;c中使用的是球形冷凝管容易使產品滯留,不能全部收集到錐形瓶中,因此儀器及裝置安裝正確的是b,
故答案為:b;
(7)4.6g乙醇的物質的量為0.1mol,9g乙酸的物質的量是0.15mol.0.1mol乙醇完全反應消耗0.1mol的乙酸,乙酸有剩余,所以需要根據乙醇的量來計算生成的乙酸乙酯的量.根據反應CH3COOH+CH3CH2OH$\frac{\underline{\;濃硫酸\;}}{△}$CH3COOCH2CH3+H2O可知,理論上生成乙酸乙酯的物質的量為0.1mol,即8.8g.實際生成了5.28g,則乙酸乙酯的產率為:$\frac{5.25g}{8.8g}×100%$≈60%
故答案為:d
點評 本題為一道高考題真題,考查了常見儀器的構造與安裝、混合物的分離、提純、物質的制取、藥品的選擇及使用、物質產率的計算等知識,題目難度較大,試題涉及的題量較大,知識點較多,充分培養了學生的分析、理解能力及靈活應用所學知識的能力.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源:2016-2017學年安徽師大附中高二上10月月考化學卷(解析版) 題型:選擇題
在一 定條件下,對于A2(g)+3B2(g)
定條件下,對于A2(g)+3B2(g) 2AB3(g)反應來說,下列所表示的化學反應速率中最大的
2AB3(g)反應來說,下列所表示的化學反應速率中最大的 是
是
A.v(A2)=0.8 mol·L-1·s-1 B.v(A2)=40 mol·L-1·min-1
C.v(AB3)=1.0 mol·L-1·s-1 D.v(B2)=1.2 mol·L-1·s-1
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 物質 | 熔點(℃) | 沸點(℃) | 密度(g•cm-3) |
| 乙醇 | -117.3 | 78.5 | 0.79 |
| 乙酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.90 |
| 濃硫酸 | - | 338.0 | 1.84 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
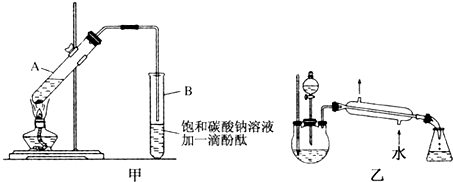
 某課外小組設計的實驗室制取乙酸乙酯的裝置如圖所示,A中盛有濃硫酸,B中盛有無水乙醇和冰醋酸.
某課外小組設計的實驗室制取乙酸乙酯的裝置如圖所示,A中盛有濃硫酸,B中盛有無水乙醇和冰醋酸.| 試劑 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸點(℃) | 34.7 | 78.5 | 118 | 77.1 |
 CH3CO18OCH2CH3+H2O.
CH3CO18OCH2CH3+H2O.查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
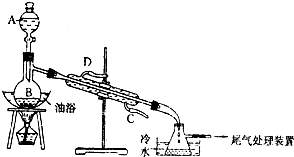
 乙酸乙酯是重要的有機合成中間體,廣泛應用于化學工業.某學生在實驗室利用如圖的實驗裝置制備乙酸乙酯并研究其反應條件.
乙酸乙酯是重要的有機合成中間體,廣泛應用于化學工業.某學生在實驗室利用如圖的實驗裝置制備乙酸乙酯并研究其反應條件.| 物質 | 沸點/°C | 密度/g?cm-3 |
| 乙醇 | 78.0 | 0.79 |
| 乙酸 | 117.9 | 1.05 |
| 乙酸乙酯 | 77.5 | 0.90 |
| 異戊醇 | 131 | 0.8123 |
| 乙酸異戊酯 | 142 | 0.8670 |
| 實驗編號 | 試管Ⅰ中的試劑 | 測得有機層的厚度/cm |
| A | 2mL乙醇、2mL乙酸、1mL 18mol/L濃硫酸 | 5.0 |
| B | 3mL乙醇、2mL乙酸 | 0.1 |
| C | 3mL乙醇、2mL乙酸、6mL 3mol/L硫酸 | 1.2 |
| D | 3mL乙醇、2mL乙酸、鹽酸 | 1.2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
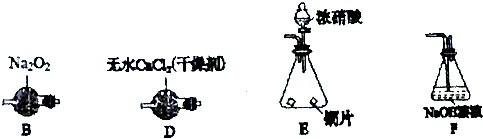
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
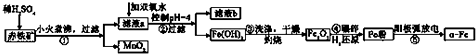
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 6.7 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
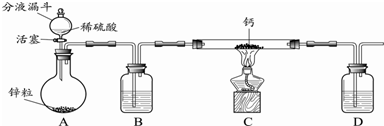
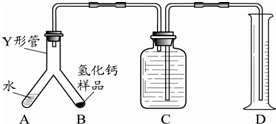
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com