
| A. | 煤的干餾和煤的液化均是物理變化 | |
| B. | 用活性炭為糖漿脫色和用次氯酸鹽漂白紙漿的原理相同 | |
| C. | 天然纖維和合成纖維的主要成分都是纖維素 | |
| D. | 海水淡化的方法有蒸餾法、電滲析法等 |
分析 A.煤的干餾和煤的液化都是化學變化;
B.活性炭脫色是利用其吸附性;
C.蠶絲是天然纖維;
D.海水淡化是指除去海水中的鹽分以獲得淡水的工藝過程(又稱海水脫鹽),其方法較多.
解答 解:A.煤的干餾是指將煤隔絕空氣加強熱使之分解的過程,煤液化生成甲醇,屬于化學變化,故A錯誤;
B.活性炭脫色是利用其吸附性,次氯酸鹽漂白是利用次氯酸的強氧化性,故B錯誤;
C.蠶絲是天然纖維,成分為蛋白質,合成纖維的成分是化學纖維,如聚乙烯,故C錯誤;
D.海水淡化是指除去海水中的鹽分以獲得淡水的工藝過程(又稱海水脫鹽),蒸餾是分離和提純液態混合物常用的方法之一蒸餾法是人類最早使用的淡化海水的方法,技術和工藝比較完備;離子交換法是用陽離子交換樹脂(HR)和水中的金屬離子Mn+進行交換的一種方法,通常通過陽離子交換樹脂可以除去鈣離子和鎂離子得到軟水,不是歷史最久、技術和工藝較完善的主要方法;電滲析法是一種利用離子交換膜進行離子交換的方法,是近年發展起來的一種較好的海水淡化技術,原理為通電后,陰離子移向陽極,陽離子移向陰極,分離鹽和水,故D正確.
故選D.
點評 本題考查化學與生活、環境的關系,為高考常見考題,為理綜中化學選擇題首先出現的習題,涉及知識面較廣,側重分析與應用、化學與生活、環境等綜合知識的考查,題目難度不大.


 輕巧奪冠周測月考直通中考系列答案
輕巧奪冠周測月考直通中考系列答案科目:高中化學 來源: 題型:選擇題
| A. | 用酚酞試紙 | B. | 用濕潤的藍色石蕊試紙 | ||
| C. | 用硝酸銀溶液 | D. | 用濕潤的淀粉-KI試紙 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | (10-8+10-10)mol•L-1 | B. | (10-4+10-6)mol•L-1 | ||
| C. | (10-6+10-10)mol•L-1 | D. | 2×10-10 mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
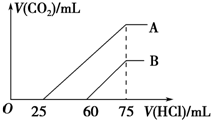 向濃度相等、體積均為50mL的A、B兩份NaOH溶液中,分別通入一定量的CO2后,再稀釋到100mL.在稀釋后的溶液中逐滴加入0.1mol.L-1的鹽酸,產生CO2的體積(標準狀況)與所加鹽酸的體積關系如圖所示.下列說法正確的是( )
向濃度相等、體積均為50mL的A、B兩份NaOH溶液中,分別通入一定量的CO2后,再稀釋到100mL.在稀釋后的溶液中逐滴加入0.1mol.L-1的鹽酸,產生CO2的體積(標準狀況)與所加鹽酸的體積關系如圖所示.下列說法正確的是( )| A. | 在NaOH溶液中通入一定量的CO2后,溶液中溶質的組成可能是①NaOH、Na2CO3 ②Na2CO3③Na2CO3、NaHCO3 ④NaHCO3 | |
| B. | B曲線說明,原溶液通入CO2后,所得溶質與鹽酸反應產生CO2的最大體積是11.2L(標準狀況) | |
| C. | 原NaOH溶液的物質的量濃度為0.100mol/L | |
| D. | B曲線表明,原溶液通入CO2后,所得溶液中溶質的化學式為NaOH、Na2CO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
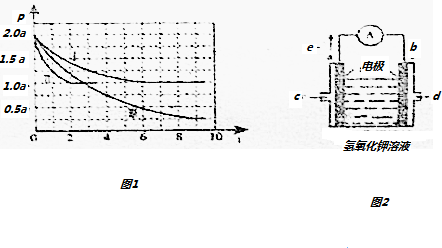
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 5min內平均反應速率vA=0.15mol•L-1•min-1 | |
| B. | 當同時對原平衡體系升高一定溫度和增加一定壓強時,達平衡后,C的物質的量分數為60%,則該反應的正反應為吸熱反應 | |
| C. | 保持其他條件不變,若起始時向容器中加入0.5molA、0.5molB、1.5molC,則反應將向逆反應方向進行 | |
| D. | t℃,向2L密閉、恒容容器中仍充入1molA和1molB,反應達到平衡狀態時,C的物質的量分數小于60% |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 已知反應:2SO2(g)+O2(g)?2SO3(g)△H<0.一定溫度下,在容積為2L的甲、乙、丙三個恒溫密閉容器中,充入的SO2(g)和O2(g)的量如圖所示:
已知反應:2SO2(g)+O2(g)?2SO3(g)△H<0.一定溫度下,在容積為2L的甲、乙、丙三個恒溫密閉容器中,充入的SO2(g)和O2(g)的量如圖所示:| A. | 三個容器中的反應速率相同 | |
| B. | 丙中的平衡常數最大,甲中最小 | |
| C. | 當容器甲中SO2的轉化率為80%時,該反應的平衡常數為160 | |
| D. | 達到平衡時,容器丙中的c(SO3)是容器甲中的兩倍 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 將0.1mol的鎂、鋁混合物溶于100mL 2mol•L-1的H2SO4溶液中,然后再滴加1mol•L-1的NaOH溶液.請回答:
將0.1mol的鎂、鋁混合物溶于100mL 2mol•L-1的H2SO4溶液中,然后再滴加1mol•L-1的NaOH溶液.請回答:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com