
 (1分) (2)FeS2 (1分)
(1分) (2)FeS2 (1分)

科目:高中化學 來源:不詳 題型:問答題
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
查看答案和解析>>
科目:高中化學 來源:不詳 題型:實驗題
|
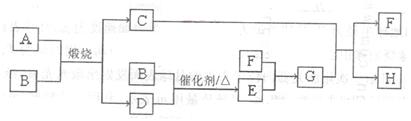
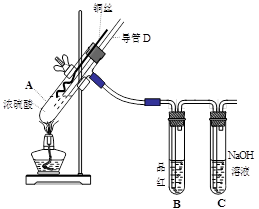
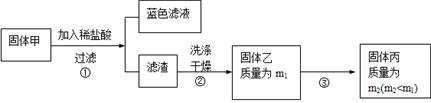 (3) 固體乙在空氣中煅燒時,使用的實驗儀器除了玻璃棒、三腳架、酒精燈外,還必須有: 。
(3) 固體乙在空氣中煅燒時,使用的實驗儀器除了玻璃棒、三腳架、酒精燈外,還必須有: 。查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.產物中硝酸銅的物質的量為0.025 mol |
| B.若混合物中Cu的物質的量為0.005 mol,則其中Cu2O、CuO的物質的量共0.020 mol |
| C.若混合物中含0.01 mol Cu,則其中Cu2O、CuO的物質的量均為0.005 mol |
| D.混合物中Cu的物質的量的取值范圍為0.005 mol<n(Cu)<0.015 mol |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:推斷題
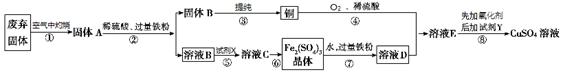
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.將銅絲插入濃硫酸中加熱,反應后把水加入反應器中,觀察硫酸銅溶液的顏色 |
| B.常溫下將銅絲伸入盛滿氯氣的集氣瓶中,觀察CuCl2的生成 |
| C.將CuCl2溶液在蒸發皿中加熱蒸干,得到無水CuCl2固體 |
| D.將表面有銅綠[Cu2(OH)2CO3]的銅器放入鹽酸中浸泡,除去銅綠 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.利用鐵加入硫酸銅溶液中的反應可以比較Cu、Fe2+的還原性 |
| B.足量的銅跟一定量的濃硝酸反應只產生一種氣體 |
| C.氮的固定只有在高溫、高壓、催化劑的條件下才能實現 |
| D.以鐵為陰極、銅片為陽極、硫酸銅為電鍍液可以實現鐵制品鍍銅 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:實驗題
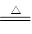 (x+y)Cu+xCO2+(x+2y+z)H2O
(x+y)Cu+xCO2+(x+2y+z)H2O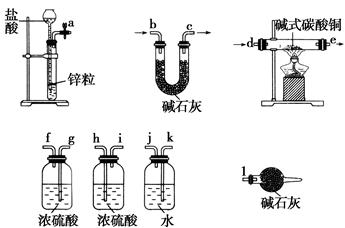
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com