
下列說法正確的是
A.石油裂解可以得到氯乙烯
B.油脂水解可得到氨基酸和甘油
C.所有烷烴和蛋白質中都存在碳碳單鍵
D.淀粉和纖維素水解的最終產物都是葡萄糖
 期末沖刺100分創新金卷完全試卷系列答案
期末沖刺100分創新金卷完全試卷系列答案科目:高中化學 來源:2016-2017學年安徽省高一上第一次月考化學試卷(解析版) 題型:選擇題
標準狀況下,①6.72 L NH3 ②1.204×1023個 H2S ③5.6 g CH4 ④0.5 mol HCl ,下列關系正確的是
A、體積大小: ④>③>②>① B、原子數目: ③>①>④>②
C、密度大小:④>②>③>① D、質量大小:④>③>②>①
查看答案和解析>>
科目:高中化學 來源:2017屆云南省高三上學期第二次月考化學卷(解析版) 題型:實驗題
用二氧化氯(ClO2)、高鐵酸鈉(Na2FeO4,摩爾質量為166g/mol)等新型凈水劑替代傳統的凈水劑Cl2對淡水進行消毒是城市飲用水處理新技術。ClO2和Na2FeO4在水處理過程中分別被還原為Cl-和Fe3+。
(1)Na2FeO4之所以能凈水、殺菌、消毒,原因是 。
(2)已知二氧化氯是一種黃綠色有刺激性氣味的有毒氣體,其熔點為-59℃,沸點為11.0℃,易溶于水。工業上用稍潮濕的KClO3和草酸(H2C2O4)在60℃時反應制得。用下圖所示的裝置模擬工業制取及收集ClO2。
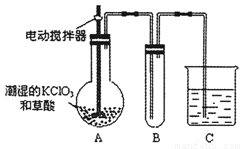
①A中反應產物有K2CO3、ClO2等,請寫出反應方程式 。
②A部分還應添加溫度控制裝置,如水浴加熱或酒精燈、溫度計,B部分還應補充的裝置為 (說明原因)。
③該裝置按②補充完整后,裝置A、B、C中還有一處設計明顯不合理的是 (填“A”“B”或“C”),請畫出正確的裝置圖。
④ClO2需隨用隨制,產物用水吸收得到ClO2溶液。為測定所得溶液中ClO2的含量,進行了下列實驗:
步驟1:準確量取ClO2溶液10ml,稀釋成100ml試樣;量取V1ml試樣加入錐形瓶中;
步驟2:調節試樣的pH≤2.0,加入足量的KI晶體,靜置片刻;
步驟3:加入淀粉指示劑,用cmol/LNa2S2O3溶液滴定至終點,消耗Na2S2O3溶液V2ml。(已知2Na2S2O3+I2=Na2S4O6+2NaI)
步驟2的目的 (用離子方程式表示)。當 時,可以判斷此滴定操作達到終點;由以上數據可以計算原ClO2溶液的濃度為 g/L(用含字母的代數式表示)。
查看答案和解析>>
科目:高中化學 來源:2017屆云南省高三上學期第二次月考化學卷(解析版) 題型:選擇題
下列實驗設計能完成或實驗結論合理的是
A. 測氯水的pH,可用玻璃棒蘸取氯水點在pH試紙上,待其變色后和標準比色卡比較
B. NH4Cl固體中混有少量的I2,可用加熱的方法將I2除去
C. 用濃硫酸吸收二氧化硫中混有少量SO3氣體
D. 少量金屬鋰保存在煤油中
查看答案和解析>>
科目:高中化學 來源:2017屆新疆生產建設兵團二中高三上第二次月考化學卷(解析版) 題型:選擇題
符合右圖的反應是
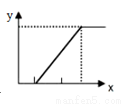
x軸 | y軸 | ||
A | 向氯化鋁溶液中加入氫氧化鈉溶液 | 氫氧化鈉的物質的量 | 生成沉淀的質量 |
B | 向碳酸鈉溶液中加入稀鹽酸 | 鹽酸的體積 | 產生氣體的體積 |
C | 向溴化亞鐵溶液中通入氯氣 | 氯氣的體積 | 生成Br2的物質的量 |
D | 向氫氧化鈣溶液中通入二氧化碳 | 二氧化碳的體積 | 生成碳酸氫鈣的質量 |
查看答案和解析>>
科目:高中化學 來源:2017屆新疆生產建設兵團二中高三上第二次月考化學卷(解析版) 題型:選擇題
某溶液中含有的溶質是FeBr2、FeI2,若先向該溶液中通入一定量的氯氣,再向反應后的溶液中滴加KSCN溶液,溶液變為紅色,則下列敘述正確的是
①原溶液中的Br-一定被氧化;
②通入氯氣之后原溶液中的Fe2+一定有部分或全部被氧化;
③不能確定通入氯氣后的溶液中是否存在Fe2+;
④若取少量所得溶液,再加入CCl4溶液,靜置、分液,向上層溶液中加入足量的AgNO3溶液,只產生白色沉淀,說明原溶液中的I-、Fe2+、Br-均被完全氧化
A.①③④ B.①②③ C.②③④ D.①②③④
查看答案和解析>>
科目:高中化學 來源:2017屆新疆生產建設兵團二中高三上第二次月考化學卷(解析版) 題型:選擇題
I2Cl6體在常溫下就會“升華”,蒸氣冷卻可得到晶體ICl3。ICl3遇水會產生大量的腐蝕性白色煙霧,有強烈的催淚性。若生成物之一是HCl,則另一種是
A.HIO2 B.HIO2 C.HIO3 D.ICl
查看答案和解析>>
科目:高中化學 來源:2017屆黑龍江省高三10月月考化學卷(解析版) 題型:選擇題
某興趣小組設計如圖所示微型實驗裝置。實驗時,先斷開K2,閉合K1,兩極均有氣泡產生;一段時間后,斷開K1、閉合K2,發現電流表A指針偏轉。下列有關描述正確的是( )
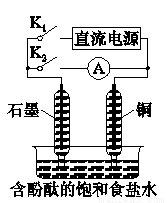
A.斷開K2,閉合K1時,總反應的離子方程式為:
2H++2Cl-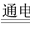 Cl2↑+H2↑
Cl2↑+H2↑
B.斷開K2,閉合K1時,石墨電極附近溶液變紅
C.斷開K1,閉合K2時,銅電極上的電極反應式為:Cl2+2e-=2Cl-
D.斷開K1,閉合K2時,石墨電極作正極
查看答案和解析>>
科目:高中化學 來源:2016-2017學年福建省四地六校高二上第一次月考化學試卷(解析版) 題型:填空題
用100mL 1.00mol·L-1鹽酸與100mL 1.10mol·L-1NaOH溶液在如下圖所示的裝置中進行中和熱測定實驗。以下是四次實驗所得數據。回答下列問題:

實驗 數據 | 鹽酸起始溫度t1/℃ | 氫氧化鈉起始溫度t2/℃ | 兩溶液混合后 溫度t3/℃ |
1 | 21.0 | 21.1 | 26.9 |
2 | 21.5 | 21.7 | 28.2 |
3 | 21.9 | 22.1 | 28.7 |
4 | 22.3 | 22.5 | 29.2 |
(1)上表中的溫度差平均值為 ℃
(2)近似認為上述兩種溶液的密度都是1 g·cm-3,中和后生成溶液的比熱容c=4.18J·(g·℃)-1。則計算得到中和熱ΔH= (取小數點后一位)。
(3)上述實驗數值結果與57.3 kJ·mol-1有偏差,產生偏差的原因可能是(填字母) 。
a.實驗裝置保溫、隔熱效果差
b.用環形銅質攪拌棒代替環形玻璃攪拌棒
c.分多次把NaOH溶液倒入盛有鹽酸的小燒杯中
d.用溫度計測定鹽酸溶液起始溫度后直接測定NaOH溶液的溫度
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com