
分析 (1)氯化鐵和銅反應生成氯化亞鐵和氯化銅,依據離子方程式書寫方法寫出;用KSCN溶液檢驗Fe3+的存在;
(2)過程Ⅰ加入鐵屑的主要作用是和氯化銅發生反應生成銅,過濾后得到固體為Fe和Cu,加入鹽酸鐵反應,銅不反應過濾分離得到銅;
(3)濾液成分為氯化亞鐵溶液,加入石灰水反應生成氫氧化亞鐵沉淀,在空氣中迅速氧化為氫氧化鐵;
(4)過程Ⅱ中調節溶液的pH為,氫氧化鐵沉淀溶液中存在沉淀溶解平衡,依據溶度積常數計算.
解答 解:(1)FeCl3蝕刻銅箔反應是三價鐵離子具有氧化性和銅反應生成亞鐵離子和銅離子,反應的離子方程式為:2Fe3++Cu=2Fe2++Cu2+;向溶液中加入KSCN溶液,若溶液變紅,則證明混合物溶液仍存在Fe3+,故答案為:2Fe3++Cu=2Fe2++Cu2+;取少量反應后的溶液于潔凈的試管中,向其中滴加KSCN溶液,若出現紅色溶液,則證明仍存在Fe3+;
(2)向廢液中投入過量鐵屑,鐵會和三氯化鐵溶液反應生成氯化亞鐵,和氯化銅反應生成銅和氯化亞鐵,所以加入鐵粉是為了得到銅,過濾得到固體是過量的鐵和銅,用鹽酸溶解鐵反應,銅不反應過濾得到銅,
故答案為:做還原劑,回收銅;加入鹽酸反應后過濾;
(3)濾液成分為氯化亞鐵溶液,加入石灰水反應生成氫氧化亞鐵沉淀,在空氣中迅速氧化為氫氧化鐵;反應的化學方程式為:FeCl2+Ca(OH)2=Fe(OH)2↓+CaCl2、4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案為:FeCl2+Ca(OH)2=Fe(OH)2↓+CaCl2 、4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(4)過程Ⅱ中調節溶液的pH為5,常溫下溶液中氫氧根離子濃度為10-9mol/L,依據溶度積常數計算鐵離子濃度,Fe(OH)3(s)?Fe3++3OH-;Ksp=c(Fe3+)×c3(OH-);c(Fe3+)=$\frac{4.0×1{0}^{-38}}{(1{0}^{-9})^{3}}$=4×10-11mol/L;
故答案為:4×10-11mol/L.
點評 本題考查了鐵離子的氧化性,提取銅的反應過程和步驟分析判斷,氫氧化鐵氫氧化亞鐵的轉化反應,溶度積的計算應用,題目難度中等.


科目:高中化學 來源: 題型:多選題
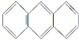 )和菲(
)和菲(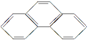 )都是比較簡單的稠環芳香烴,有關它們的說法正確的是( )
)都是比較簡單的稠環芳香烴,有關它們的說法正確的是( )| A. | 蒽和菲屬于同系物 | |
| B. | 蒽和菲屬于同分異構體 | |
| C. | 蒽的一氯代物有3種,而菲的一氯代物有5種 | |
| D. | 蒽和菲均可以看成是苯的同系物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH3CH2COOCH(CH3)2 | B. | CH3CH2COOCH2CH=CH2 | ||
| C. | (CH3)2CHCOOCH2CH(CH3)2 | D. | CH3CH2CH2COOCH2CH(CH3)2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鋁片加入到少量濃燒堿溶液中:Al+3OH-═Al(OH)3 | |
| B. | 向明礬溶液中滴加Ba(OH)2溶液,使SO42-全部沉淀:2Al++6OH-+3SO42-+3Ba2+═2Al(OH)3↓+3BaSO4↓ | |
| C. | NaHSO4溶液與Ba(OH)2溶液反應至中性:2H++2OH-+SO42-+Ba2+═BaSO4↓+2H2O | |
| D. | 用惰性電極電解 飽和氯化鈉溶液:2Cl-+2H+═H2↑+Cl2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 加入KSCN溶液變紅色的溶液:NH4+、K+、I-、SO42- | |
| B. | 在pH=11的溶液中:Na+、AlO2-、NO3-、S2-、SO32- | |
| C. | 由水電離的c(OH-)=10-13mol•L-1的溶液中:Na+、Cl-、HCO3-、NO3- | |
| D. | 使甲基橙變紅色的溶液:Fe2+、K+、SO42-、NO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 80mL 10mol•L-1 鹽酸與足量MnO2加熱反應,產生Cl2分子數為0.2NA | |
| B. | 2 L0.5 mol•L-1硫酸鉀溶液中陰離子所帶電荷數為NA | |
| C. | 標況下,11.2 L氯氣完全溶于1 L水中,所得溶液中Cl-和ClO-兩種粒子數之和為NA | |
| D. | 標準狀況下,11.2LSO3所含的分子數大于0.5NA |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com