
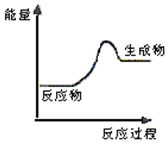
| A. | 該反應可能為吸熱反應 | |
| B. | 該反應一定有能量轉化成了生成物的化學能 | |
| C. | 反應物比生成物穩定 | |
| D. | 生成物的總能量高于反應物的總能量,反應不需要加熱 |
科目:高中化學 來源: 題型:選擇題
| 化學式 | CH3COOH | HCN |
| 電離平衡常數 | 1.8×10-5 | 4.9×10-10 |
| A. | 體積和pH相同的CH3COOH溶液與HCN溶液,分別與足量的Fe反應,HCN溶液產生的H2更多 | |
| B. | 體積和pH相同的CH3COOH溶液與HCN溶液,中和NaOH溶液所消耗NaOH的物質的量相同 | |
| C. | amol•L-1HCN溶液加水稀釋后,電離平衡常數減小,加入KCN晶體后,電離平衡常數增大 | |
| D. | 25℃時,在等濃度的CH3COOH溶液與HCN溶液中,水的電離程度前者大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 新制的氯水在光照條件下顏色變淺 | |
| B. | H2、I2、HI平衡混合氣體加壓后顏色變深 | |
| C. | 鋼鐵在潮濕的空氣中容易生銹 | |
| D. | 加入催化劑有利于氨催化氧化的反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 實驗室要配制0.lmol/LNaOH溶液400mL,需稱取NaOH 固體1.6g | |
| B. | 焰火的五彩繽紛是某些金屬元素化學性質的展現 | |
| C. | Al2O3熔點很高,可用作耐火材料 | |
| D. | 純鋅和鐵相連接后,插入同一稀鹽酸中,鋅極上發生氧化還原反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
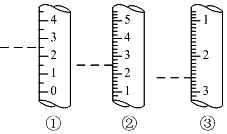 托盤天平、容量瓶、量筒是常見的中學化學計量儀器,熟知這些儀器的使用是定量研究化學的基礎.
托盤天平、容量瓶、量筒是常見的中學化學計量儀器,熟知這些儀器的使用是定量研究化學的基礎.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | $\frac{z}{12m}$ | B. | $\frac{12z}{m}$ | C. | $\frac{{N}_{A}}{m}$ | D. | $\frac{{N}_{A}}{z}$ |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
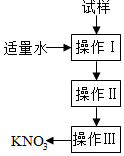 實驗室提純含少量氯化鈉雜質的硝酸鉀的過程如圖所示.下列分析正確的是( )
實驗室提純含少量氯化鈉雜質的硝酸鉀的過程如圖所示.下列分析正確的是( )| A. | 操作Ⅰ是過濾,將固體分離除去 | |
| B. | 操作Ⅱ是加熱濃縮,趁熱過濾,除去雜質氯化鈉 | |
| C. | 操作Ⅲ是過濾、洗滌,將硝酸鉀晶體從溶液中分離出來 | |
| D. | 操作Ⅰ~Ⅲ總共只需一次過濾操作 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 實驗編號 | NaOH溶液的濃度 (mol/L) | 滴定完成時,NaOH溶液滴入的體積(mL) | 待測鹽酸溶液的體積 (mL) |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.72 | 20.00 |
| 3 | 0.10 | 22.80 | 20.00 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 溫度/℃ | 1000 | 1100 |
| 平衡常數 | 0.68 | 0.50 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com