
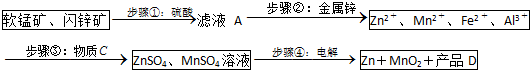
| Zn2+ | Mn2+ | Fe2+ | Fe3+ | Al3+ | |
| pH | 8.0 | 10.1 | 9.0 | 3.2 | 4.7 |
分析 (1)MnO2在酸性溶液中分別和CuS和FeS發生氧化還原反應,Mn元素的化合價降低,S元素的化合價升高,且Fe元素化合價升高;
(2)濾液A中含金屬離子,加Zn發生置換反應;
(3)由轉化可知,鐵離子、鋁離子轉化為沉淀;
(4)步驟④中電解過程中MnO2應在陽極生成,因Mn元素失去電子,陰極上Zn得到電子,得到的硫酸可循環使用.
解答 解:(1)MnO2在酸性溶液中分別和CuS和FeS發生氧化還原反應,Mn元素的化合價降低,S元素的化合價升高,且Fe元素化合價升高,由電子、原子守恒可知,反應分別為MnO2+CuS+2H2SO4=MnSO4+CuSO4+S↓+2H2O、MnO2+2FeS+6H2SO4=Fe2(SO4)3+3MnSO4+2S↓+6H2O,
故答案為:MnO2+CuS+2H2SO4=MnSO4+CuSO4+S↓+2H2O;MnO2+2FeS+6H2SO4=Fe2(SO4)3+3MnSO4+2S↓+6H2O;
(2)步驟②加入金屬鋅發生如下反應:Zn+CuSO4═ZnSO4+Cu,Zn+CdSO4═ZnSO4+Cd,Zn+2Fe3+═Zn2++2Fe2+,過濾得濾液B,其中的成分有MnSO4、Al2(SO4)3、ZnSO4、FeSO4,濾渣乙中有Cu、Cd,加以回收,
故答案為:Cu、Cd;
(3)由轉化可知,鐵離子、鋁離子轉化為沉淀,其中一種為MnO2,其作用是將Fe2+氧化為Fe3+;另外一種固體物質可為Zn(OH)2(Mn(OH)2、ZnCO3、MnCO3等)促進鐵離子水解轉化為沉淀,
故答案為:將Fe2+氧化為Fe3+;Zn(OH)2;
(4)因Mn元素失去電子,可知步驟④中電解過程中MnO2在陽極析出,該電極上發生的反應方程式為Mn2+-2e-+2H2O=MnO2+4H+,硫酸根離子不變,且生成氫離子,可知產品D的化學式為H2SO4,該物質對整個生產的意義是用于溶解軟錳礦和閃鋅礦,循環使用,
故答案為:陽;Mn2+-2e-+2H2O=MnO2+4H+;H2SO4;用于溶解軟錳礦和閃鋅礦,循環使用.
點評 本題考查混合物分離提純的綜合應用及物質制備實驗,為高頻考點,題目難度中等,明確簡化流程中的反應原理、混合物分離方法為解答的關鍵,試題側重分析與應用能力的考查.


科目:高中化學 來源: 題型:解答題
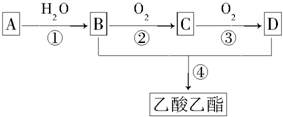
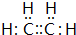 ;C的分子式是C2H4O.
;C的分子式是C2H4O.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
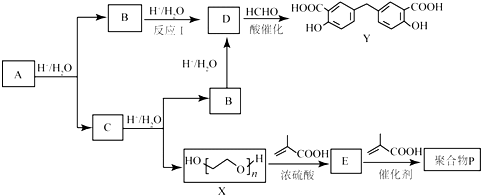
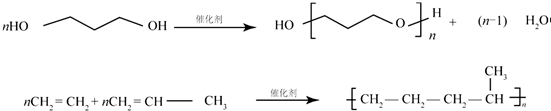
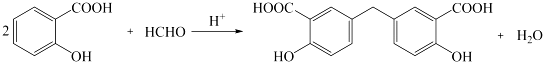 .
.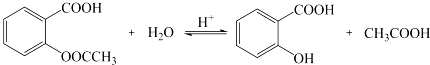 .
.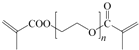 .
.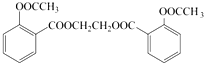 .
.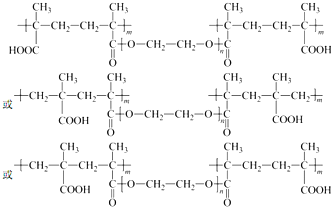 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
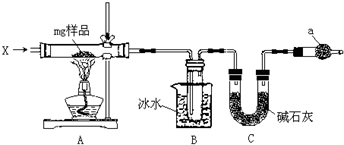
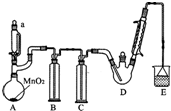 某探究小組設計如圖所示裝置(夾持、加熱儀器略),模擬工業生產進行制備三氯乙醛(CCl3CHO)的實驗.查閱資料,有關信息如下:
某探究小組設計如圖所示裝置(夾持、加熱儀器略),模擬工業生產進行制備三氯乙醛(CCl3CHO)的實驗.查閱資料,有關信息如下:| C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
| 相對分子質量 | 46 | 147.5 | 163.5 | 64.5 |
| 熔點/℃ | -114.1 | -57.5 | 58 | -138.7 |
| 沸點/℃ | 78.3 | 97.8 | 198 | 12.3 |
| 溶解性 | 與水互溶 | 可溶于水、乙醇 | 可溶于水、乙醇、三氯乙醛 | 微溶于水,可溶于乙 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
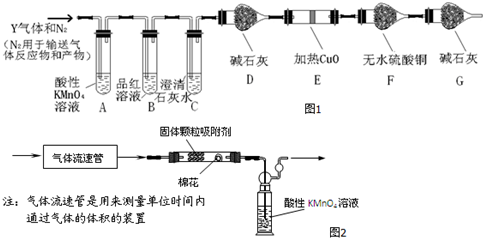
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 126C和146C是一種核素 | |
| B. | 紅磷和白磷互為同素異形體 | |
| C. | CH3COOCH2CH3和CH3CH2COOCH3是不同物質 | |
| D. | CH3CH2OH可看成是由-C2H5和-OH兩種基團組成 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
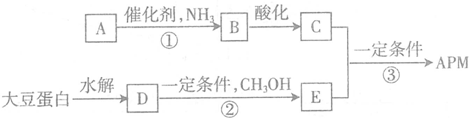
 .C中所含官能團的名稱為羧基、氨基.
.C中所含官能團的名稱為羧基、氨基. .
.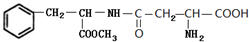 和
和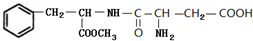 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com