
【題目】鋼鐵很容易生銹而被腐蝕,每年因腐蝕而損失的鋼材占世界鋼鐵年產量的1/10。
(1)鋼鐵腐蝕主要是吸氧腐蝕,該腐蝕過程中的電極反應式。
正極:_____________________;負極:____________________。
(2)為了降低某水庫的鐵閘門被腐蝕的速率,可以采用下圖所示甲的方案,其中焊接在鐵閘門的固體材料R可以采用_______________。
A.銅 B.鈉 C.鋅 D.石墨
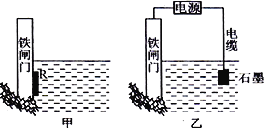
(3)上圖中乙方案也可降低鐵閘門腐蝕速率,其中鐵閘門應該連接在直流電源的_____________極。
(4)除了以上金屬防護的方法外,請再例舉兩種辦法:___________;___________。
【答案】O2+4e-+2H2O=4OH- 2Fe-4e- = 2Fe2+ C 負 改變金屬組成或內部結構 在金屬的表面覆蓋保護層(其它合理答案也可以)
【解析】
如圖甲所示,鐵閘門-金屬R-海水構成原電池,鐵做正極得到保護,所以屬于原電池原理。如圖乙所示,鐵閘門與電源負極相連,作陰極,得到保護,該裝置稱為外加電流的陰極保護法。
(1)鋼鐵發生吸氧腐蝕,負極上Fe失電子發生氧化反應,電極反應式為Fe-2e-=Fe2+,正極上氧氣得電子發生還原反應,電極反應式為O2+2H2O+4e-=4OH-。
(2)作原電池負極的金屬加速被腐蝕,作原電池正極的金屬被保護,根據圖知,該裝置是利用原電池原理保護Fe,所以應該選取比Fe活潑的金屬,如鋅。不能選擇鈉,鈉太活潑,直接和水發生反應。
(3)作電解池陽極的金屬加速被腐蝕,作電解池陰極的金屬被保護,根據圖知,該裝置是利用電解池原理保護Fe,則鐵作電解池陰極,應該連接電源負極,故答案為:負。
(4)金屬防護的方法還有在金屬的表面覆蓋保護層、改變金屬內部結構等方法。


 亮點激活精編提優100分大試卷系列答案
亮點激活精編提優100分大試卷系列答案科目:高中化學 來源: 題型:
【題目】由W、X、Y、Z四種金屬按下列裝置進行實驗。下列說法不正確的是
甲 | 乙 | 丙 | |
裝置 |
|
|
|
現象 | 金屬W不斷溶解 | Y 的質量增加 | W上有氣體產生 |
A.裝置甲中W作原電池負極
B.裝置乙中Y電極上的反應式為Cu2++2e=Cu
C.裝置丙中溶液的c(H+)不變
D.四種金屬的活動性強弱順序為Z>W>X>Y
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示為組成人體細胞的主要的元素及其比例。下列相關敘述中,錯誤的是( )

A.圖中所示為細胞鮮重中主要的元素的所占比例
B.因為 O 的含量最多,所以 O 是構成有機物的最基本元素
C.細胞失去大部分水分后,C 的所占比例最大
D.圖中所示的元素在非生物界也可以找到
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下聯氨(N2H4)的水溶液中有:
①N2H4+H2O![]() N2H5++OH- K1
N2H5++OH- K1
②N2H5++H2O![]() N2H62++OH- K2
N2H62++OH- K2
(提示:二元弱堿的電離也是分步電離)
該溶液中的微粒的物質的量分數δ(X)隨-lgc(OH-)變化的關系如圖所示。下列敘述錯誤的是( )
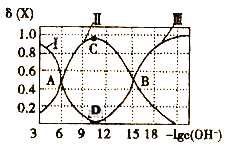
A.據A點可求:K1=10-6
B.D點溶液的c(OH-)=10-l1
C.若C點為N2H5Cl溶液,則存在:c(Cl-)>c(N2H5+)+2c(N2H62+)
D.在N2H5Cl水溶液中,c(N2H4)+c(OH-)=2c(N2H62+)+c(H+)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫常壓下,取下列四種有機物各1mol,分別在足量的氧氣中燃燒,消耗氧氣最多的是
A. C2H5OH B. CH4 C. C2H4O D. C3H8
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知FeSO4·7H2O晶體在加熱條件下發生如下反應:2FeSO4·7H2O![]() Fe2O3+SO2↑+SO3↑+14H2O↑;如圖的裝置可用來檢驗上述反應中所有的氣體產物,請回答下列問題:
Fe2O3+SO2↑+SO3↑+14H2O↑;如圖的裝置可用來檢驗上述反應中所有的氣體產物,請回答下列問題:
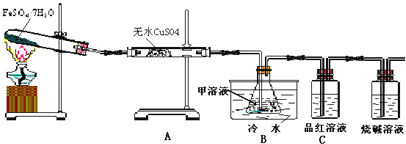
(1)用于檢驗SO2氣體的裝置是______(填裝置的字母),確認水蒸氣存在的現象是______;
(2)利用裝置B可以確認的產物是______,裝置B中的甲溶液可選(填序號)______。
①足量澄清石灰水②足量氯化鋇溶液③足量硝酸鋇溶液
該裝置中冷水的作用是______;
(3)為探究Fe2O3的性質和用途,取試管中少許固體溶于適量鹽酸中制備飽和鐵鹽溶液,將此飽和溶液逐滴加入沸水中加熱片刻,觀察液體的顏色變為______,檢驗該分散系最簡方法的操作為______.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度時,在2L密閉容器中X、Y、Z三種氣態物質的物質的量(n)隨時間(t)變化的曲線如圖所示,由圖中數據
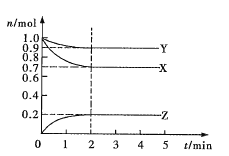
(1)該反應的化學方程式為______________。
(2)反應開始至2min,用Z表示的平均反應速率為_________。
(3)下列敘述能說明上述反應達到化學平衡狀態的是________(填序號)
A.混合氣體的總物質的量不隨時間的變化而變化
B.混合氣體的壓強不隨時間的變化而變化
C.單位時間內每消耗![]() X,同時生成
X,同時生成![]() Z
Z
D.混合氣體的總質量不隨時間的變化而變化
E.混合氣體的密度不再發生改變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向溴水中加入足量乙醛溶液,可以看到溴水褪色。據此對溴水與乙醛發生的有機反應類型進行如下探究,請你完成下列填空:
Ⅰ.猜測:
(1)溴水與乙醛發生取代反應;
(2)溴水與乙醛發生加成反應;
(3)溴水與乙醛發生___反應。
Ⅱ.設計方案并論證:
為探究哪一種猜測正確,某研究性學習小組提出了如下兩種實驗方案:
方案1:檢驗褪色后溶液的酸堿性。
方案2:測定反應前用于溴水制備的Br2的物質的量和反應后Br-離子的物質的量。
(1)方案1是否可行?___?理由是___。
(2)假設測得反應前用于溴水制備的Br2的物質的量為amol,
若測得反應后n(Br-)=___mol,則說明溴水與乙醛發生加成反應;
若測得反應后n(Br-)=___mol,則說明溴水與乙醛發生取代反應;
若測得反應后n(Br-)=___mol,則說明猜測(3)正確。
Ⅲ.實驗驗證:某同學在含0.005molBr2的10mL溶液中,加入足量乙醛溶液使其褪色;再加入過量AgNO3溶液,得到淡黃色沉淀1.88g(已知反應生成有機物與AgNO3不反應)。根據計算結果,推知溴水與乙醛反應的離子方程式為___。
Ⅳ.拓展:
請你設計對照實驗,探究乙醛和乙醇的還原性強弱(填寫下表)。
實驗操作步驟 | 實驗現象 | 結論 |
___ | ___ | ___ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com