
 開心快樂假期作業暑假作業西安出版社系列答案
開心快樂假期作業暑假作業西安出版社系列答案 名題訓練系列答案
名題訓練系列答案科目:高中化學 來源:2012-2013學年重慶市三峽名校聯盟高一下學期期中考試化學試卷(帶解析) 題型:填空題
周期表中前20號幾種元素,其相關信息如下(鈹的原子半徑為0.089nm):
| 元素代號 | A | B | C | D | E |
| 原子半徑/nm | 0.075 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合價 | +5,—3 | +3 | +6,—2 | —1 | —2 |
 2AE2(g)已達到平衡狀態的是 (填代號)
2AE2(g)已達到平衡狀態的是 (填代號)查看答案和解析>>
科目:高中化學 來源:2012-2013學年海南省瓊海市嘉積中學高二下教學質量監測二化學卷(帶解析) 題型:填空題
化學學科中的平衡理論主要包括:化學平衡、電離平衡和水解平衡三種,且均符合勒夏特列原理。請回答下列問題:
Ⅰ、在恒容密閉容器中,發生反應3A(g)+B(g) 2C(g) ΔH=Q kJ/mol。回答下列問題:
2C(g) ΔH=Q kJ/mol。回答下列問題:
(1)寫出該反應平衡常數的表達式__________。
(2)下列各項能作為判斷該反應達到化學平衡狀態的依據是________(填序號)。
① v(A)=3v(B) ②混合氣體的密度保持不變
③有3 mol A消耗的同時有1 mol B生成 ④C的濃度保持不變
(3)根據實驗測得的數據可知,溫度越高該反應的化學平衡常數越大,則Q______0(填“大于”或“小于”)。
Ⅱ、(1)室溫下,取pH=2的鹽酸和醋酸溶液各100 mL,向其中分別加入適量的Zn粒,反應過程中兩溶液的pH變化如圖所示。則圖中表示醋酸溶液中pH變化曲線的是________(填 “a”或“b”)。設鹽酸中加入Zn質量為m1,醋酸溶液中加入的Zn質量為m2,則m1________m2(選填“<”、“=”或“>”)。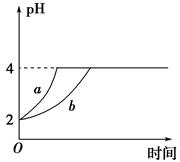
(2)若室溫下pH=2的鹽酸和醋酸溶液各 100 mL,分別加水稀釋后使pH=4,設鹽酸中加入水的體積為V1,醋酸溶液中加入的水的體積為V2,則 V1______V2(填“<”“=”或“>”)。
Ⅲ、常溫下,濃度均為0.1 mol/L 的下列六種溶液的pH如下表:
| 溶質 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
查看答案和解析>>
科目:高中化學 來源:2014屆海南省瓊海市高二下教學質量監測二化學卷(解析版) 題型:填空題
化學學科中的平衡理論主要包括:化學平衡、電離平衡和水解平衡三種,且均符合勒夏特列原理。請回答下列問題:
Ⅰ、在恒容密閉容器中,發生反應3A(g)+B(g) 2C(g) ΔH=Q kJ/mol。回答下列問題:
2C(g) ΔH=Q kJ/mol。回答下列問題:
(1)寫出該反應平衡常數的表達式__________。
(2)下列各項能作為判斷該反應達到化學平衡狀態的依據是________(填序號)。
① v(A)=3v(B) ②混合氣體的密度保持不變
③有3 mol A消耗的同時有1 mol B生成 ④C的濃度保持不變
(3)根據實驗測得的數據可知,溫度越高該反應的化學平衡常數越大,則Q______0(填“大于”或“小于”)。
Ⅱ、(1)室溫下,取pH=2的鹽酸和醋酸溶液各100 mL,向其中分別加入適量的Zn粒,反應過程中兩溶液的pH變化如圖所示。則圖中表示醋酸溶液中pH變化曲線的是________(填 “a”或“b”)。設鹽酸中加入Zn質量為m1,醋酸溶液中加入的Zn質量為m2,則m1________m2(選填“<”、“=”或“>”)。

(2)若室溫下pH=2的鹽酸和醋酸溶液各 100 mL,分別加水稀釋后使pH=4,設鹽酸中加入水的體積為V1,醋酸溶液中加入的水的體積為V2,則 V1______V2(填“<”“=”或“>”)。
Ⅲ、常溫下,濃度均為0.1 mol/L 的下列六種溶液的pH如下表:
|
溶質 |
CH3COONa |
NaHCO3 |
Na2CO3 |
NaClO |
NaCN |
C6H5ONa |
|
pH |
8.8 |
9.7 |
11.6 |
10.3 |
11.1 |
11.3 |
(1)上述鹽溶液中的陰離子,結合H+能力最強的是
(2)根據表中數據判斷,濃度均為0.01 mol/L 的下列五種物質的溶液中,酸性最強的是_______ (填編號) ; 將各溶液分別稀釋100倍, pH變化最小的是 (填編號) 。
A.HCN B.HClO C.C6H5OH D.CH3COOH E.H2CO3
(3)據上表數據,請你判斷下列反應不能成立的是 (填編號)。
A.CH3COOH+ Na2CO3=NaHCO3+CH3COONa
B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+2C6H5 ONa=Na2CO3+2C6H5OH
Ⅳ、已知:ZnCl2·xH2O易溶于水,且其濃的水溶液呈較強酸性;SOCl2 (氯化亞砜)極易和水發生如下反應:SOCl2+H2O=SO2+2HCl。實驗室中制取無水氯化鋅采用ZnCl2·xH2O與SOCl2混合加熱的方法。試回答:
SOCl2的作用是___________________________________。
查看答案和解析>>
科目:高中化學 來源:2015屆重慶市三峽名校聯盟高一下學期期中考試化學試卷(解析版) 題型:填空題
周期表中前20號幾種元素,其相關信息如下(鈹的原子半徑為0.089nm):
元素代號 A B C D E
原子半徑/nm 0.075 0.143 0.102 0.099 0.074
主要化合價 +5,—3 +3 +6,—2 —1 —2
F原子中無中子,G在地殼中含量居第二位,H元素焰色反應呈紫色。
請回答下列問題:
(1)B的原子結構示意圖為 。
(2)F2C和F2E兩種化合物中,沸點較高的是 (填化學式),原因是 。
(3)用電子式表示化合物AF3的形成過程 。
(4)G的單質能與H的最高價氧化物的水化物溶液反應,反應的化學方程式為 。
(5)CE2能使酸性高錳酸鉀溶液褪色(有Mn2+生成),寫出其反應的離子方程式
。
(6)在2L密閉容器中,一定溫度下,能說明反應2AE(g)+E2(g) 2AE2(g)已達到平衡狀態的是 (填代號)
2AE2(g)已達到平衡狀態的是 (填代號)
a. 2V逆(AE)=V正(E2)
b.容器內壓強保持不變
c. 容器內密度保持不變
d. 各組分的物質的量濃度相等
e. 混合氣體的平均相對分子質量不再改變
(7)某同學設計了以G同族的短周期元素的最低價氫化物為燃料的電池,電解質溶液含HEF。 則該電池的負極的電極反應式為 。
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
化學學科中的平衡理論主要包括:化學平衡、電離平衡和水解平衡三種,且均符合勒夏特列原理。請回答下列問題:
Ⅰ、在恒容密閉容器中,發生反應3A(g)+B(g)![]() 2C(g) ΔH=Q kJ/mol。回答下列問題:
2C(g) ΔH=Q kJ/mol。回答下列問題:
(1)寫出該反應平衡常數的表達式__________。
(2)下列各項能作為判斷該反應達到化學平衡狀態的依據是________(填
序號)。
① v(A)=3v(B) ②混合氣體的密度保持不變
③有3 mol A消耗的同時有1 mol B生成 ④C的濃度保持不變
(3)根據實驗測得的數據可知,溫度越高該反應的化學平衡常數越大,則Q______0(填“大于”或“小于”)。
Ⅱ、(1)室溫下,取pH=2的鹽酸和醋酸溶液各100 mL,向其中分別加入適量的Zn粒,反應過程中兩溶液的pH變化如圖所示。則圖中表示醋酸溶液中pH變化曲線的是________(填“a”或“b”)。設鹽酸中加入Zn質量為m1,醋酸溶液中加入的Zn質量為m2,則m1________m2(選填“<”、“=”或“>”)。


(2)若室溫下pH=2的鹽酸和醋酸溶液各 100 mL,分別加水稀釋后使pH=4,設鹽酸中加入水的體積為V1,醋酸溶液中加入的水的體積為V2,則 V1______V2(填“<”“=”或“>”)。
Ⅲ、常溫下,濃度均為0.1 mol/L 的下列六種溶液的pH如下表:
| 溶質 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
(1)上述鹽溶液中的陰離子,結合H+能力最強的是
(2)根據表中數據判斷,濃度均為0.01 mol/L 的下列五種物質的溶液中,酸性最強的是_______ (填編號) ; 將各溶液分別稀釋100倍, pH變化最小的是 (填編號) 。
A.HCN B.HClO C.C6H5OH D.CH3COOH E.H2CO3
(3)據上表數據,請你判斷下列反應不能成立的是 (填編號)。
A.CH3COOH+ Na2CO3=NaHCO3+CH3COONa
B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+2C6H5ONa=Na2CO3+2C6H5OH
Ⅳ、已知:ZnCl2·xH2O易溶于水,且其濃的水溶液呈較強酸性;SOCl2 (氯化亞砜)極易和水發生如下反應:SOCl2+H2O=SO2+2HCl。實驗室中制取無水氯化鋅采用ZnCl2·xH2O與SOCl2混合加熱的方法。試回答:
SOCl2的作用是___________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com