
【題目】按題目要求填寫下列空白。
(1) ![]() 按官能團的不同分類,有機物類型為________類。
按官能團的不同分類,有機物類型為________類。
(2)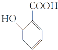 中官能團的名稱是________________。
中官能團的名稱是________________。
(3)鍵線式![]() 表示的有機物的結構簡式是____________。
表示的有機物的結構簡式是____________。
(4)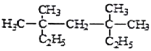 系統命名法為_________________。
系統命名法為_________________。
系統命名法命名有機物時應注意的問題_______ 、 _______(至少寫兩點)
【答案】酯 羧基、羥基 CH3CH=C(CH3)CH=CHCH3 3,3,5,5-四甲基庚烷 選主鏈時需要選取最長的碳鏈,如果是烯烴,需要選取含有碳碳雙鍵的最長碳鏈為主鏈 編號時需要從離支鏈最近一端開始編號,如果是烯烴,則需要從離碳碳雙鍵最近的一端開始編號
【解析】
(1)![]() 是甲酸甲酯;
是甲酸甲酯;
(2) 中官能團有—OH和—COOH;
中官能團有—OH和—COOH;
(3)![]() 中含有2個碳碳雙鍵,端點和拐點均為碳原子,據此書寫其結構簡式;
中含有2個碳碳雙鍵,端點和拐點均為碳原子,據此書寫其結構簡式;
(4) 為烷烴,最長碳鏈含有7個C,主鏈為庚烷,結合烷烴的命名方法命名;
為烷烴,最長碳鏈含有7個C,主鏈為庚烷,結合烷烴的命名方法命名;
系統命名法命名有機物時應注意的問題有:主鏈選擇是否最長,編號是否正確,編號之和是否最小等,據此解答。
(1)![]() 含有酯基,是甲酸甲酯,屬于酯,故答案為:酯;
含有酯基,是甲酸甲酯,屬于酯,故答案為:酯;
(2) 中官能團有—OH為羥基,—COOH為羧基,故答案為:羧基、羥基;
中官能團有—OH為羥基,—COOH為羧基,故答案為:羧基、羥基;
(3)![]() 中含有2個碳碳雙鍵,其結構簡式為:CH3CH=C(CH3)CH=CHCH3,故答案為:CH3CH=C(CH3)CH=CHCH3;
中含有2個碳碳雙鍵,其結構簡式為:CH3CH=C(CH3)CH=CHCH3,故答案為:CH3CH=C(CH3)CH=CHCH3;
(4) 為烷烴,最長碳鏈含有7個C,主鏈為庚烷,編號從右邊開始,在3號、5號C各含有2個甲基,其名稱為:3,3,5,5-四甲基庚烷,故答案為:3,3,5,5-四甲基庚烷;
為烷烴,最長碳鏈含有7個C,主鏈為庚烷,編號從右邊開始,在3號、5號C各含有2個甲基,其名稱為:3,3,5,5-四甲基庚烷,故答案為:3,3,5,5-四甲基庚烷;
系統命名法命名有機物時應注意的問題有:選主鏈時需要選取最長的碳鏈,如果是烯烴等,需要選取含有碳碳雙鍵的最長碳鏈為主鏈;編號時需要從離支鏈最近一端開始編號,如果是烯烴,則需要從離碳碳雙鍵最近的一端開始編號,等等,故答案為:選主鏈時需要選取最長的碳鏈,如果是烯烴,需要選取含有碳碳雙鍵的最長碳鏈為主鏈;編號時需要從離支鏈最近一端開始編號,如果是烯烴,則需要從離碳碳雙鍵最近的一端開始編號。


 周周清檢測系列答案
周周清檢測系列答案 輕巧奪冠周測月考直通高考系列答案
輕巧奪冠周測月考直通高考系列答案科目:高中化學 來源: 題型:
【題目】利用硫酸渣(主要含![]() 、FeO,雜質為
、FeO,雜質為![]() 和
和![]() 等)生產鐵基顏料鐵黃(FeOOH)的制備流程如下:
等)生產鐵基顏料鐵黃(FeOOH)的制備流程如下:

(1)FeOOH中Fe元素的化合價為____。
(2)“酸溶”時,所選擇的硫酸為溶質質量分數49%,密度![]() ,該硫酸物質的量濃度是___
,該硫酸物質的量濃度是___![]() ,
,![]() 反應的離子方程式為____。
反應的離子方程式為____。
(3)濾渣Ⅰ的主要成分是![]() 和___(填化學式);
和___(填化學式);![]() 被
被![]() 還原的離子方程式為_____。
還原的離子方程式為_____。
(4)“氧化”中,需檢驗溶液中的離子是否氧化完全,所選用的試劑是____。
(5)濾液Ⅱ中溶質是___(填化學式);洗滌固體的操作是_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】我國科學家研制了一種新型的高比能量鋅—碘溴液流電池,其工作原理如圖所示。圖中貯液器可儲存電解質溶液,提高電池的容量。下列敘述不正確的是( )

A. 放電時,a電極反應為I2Br-+2e-=2I-+Br-
B. 充電時,b電極每增重0.65g,溶液中有0.01mol I-被氧化
C. 放電時,溶液中離子的數目增大
D. 充電時,a電極接外電源正極
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某學習小組通過查閱資料發現用KClO3和濃鹽酸也可以制備氯氣。為此該小組利用如圖裝置在實驗室制取Cl2并探究其有關性質:
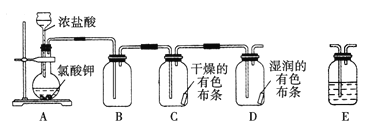
(1)裝置A中存在一處錯誤,改正這處錯誤:______________。
(2)配平裝置A中發生反應的化學方程式:____KClO3+____HCl(濃)=__KCl+___Cl2↑+___H2O,此反應中氧化產物與還原產物的物質的量之比為 ____________。請用單線橋標出該反應電子轉移的方向和數目 ____________________。
(3)為了除去氯氣中的氯化氫,需要在裝置A、B之間添加裝置E,裝置E中所盛裝的試劑為____。為了探究使有色布條褪色的是氯氣還是氯氣與水反應的生成物,需要在整套裝置中添加裝置E,其中加入濃硫酸,裝置E在整套裝置中的添加位置為____(選填序號)。
a.A、B之間 b.B、C之間 c.C、D之間 d.D之后
(4)將氯氣通入冷的石灰乳中,即可制得以______________(填化學式)為有效成分的漂白粉,發生反應的化學方程式為__________________________。
(5)另外一個學習小組就環境保護方面指出了上述裝置的缺陷并給出了改進措施。該改進措施是____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氮化鎂![]() 是一種重要的化學試劑。某化學興趣小組擬制備氮化鎂并測定產品純度。
是一種重要的化學試劑。某化學興趣小組擬制備氮化鎂并測定產品純度。
已知:①氮化鎂極易與水反應;②實驗室在加熱條件下用飽和![]() 溶液和飽和
溶液和飽和![]() 溶液混合制備
溶液混合制備![]() ;③焦性沒食子酸溶液用于吸收少量
;③焦性沒食子酸溶液用于吸收少量![]() 。
。
Ⅰ.制備氮化鎂。
他們選擇下列裝置設計實驗(裝置可重復使用):
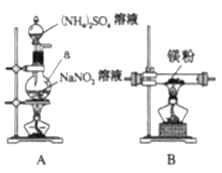
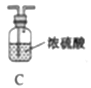

(1)儀器a的名稱是____,氮化鎂的電子式是____。
(2)氣體從左至右,裝置連接順序為____。(填代號)
(3)寫出A中發生反應的化學方程式:____。
(4)用化學方法檢驗產品中含有氮化鎂![]() ,設計實驗方案:____。
,設計實驗方案:____。
Ⅱ.測定產品純度。
利用如圖裝置測定氮化鎂產品純度(雜質不產生氣體,氨氣不溶于煤油)。

(5)當產品與蒸餾水完全反應后,冷卻至室溫、調平液面、讀數。調平液面的操作是__。
(6)取產品質量為wg,開始量氣管讀數為![]() ,最終量氣管讀數為
,最終量氣管讀數為![]() (折合成標準狀況),則該樣品純度為____(用代數式表示)。如果開始俯視刻度線,終點時仰視刻度線,則測得結果___(填“偏高”“偏低”或“無影響”)。
(折合成標準狀況),則該樣品純度為____(用代數式表示)。如果開始俯視刻度線,終點時仰視刻度線,則測得結果___(填“偏高”“偏低”或“無影響”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室用固體Na2CO3配制90mL 0.200 mol·L-1的Na2CO3溶液,回答下列問題:
(1)通過計算得出可用天平稱取Na2CO3固體________g。
(2)若要實施配制,除天平、燒杯、玻璃棒外,還需的玻璃儀器有 _______ ,______。
(3)溶解過程中,玻璃棒的作用是__________________。
(4)配制完畢后,教師指出有四位同學進行了下列某一項錯誤操作,你認為這四項錯誤操作中會導致所得溶液濃度偏低的是____(填選項字母)。
a.定容時俯視容量瓶刻度線
b.轉移時未洗滌燒杯和玻璃棒
c.容量瓶使用時未干燥
d.定容后,把容量瓶倒置搖勻后發現液面低于刻度線,便補充幾滴水至刻度線
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】歷史上被稱為“世界八大公害”和“20 世紀十大環境公害”之一的洛杉磯光化學煙霧事件使 人們深刻認識到了汽車尾氣的危害性。汽車尾氣中氮氧化物和碳氫化合物受紫外線作用可產 生二次污染物光化學煙霧,其中某些反應過程如圖所示。下列說法不正確的是( )
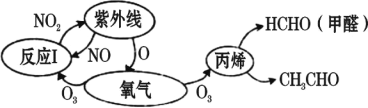
A.煙霧是一種固溶膠,其分散劑是空氣B.O2 和 O3 是氧的兩種同素異形體
C.反應 I 屬于氧化還原反應D.NO2 不是酸性氧化物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】“84 消毒液”能有效殺滅甲型 H1N1 病毒,某同學購買了一瓶“威露士”牌“84 消毒液”,該消毒液通常稀釋 100 倍(體積比)使用。查閱相關資料和消毒液包裝說明得到 如下信息:
① ②NaClO = Na++ClO-
②NaClO = Na++ClO-
(1)該“84 消毒液”的物質的量濃度約為_____(保留 1 位小數)。
(2)某同學取 100mL 該“84 消毒液”,按要求稀釋后用于消毒,稀釋后的溶液中c(Na+)=_____mol·L1。
(3)該同學參閱該“84 消毒液”的配方,欲用 NaClO 固體配制 480mL 含 NaClO 質量分數為25%的消毒液。下列說法不正確的是____________(填字母)。
A.如下圖所示的儀器中,有三種是不需要的,還另需要一種玻璃儀器
B.將稱量好的 NaClO 固體在燒杯中溶解后應立即轉入容量瓶
C.定容時俯視容量瓶刻度線會導致所配溶液濃度偏高
D.需要稱量 NaClO 固體的質量為 149.0g
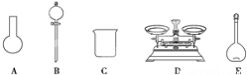
(4)該同學對容量瓶及其使用方法的認識中正確的是_____(填字母)。
A.容量瓶上標有容積、溫度和濃度 B.使用前要檢查容量瓶是否漏液 C.容量瓶用蒸餾水洗凈后,須烘干后再使用 D.配制溶液過程中,容量瓶內液體只需要一次搖勻過程
(5)一瓶上述“威露士”牌“84 消毒液”能吸收空氣中_____L 的 CO2(標準狀況)而變質。(已 知:CO2+NaClO+H2O=NaHCO3+HClO)
(6)“84 消毒液”與稀硫酸混合使用可增強消毒能力,某消毒小組人員用18.4 mol·L-1 的濃 硫酸配制 500 mL2.3 molL﹣1 的稀硫酸用于增強“84 消毒液”的消毒能力,需取用濃硫酸的體 積為______________mL。
(7)在配制過程中,下列操作中能使所配溶液的濃度偏高的有_____(填代號)。
①用量筒量取 98%的硫酸時俯視
②洗滌量取濃硫酸的量筒,并將洗滌液轉移到容量瓶中
③未等稀釋后的 H2SO4 溶液冷卻至室溫就轉移到容量瓶中
④轉移前,容量瓶中含有少量蒸餾水
⑤定容時,加蒸餾水超過標線,又用膠頭滴管吸出
⑥定容搖勻后,發現液面低于標線,又用膠頭滴管加蒸餾水至標線
⑦定容時,仰視刻度線
(8)現有密度為 d g/mL 濃度為 18 mol/L 的濃硫酸溶液 100 g ,需要加入一定量的水將其 稀釋為濃度是 9 mol/L,則加入水的體積是_____(填字母)
A.大于 100 mL B.小于 l00 mL C.等于 100 mL
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有一混合物的水溶液,可能含有以下離子中的幾種:![]() 、
、![]() 、
、![]() 、
、![]() 現取三份各100mL溶液進行如下實驗:第一份加入
現取三份各100mL溶液進行如下實驗:第一份加入![]() 溶液有沉淀A產生:第二份加足量NaOH溶液加熱后,收集到0.08ml氣體B;第三份加足量
溶液有沉淀A產生:第二份加足量NaOH溶液加熱后,收集到0.08ml氣體B;第三份加足量![]() 溶液后,得到干燥沉淀C 12.54g,經足量鹽酸洗滌干燥后,沉淀質量為4.66g
溶液后,得到干燥沉淀C 12.54g,經足量鹽酸洗滌干燥后,沉淀質量為4.66g
請回答以下問題
(1) 沉淀C的成分是_________,其物質的量分別是_____________
(2) 寫出產生氣體B的離子方程式 ____________________
(3) 該混合液中可能含的離子有___________,一定含有的陽離子有_________其物質的量分別是_____________一定沒有的離子是_________________
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com