
【題目】如圖是M、N兩種主族元素的原子結構示意圖,下列說法正確的是( )
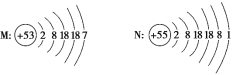
A.M位于第五周期Ⅶ族
B.N位于IA族,該主族中的元素又稱為堿金屬元素
C.N在空氣中燃燒,生成化學式為N2O的氧化物
D.M所在的主族中各元素是同周期元素中非金屬性最強的元素
 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
【題目】某化學課外興趣小組為驗證鹵素單質氧化性的相對強弱,用如圖所示裝置進行實驗(夾持儀器已略去,氣密性已檢驗)。
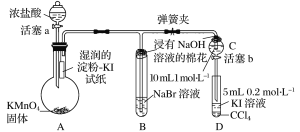
實驗過程:
Ⅰ.打開彈簧夾,打開活塞a,滴加濃鹽酸。
Ⅱ.當B和C中的溶液都變為黃色時,夾緊彈簧夾。
Ⅲ.當B中溶液由黃色變為紅棕色時,關閉活塞a。
Ⅳ. ……
(1)盛放濃鹽酸的儀器名稱為____________________。
(2)在燒瓶內發生反應時,體現濃鹽酸的性質為__________________。
(3)驗證氯氣的氧化性強于碘的實驗現象是__________________________。
(4)B中溶液發生反應的離子方程式是____________________________。
(5)浸有NaOH溶液的棉花的作用為______________________________。
(6)為驗證溴的氧化性強于碘,過程Ⅳ的操作步驟和現象是______________。
(7)過程Ⅲ實驗的目的是________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】三效催化劑是最為常見的汽車尾氣催化劑,其催化劑表面物質轉化的關系如圖所示,下列說法正確的 ( )
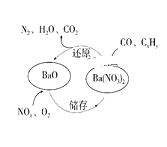
A.在轉化過程中,氮元素均被還原
B.依據圖示判斷催化劑不參與儲存和還原過程
C.還原過程中生成0.1mol N2,轉移電子數為0.5 NA
D.三效催化劑能有效實現汽車尾氣中CO、CxHy、NOx三種成分的凈化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于晶體的說法正確的組合是( )
①分子晶體中都存在共價鍵
②在晶體中只要有陽離子就一定有陰離子
③金剛石、SiC、H2O、H2S晶體的熔點依次降低
④離子化合物中只有離子鍵沒有共價鍵,分子晶體中肯定沒有離子鍵
⑤CaTiO3晶體中(晶胞結構如圖所示)每個Ti4+和12個O2-相緊鄰
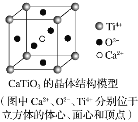
⑥SiO2晶體中每個硅原子與兩個氧原子以共價鍵相結合
⑦晶體中分子間作用力越大,分子越穩定
⑧氯化鈉溶于水時離子鍵被破壞
A. ①②③⑥B. ①②④C. ③⑤⑦D. ③⑤⑧
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鈹及其化合物的應用正日益被重視。
(1)最重要的含鈹礦物是綠柱石,含2%鉻(Cr)的綠柱石即為祖母綠。基態Cr原子價電子的排布圖為_______。
(2)鈹與相鄰主族的鋁元素性質相似。下列有關鈹和鋁的敘述正確的有_____(填字母)。
A.都屬于p區主族元素 B.電負性都比鎂大
C.第一電離能都比鎂大 D.氯化物的水溶液pH均小于7
(3)鈹、鋁晶體都是由金屬原子密置層在三維空間堆積而成(最密堆積)。鈹的熔點(1551K)比鋁的熔點(930K)高,原因是____。
(4)氯化鈹在氣態時存在BeCl2分子(a)和二聚分子(BeCl2)2(b),固態時則具有如下圖所示的鏈狀結構(c)。
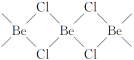
①a屬于____(填“極性”或“非極性”)分子。
②二聚分子(BeCl2)2中Be原子的雜化方式相同,且所有原子都在同一平面上。b的結構式為____(標出配位鍵)。
(5)Al單質的晶體中原子的堆積方式如圖乙所示,其晶胞特征如圖丙所示,原子之間相互位置關系的平面圖如圖丁所:
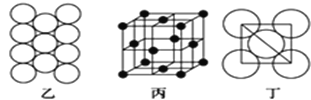
若已知Al的原子半徑為d,NA代表阿伏加德羅常數,Al的相對原子質量為M,則一個晶胞中Al原子的數目為___個;Al晶體的密度為_____(用字母表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硒(Se)和銅(Cu)在生產生活中有廣泛的應用。硒可以用作光敏材料、電解錳行業的催化劑,也是動物體必需的營養元素和對植物有益的營養元素等。氯化亞銅(CuCl)廣泛應用于化工、印染、電鍍等行業。CuCl難溶于醇和水,可溶于氯離子濃度較大的體系,在潮濕空氣中易水解氧化。以海綿銅(主要成分是Cu和少量CuO)為原料,采用硝酸銨氧化分解技術生產CuCl的工藝過程如下所示:
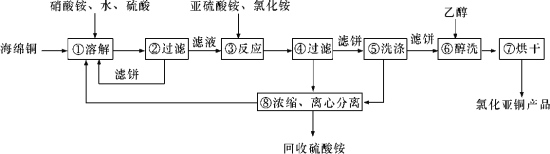
請回答下列問題:
(1)若步驟①中得到的氧化產物只有一種,則它的化學式是____________。
(2)寫出步驟③中主要反應的離子方程式:_________。
(3)步驟⑤包括用pH=2的溶液酸洗、水洗兩步操作,酸洗采用的酸是_______(寫酸的名稱)。
(4)上述工藝中,步驟⑥和⑦的作用是__________。
(5)Se為ⅥA族元素,用乙二胺四乙酸銅陰離子水溶液和硒代硫酸鈉(Na2SeSO3)溶液反應可獲得納米硒化銅,硒代硫酸鈉還可用于Se的精制,寫出硒代硫酸鈉(Na2SeSO3)與H2SO4溶液反應得到精硒的化學方程式:______________。
(6)氯化亞銅產率與溫度、溶液pH關系如下圖所示。據圖分析,流程化生產氯化亞銅的過程中,溫度過低影響CuCl產率的原因是_________;溫度過高、pH過大也會影響CuCl產率的原因是____________。
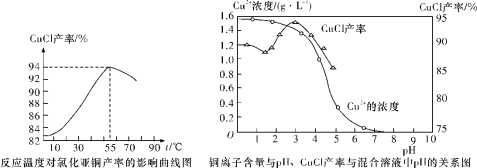
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關化學反應速率、化學反應限度的說法中,正確的是( )
A.反應C(s)+H2O(g)![]() CO(g)+H2(g),增加碳的用量可加快反應速率
CO(g)+H2(g),增加碳的用量可加快反應速率
B.用鐵片與稀硫酸反應制H2,改用 98%的濃硫酸可加快生成H2的速率
C.反應2SO2(g)+O2(g)![]() 2SO3(g)在密閉容器中進行,壓縮容器體積,反應速率增大
2SO3(g)在密閉容器中進行,壓縮容器體積,反應速率增大
D.可逆反應達到化學平衡狀態時,正、逆反應的速率相等且都為0
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫代硫酸鈉(Na2S2O3)可用作分析試劑、基準試劑、還原劑、除氯劑等。
Ⅰ、實驗室制備硫代硫酸鈉裝置圖如下。

(1)儀器B的名稱是________。
(2)寫出裝置B制備Na2S2O3的化學反應方程式____________________________。
(3)NaOH溶液的作用是____________________________________。
Ⅱ、測硫代硫酸鈉樣品純度步驟如下
①稱取Ⅰ中制得硫代硫酸鈉樣品8.0g配成250mL溶液
②從①中量取20.00mL溶液于錐形瓶中
③用0.lmol·L-1標準碘液滴定,實驗測得數據如下
滴定前讀數(mL) | 滴定后讀數(mL) | 待測液體積(mL) | |
實驗一 | 1.20 | 21.00 | 20.00 |
實驗二 | 0.40 | 19.20 | 20.00 |
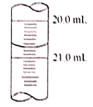
實驗三 | 0.50 | x | 20.00 |
(4)該滴定時,向錐形瓶中加入1至2滴淀粉液作指示劑,則達到滴定終點的判斷標準是______________。
(5)x讀數如圖所示,則x=________,根據所測的數據計算該硫代硫酸鈉樣品純度為_______________。(已知I2+2Na2S2O3=2NaI+Na2S4O6)
(6)若步驟①中量取20.00mL硫代硫酸鈉溶液時,未用硫代硫酸鈉溶液潤洗滴定管,則測得樣品的純度將______________(填“偏大”或“偏小”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】依據圖中氮元素及其化合物的轉化關系,回答問題:
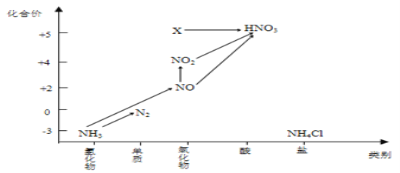
(1)該圖利用“______和核心元素的_____是研究物質性質的兩個重要角度”建立。
(2)實驗室常用NH4Cl與Ca(OH)2制取氨氣,該反應的化學方程式為________。
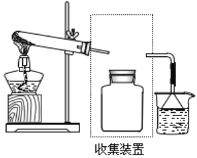
(3)若要收集一瓶氨氣,請在橫線上把圖虛框內連接裝置圖不全的部分畫出。_____
![]()
(4)工業上以NH3、空氣、水為原料生產硝酸的工藝流程簡圖如圖所示:
![]()
寫出NH3→NO的化學方程式__________________________________。
(5)圖中,X的化學式為_______,將X轉化為HNO3屬于______________反應(填“氧化還原”或“非氧化還原”)反應。
(6)若要將NH3→N2,從原理上看,下列試劑可行的是________(填序號)。
A.O2 B.Na C.NH4Cl D.NO2
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com