
對于1 mol CO和1 mol N2,下列說法不正確的是()
A.它們所含的分子數相同
B.它們的體積一定相等
C.它們的質量一定相同
D.它們所含的質子數和電子數都相等
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:閱讀理解
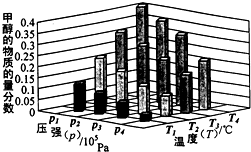 能源是制約國家發展進程的因素之一.甲醇、二甲醚等被稱為2 1世紀的綠色能源,工業上利用天然氣為主要原料與二氧化碳、水蒸氣在一定條件下制備合成氣(CO、H2),再制成甲醇、二甲醚.
能源是制約國家發展進程的因素之一.甲醇、二甲醚等被稱為2 1世紀的綠色能源,工業上利用天然氣為主要原料與二氧化碳、水蒸氣在一定條件下制備合成氣(CO、H2),再制成甲醇、二甲醚.查看答案和解析>>
科目:高中化學 來源: 題型:
A.它們所含的分子數相同
B.它們的體積一定相等
C.它們的質量一定相同
D.它們所含的質子數和電子數都相等
查看答案和解析>>
科目:高中化學 來源: 題型:
(12分)工業上一般可采用如下反應來合成甲醇:
CO(g)+2H2(g)CH3OH(g) ΔH =-akJ·mol-1
(1)上圖是該反應在不同溫度下CO的轉化率隨時間變化的曲線。
① a __0(填“>” “<” “=”)。
② 下列說法正確的是_ _(填序號)。
a.1 molCO(g) 和2 mol H2(g) 所具有的能量小于1 mol CH3OH(g) 所具有的能量
b.將1 molCO(g) 和2 mol H2(g) 置于一密閉容器中充分反應后放出a KJ的熱量
c.升高溫度,平衡向逆反應移動,上述熱化學方程式中的a值將減小
d.如將一定量CO(g) 和H2(g)置于某密閉容器中充分反應后放熱a KJ,則此過程中有1 mol CO(g) 被還原
(2)在一定條件下,科學家利用從煙道氣中分離出CO2與太陽能電池電解水產生的H2合成甲醇,其過程如下圖所示:
① 該合成路線對于環境保護的價值在于_ _。
② 15%~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱堿性,上述合成線路中用作CO2
吸收劑。用離子方程式表示乙醇胺水溶液呈弱堿性的原因:
。
(3)甲醇燃料電池的工作原理如下左圖所示。該電池工作時,c口通入的物質發生的電極
反應式為:_ _。
(4)以上述電池做電源,用上右圖所示裝置,在實驗室中模擬鋁制品表面“鈍化”處理的過程中,發現溶液逐漸變渾濁,原因是(用相關的電極反應式和離子方程式表示):
_ 。
查看答案和解析>>
科目:高中化學 來源:2013屆四川省成都市高二5月月考化學試卷(解析版) 題型:填空題
(12分)工業上一般可采用如下反應來合成甲醇:
CO(g)+2H2(g) CH3OH(g)
ΔH =-a
kJ·mol-1
CH3OH(g)
ΔH =-a
kJ·mol-1

(1)上圖是該反應在不同溫度下CO的轉化率隨時間變化的曲線。
① a __0(填“>” “<” “=”)。
② 下列說法正確的是_ _(填序號)。
a.1 mol CO(g) 和2 mol H2(g) 所具有的能量小于1 mol CH3OH(g) 所具有的能量
b.將1 mol CO(g) 和2 mol H2(g) 置于一密閉容器中充分反應后放出a KJ的熱量
c.升高溫度,平衡向逆反應移動,上述熱化學方程式中的a值將減小
d.如將一定量CO(g) 和H2(g) 置于某密閉容器中充分反應后放熱a KJ,則此過程中有1 mol CO(g) 被還原
(2)在一定條件下,科學家利用從煙道氣中分離出CO2與太陽能電池電解水產生的H2合成甲醇,其過程如下圖所示:

① 該合成路線對于環境保護的價值在于_ _。
② 15%~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱堿性,上述合成線路中用作CO2
吸收劑。用離子方程式表示乙醇胺水溶液呈弱堿性的原因:
。
(3)甲醇燃料電池的工作原理如下左圖所示。該電池工作時,c口通入的物質發生的電極
反應式為:_ _。

(4)以上述電池做電源,用上右圖所示裝置,在實驗室中模擬鋁制品表面“鈍化”處理的過程中,發現溶液逐漸變渾濁,原因是(用相關的電極反應式和離子方程式表示):
_ 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com