
(1)圖所示裝置為化學實驗中常見的儀器,它除了用于洗氣外,還有其他用途。![]() 學科網
學科網
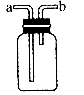
![]() 學科網
學科網
①醫院給病人輸氧時往往在氧氣罐與病人呼吸器之間安裝盛水的該裝置,通過觀察氣泡產生情況以便調節供氧速率,此時氧氣從 口導入。![]() 學科網
學科網
②實驗室用![]() 和濃HCl制
和濃HCl制![]() 實驗中,將生成的
實驗中,將生成的![]() 通入NaOH溶液之前,先將
通入NaOH溶液之前,先將![]() 從該裝置 管進,從 管導出,此時該裝置起的作用是防止NaOH倒流。
從該裝置 管進,從 管導出,此時該裝置起的作用是防止NaOH倒流。![]() 學科網
學科網
③當用此裝置收集NO時,需采取什么措施?![]() 學科網
學科網
(2)被稱為“魔棒”的熒光棒已成為節日之夜青少年的喜愛之物,其發光原理是利用過氧化氫氧化草酸酯產生能量,該能量被傳遞給熒光物質后便發出熒光。回答下列問題:![]() 學科網
學科網
①有人說,發光的魔棒不能湊近石油氣之類的可燃性氣體,否則會導致爆炸,是否正確?說明理由。![]() 學科網
學科網
②通過擠壓,使過氧化氫與革酸酯混合反應,導致魔棒發光,一段時間后,光的亮度降低,此時,把魔棒往手心上敲打幾下,亮度會重新增大,原因是什么?(提示:草酸酯是一種有較高黏度的有機化合物)![]() 學科網
學科網
③在設計魔棒時,其連續發光的能力在8~12h,如果在發光中途,把它放人冰箱的冷凍室中,發光便會停止或基本停止。把魔棒從冷凍室中取出靜止一會兒,它又會連續發光,原因是什么?![]() 學科網
學科網
 開心蛙狀元測試卷系列答案
開心蛙狀元測試卷系列答案科目:高中化學 來源: 題型:閱讀理解

| x |
| y |
| x |
| y |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解

| ||
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:
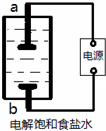 某興趣小組模擬氯堿工業生產原理并探究其產品的性質.已知文獻記載:
某興趣小組模擬氯堿工業生產原理并探究其產品的性質.已知文獻記載:查看答案和解析>>
科目:高中化學 來源: 題型:
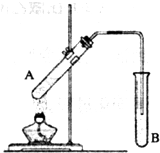 實驗室用右圖所示裝置制取乙酸乙酯.
實驗室用右圖所示裝置制取乙酸乙酯.查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com