
【題目】“溫室效應”是全球關注的環境問題之一。CO2是目前大氣中含量最高的一種溫室氣體,CO2的綜合利用是解決溫室及能源問題的有效途徑。
(1)CO2催化加氫能合成低碳烯烴:2CO2(g)+6H2(g)![]() C2H4(g)+4H2O(g)。不同溫度下平衡時的四種氣態物質的物質的量如圖所示,則曲線b表示的物質為________(填化學式)。
C2H4(g)+4H2O(g)。不同溫度下平衡時的四種氣態物質的物質的量如圖所示,則曲線b表示的物質為________(填化學式)。

(2)CO2和H2在催化劑Cu/ZnO作用下可發生兩個平行反應,分別生成CH3OH和CO。
反應A:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
反應B:CO2(g)+H2(g)![]() CO(g)+H2O(g)
CO(g)+H2O(g)
控制CO2和H2初始投料比為1∶3時,溫度對CO2平衡轉化率及甲醇和CO產率的影響如圖所示。

①由圖可知溫度升高CO的產率上升,其主要原因可能是_____。
②由圖可知獲取CH3OH最適宜的溫度是________,下列措施有利于提高CO2轉化為CH3OH的平衡轉化率的有________(填字母)。
A. 使用催化劑
B. 增大體系壓強
C. 增大CO2和H2的初始投料比
D. 投料比和容器體積不變,增加反應物的濃度
(3)在恒溫恒容條件下,反應A達到平衡的標志有_____
A. 容器中氣體壓強不再發生變化
B. 容器中氣體密度不再發生變化
C. 容器中氣體顏色不再發生變化
D. 容器中氣體平均摩爾質量不再發生變化
(4)由CO2制取C的太陽能工藝如圖所示。“熱分解系統”發生的反應為2Fe3O4![]() 6FeO+O2↑,每分解1 mol Fe3O4轉移電子的物質的量為_____;“重整系統”發生反應的化學方程式為___。
6FeO+O2↑,每分解1 mol Fe3O4轉移電子的物質的量為_____;“重整系統”發生反應的化學方程式為___。

【答案】H2O 反應B正反應是吸熱反應,溫度升高平衡正向移動,CO產率升高 250 ℃ BD AD 2 mol 6FeO+CO2![]() 2Fe3O4+C
2Fe3O4+C
【解析】
(1)據圖,升高溫度,氫氣物質的量增大,平衡逆向移動,則正反應是放熱反應,a曲線隨著溫度升高,物質的量增大,為二氧化碳,b、c隨著溫度升高其物質的量降低,為生成物水、乙烯,但水的變化量大于乙烯,據此判斷b曲線代表物質;
(2)①反應B正反應是吸熱反應,溫度升高平衡正向移動,CO產率升高;
②據圖示進行分析250℃甲醇轉化率最高;由CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)△H1=-53.7kJ·mol-1 可知提高CO2轉化為CH3OH平衡轉化率,應使平衡向正向移動,可降低溫度,增大濃度;
CH3OH(g)+H2O(g)△H1=-53.7kJ·mol-1 可知提高CO2轉化為CH3OH平衡轉化率,應使平衡向正向移動,可降低溫度,增大濃度;
(3)可逆反應達到平衡狀態時,正逆反應速率相等,反應體系中各物質的物質的量、物質的量濃度、百分含量及由此引起的一系列物理量不變;
(4)該反應中Fe元素化合價由+3價變為+2價,O元素化合價由-2價變為0價,根據轉移電子和Fe3O4之間的關系式計算;據圖,反應物是二氧化碳和FeO,生成物的四氧化三鐵和C,反應條件是700K.
(1)據圖,升高溫度,氫氣物質的量增大,平衡逆向移動,則正反應是放熱反應,a曲線隨著溫度升高,物質的量增大,為二氧化碳,b、c隨著溫度升高其物質的量降低,為生成物水、乙烯,但水的變化量大于乙烯,所以b曲線代表H2O。
(2)①由圖2可知溫度升高CO的產率上升,其主要原因可能是反應B正反應是吸熱反應,溫度升高平衡正向移動,CO產率升高;
②據圖示進行分析250℃甲醇轉化率最高,故獲取CH3OH最適宜的溫度是250℃;
A.使用催化劑,平衡不移動,不能提高轉化率,故A錯誤;
B、增大體系壓強,平衡向正方向移動,提高甲醇轉化率,故B正確;
C、增大CO2和H2的初始投料比,可增大氫氣的轉化率,二氧化碳的轉化率減小,故C錯誤;
D、投料比不變,增加反應物的濃度,平衡正向移動,可增大轉化率,故D正確;
故選BD。
(3)反應A:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
A. 容器中氣體壓強不再發生變化,各物質百分含量保持不變時,正逆反應速率相等,該反應達到平衡狀態,故A正確;
B. 反應前后氣體總質量不變、容器容積不變,則無論反應是否達到平衡狀態,容器中混合氣體密度始終不變,所以當容器中混合氣體的密度保持不變時,該反應不一定達到平衡狀態,故B錯誤;
C. 反應A中,氣體均為無色,容器中氣體顏色不再發生變化,無法判斷是否達到平衡,故C錯誤;
D. 反應前后氣體總質量不變、但反應前后氣體的物質的量發生變化,容器中氣體平均摩爾質量不再發生變化,各物質百分含量保持不變時,正逆反應速率相等,該反應達到平衡狀態,故D正確;
故選AD。
(4)該反應中Fe元素化合價由+3價變為+2價,O元素化合價由-2價變為0價,分解2mol四氧化三鐵轉移4mol電子,則分解1mol四氧化三鐵轉移2mol電子;
據圖,反應物是二氧化碳和FeO,生成物的四氧化三鐵和C,反應條件是700K,反應方程式為6FeO(S)+CO2![]() 2Fe3O4+C。
2Fe3O4+C。


 名校通行證有效作業系列答案
名校通行證有效作業系列答案科目:高中化學 來源: 題型:
【題目】現有一定量含有Na2O雜質的Na2O2試樣。請從下圖中選用適當的實驗裝置,設計一個最簡單的實驗,測定Na2O2試樣的純度(可供選用的反應物只有CaCO3固體,稀鹽酸和蒸餾水)。請填寫下列空白:

(1)寫出在實驗中Na2O2和Na2O分別發生反應的化學方程式_________________________,_________________
(2)應選用的裝置是(只要求寫出圖中裝置的標號)_______________________
(3)所選用裝置的連接順序應是(填各接口的字母;連接膠管省略)________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】大氣與生態圈的氮循環如圖所示,下列敘述不正確的是

A. ④維持大氣中氮元素含量穩定
B. ①是野生植物生長所需氮元素的重要來源
C. ⑤為硝化過程、④為反硝化過程,都是氮元素的還原反應過程
D. ②是氮肥工業基礎,科學家努力將固氮變化條件趨近生物固氮
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學用某種粗鹽進行提純實驗,步驟見下圖.

請回答:
(1)步驟①和②的操作名稱是________.
(2)步驟③判斷加入鹽酸“適量”的方法是_____;
步驟④加熱蒸發時要用玻璃棒不斷攪拌,這是為了防止___________,當蒸發皿中有較多量固體出現時,應___________,用余熱使水分蒸干.
(3)猜想和驗證:
猜想 | 驗證的方法 | 現象 | 結論 |
猜想Ⅰ:固體A中含 CaCO3、MgCO3 | 取少量固體A于試管中,滴加稀鹽酸,并用涂有澄清石灰水的小燒杯罩于試管口 | _____ | 猜想Ⅰ成立 |
猜想Ⅱ:固體A中含 BaCO3 | 取少量固體A于試管中,先滴入________,再滴入Na2SO4溶液 | 有氣泡放出,無白色沉淀 | ______ |
猜想Ⅲ:最后制得的NaCl晶體中還含有Na2SO4 | 取少量NaCl晶體溶于試管中的蒸餾水,________ | _____ | 猜想Ⅲ成立 |
請寫出猜想Ⅲ驗證過程中發生的化學反應方程式_____
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A—J都是初中化學常用的物質。其中B、E、H、J是單質,其余均為化合物,氣體C可用于滅火。它們相互間的轉化關系如下圖所示(部分反應物、生成物及反應條件已略去)。

請回答下列問題:
⑴寫出物質D、J的化學式:D___________,J___________。
⑵“氣體C→B”的轉化過程,在自然界中稱為____________作用。
⑶反應①的反應條件___________,其基本反應類型___________。
⑷寫出反應②的化學方程式:______________________。
⑸若要實現“H+I→紅色固體J”的轉化,物質I必須滿足的條件是___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一恒溫、恒容密閉容器中發生反應:Ni(s)+4CO(g)![]() Ni(CO)4(g),△H<0。利用該反應可以將粗鎳轉化為純度達99.9%的高純鎳。對該反應的說法正確的是
Ni(CO)4(g),△H<0。利用該反應可以將粗鎳轉化為純度達99.9%的高純鎳。對該反應的說法正確的是
A. 增加Ni的量可提高CO的轉化率,Ni的轉化率降低
B. 縮小容器容積,平衡右移,△H減小
C. 反應達到平衡后,充入CO再次達到平衡時,CO的體積分數降低
D. 當4v[Ni(CO)4]=v(CO)時或容器中混合氣體密度不變時,都可說明反應已達化學平衡狀態
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數的值,下列說法正確的是
A. 14gCO和N2的混合氣體所含有的電子數為14NA
B. 用濃鹽酸分別和MnO2、KClO3反應制備1mol氯氣,轉移的電子數均為2NA
C. 1.0L2.0 mol/ LNaOH溶液中含有氧原子數為2NA
D. 1moI NH4NO3溶于稀氨水中使溶液呈中性,溶液中NH4+數目為NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列事實中,能說明氯的非金屬性比硫強的是( )
A.次氯酸(HClO)的酸性比硫酸強
B.次氯酸的氧化性比稀硫酸強
C.氯化氫比硫化氫的熱穩定性好
D.最外層電子數氯原子的比硫原子的多
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】欲用含有少量氯化鈣的氯化鈉固體,配制100 mL a mol/L的氯化鈉溶液,設計了下面的操作方案。根據方案操作步驟回答下列問題:
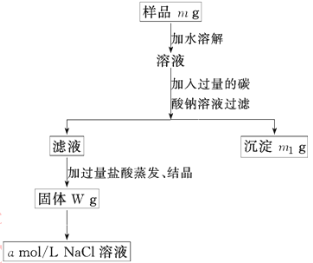
(1)稱量粗鹽樣品m g,在托盤天平左盤上放_____,右盤上放_____。
(2)過濾時,漏斗下端管口應_____,漏斗里液面應_______。
(3)蒸發操作時應將液體放在___中加熱,等加熱至____時即停止加熱。
(4)在樣品的溶液中加入過量的Na2CO3溶液,作用是_______,反應的化學方程式是_______。
(5)在濾液中加入鹽酸的作用是_______,反應的化學方程式是_____。
(6)配制80 mL a mol/L的NaCl溶液時,應從W g固體中稱取NaCl的質量為_____,配制時應在____中進行定容。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com