
(14分)
Ⅰ、實驗室常用以下方法制取氯氣:MnO2+ 4HCl(濃) 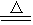 MnCl2+Cl2↑ + 2H2O,
MnCl2+Cl2↑ + 2H2O,
(1)用雙線橋標出電子轉(zhuǎn)移方向和數(shù)目。(在答題紙上標)
(2)在標準狀況下生成的Cl2為11.2L時,參加反應的HCl的物質(zhì)的量為 ,
被氧化HCl的質(zhì)量為 。
Ⅱ、科學家發(fā)現(xiàn),食用蝦類等水生甲殼類動物的同時服用維生素C容易中毒。這是因為
對人體無害的+5價砷類化合物在維生素C的作用下,能夠轉(zhuǎn)化為有毒的+3價的含砷化
合物。通過以上信息填空:
(1)維生素C具有 (填氧化性或還原性)。
(2)上述過程中+5價砷類物質(zhì)作為 (填氧化劑或還原劑),+5價砷元素發(fā)生
反應(填氧化或還原);2mol +5價砷完全轉(zhuǎn)化為 +3價砷,共轉(zhuǎn)移 個
電子(用NA表示阿伏加德羅常數(shù))。
(每空2分,共14分)
Ⅰ、(1) (2)2mol,36.5g。
(2)2mol,36.5g。
Ⅱ、(1) 還原性 (2)氧化劑 ; 還原 ;4NA
解析試題分析:Ⅰ、(1)根據(jù)反應的方程式可知,鹽酸中氯元素的化合價從-1價升高到0價,失去1個電子。而二氧化錳中Mn元素的化合價從+4價降低到+2價,得到2個電子,所以根據(jù)電子到得失守恒可知,正確的表示應該是 。
。
(2)氯氣的物質(zhì)的量是11.2L÷22.4L/mol=0.5mol,則根據(jù)反應的化學方程式可知,參加反應的氯化氫是0.5mol×4=2mol。其中被氧化的氯化氫是1mol,質(zhì)量是36.5g。
Ⅱ、(1)+5價砷類化合物在維生素C的作用下,能夠轉(zhuǎn)化為有毒的+3價的含砷化,這說明砷元素得到電子,所以維生素C失去電子,具有還原性。
(2)As元素的化合價從+5價降低到+3價,得到2個電子,做氧化劑,則+5價砷元素發(fā)生還原反應。2mol +5價砷完全轉(zhuǎn)化為 +3價砷,得到4mol電子,則共轉(zhuǎn)移4NA個電子。
考點:考查氧化還原反應的表示、計算以及有關判斷
點評:該題是基礎性試題的考查,也是高考中的常見考點,難度不大。試題放熱關鍵是熟練掌握氧化還原反應的有關概念,判斷的依據(jù),然后再結(jié)合題意靈活分析即可。該題有利于培養(yǎng)學生分析問題、解決問題的能力。


科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
Ⅰ.玻璃棒是中學化學實驗室中常用的儀器。下列實驗過程中,一般不需要用玻璃棒的是
(填寫編號)
①用pH試紙測定Na2CO3溶液的pH ②配制一定物質(zhì)的量濃度的氯化鈉溶液 ③將適量氯化鐵飽和溶液滴入沸水中制備氫氧化鐵膠體 ④探究Ba(OH)2![]() 8H20晶體和NH4Cl晶體反應過程中的能量變化 ⑤用蒸餾法分離兩種沸點差距較大的液體 ⑥過濾分離互不相溶的固體和液體 ⑦用已知濃度的鹽酸滴定待測濃度的NaOH溶液的酸堿中和滴定過程 ⑧稀釋濃H2SO4的過程
8H20晶體和NH4Cl晶體反應過程中的能量變化 ⑤用蒸餾法分離兩種沸點差距較大的液體 ⑥過濾分離互不相溶的固體和液體 ⑦用已知濃度的鹽酸滴定待測濃度的NaOH溶液的酸堿中和滴定過程 ⑧稀釋濃H2SO4的過程
Ⅱ.為測定某含有雜質(zhì)Na2O的Na2O2樣品的純度,某小組同學分別設計了如下方案。
【方案一】準確稱量樣品mg,與水充分反應后將溶液的體積稀釋為VmL,從中取出V1mL溶液,裝入錐形瓶,用已知濃度的鹽酸進行滴定,以確定溶液的濃度,再計算出樣品中Na2O2的含量。
⑴此方案中,酸堿中和滴定時應選用 滴定管。
⑵寫出此方案中涉及到的反應的離子方程式 。
【方案二】準確稱量樣品mg,將樣品與二氧化碳充分反應,通過測定反應產(chǎn)生氧氣的體積,計算出樣品中Na2O2的含量。
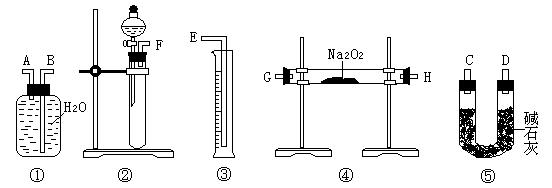
⑶該方案的實驗過程中,儀器的連接順序是 (填儀器下方序號),①中的進氣口為 (填“A”或“B”)
⑷裝置⑤的作用是 。
⑸你認為方案一、方案二中測定結(jié)果比較準確的是 。
查看答案和解析>>
科目:高中化學 來源: 題型:
(14分)
Ⅰ.玻璃棒是中學化學實驗室中常用的儀器。下列實驗過程中,一般不需要用玻璃棒的是
(填寫編號)
①用pH試紙測定Na2CO3溶液的pH ②配制一定物質(zhì)的量濃度的氯化鈉溶液③將適量氯化鐵飽和溶液滴入沸水中制備氫氧化鐵膠體④探究Ba(OH)2![]() 8H20晶體和NH4Cl晶體反應過程中的能量變化 ⑤用蒸餾法分離兩種沸點差距較大的液體 ⑥過濾分離互不相溶的固體和液體⑦用已知濃度的鹽酸滴定待測濃度的NaOH溶液的酸堿中和滴定過程 ⑧稀釋濃H2SO4的過程
8H20晶體和NH4Cl晶體反應過程中的能量變化 ⑤用蒸餾法分離兩種沸點差距較大的液體 ⑥過濾分離互不相溶的固體和液體⑦用已知濃度的鹽酸滴定待測濃度的NaOH溶液的酸堿中和滴定過程 ⑧稀釋濃H2SO4的過程
Ⅱ.為測定某含有雜質(zhì)Na2O的Na2O2樣品的純度,某小組同學分別設計了如下方案。
【方案一】準確稱量樣品mg,與水充分反應后將溶液的體積稀釋為VmL,從中取出V1mL溶液,裝入錐形瓶,用已知濃度的鹽酸進行滴定,以確定溶液的濃度,再計算出樣品中Na2O2的含量。
⑴此方案中,酸堿中和滴定時應選用 滴定管。
⑵寫出此方案中涉及到的反應的離子方程式 。
【方案二】準確稱量樣品mg,將樣品與二氧化碳充分反應,通過測定反應產(chǎn)生氧氣的體積,計算出樣品中Na2O2的含量。
⑶該方案的實驗過程中,儀器的連接順序是 (填儀器下方序號),①中的進氣口為 (填“A”或“B”)
⑷裝置⑤的作用是 。
⑸你認為方案一、方案二中測定結(jié)果比較準確的是 。
查看答案和解析>>
科目:高中化學 來源:遼寧省撫順市六校聯(lián)合體2009—2010學年度高三二模(理綜)試題化學部分 題型:實驗題
(14分)
Ⅰ.玻璃棒是中學化學實驗室中常用的儀器。下列實驗過程中,一般不需要用玻璃棒的是
(填寫編號)
①用pH試紙測定Na2CO3溶液的pH ②配制一定物質(zhì)的量濃度的氯化鈉溶液③將適量氯化鐵飽和溶液滴入沸水中制備氫氧化鐵膠體④探究Ba(OH)2 8H20晶體和NH4Cl晶體反應過程中的能量變化⑤用蒸餾法分離兩種沸點差距較大的液體⑥過濾分離互不相溶的固體和液體⑦用已知濃度的鹽酸滴定待測濃度的NaOH溶液的酸堿中和滴定過程⑧稀釋濃H2SO4的過程
8H20晶體和NH4Cl晶體反應過程中的能量變化⑤用蒸餾法分離兩種沸點差距較大的液體⑥過濾分離互不相溶的固體和液體⑦用已知濃度的鹽酸滴定待測濃度的NaOH溶液的酸堿中和滴定過程⑧稀釋濃H2SO4的過程
Ⅱ.為測定某含有雜質(zhì)Na2O的Na2O2樣品的純度,某小組同學分別設計了如下方案。
【方案一】準確稱量樣品mg,與水充分反應后將溶液的體積稀釋為VmL,從中取出V1mL溶液,裝入錐形瓶,用已知濃度的鹽酸進行滴定,以確定溶液的濃度,再計算出樣品中Na2O2的含量。
⑴此方案中,酸堿中和滴定時應選用 滴定管。
⑵寫出此方案中涉及到的反應的離子方程式 。
【方案二】準確稱量樣品mg,將樣品與二氧化碳充分反應,通過測定反應產(chǎn)生氧氣的體積,計算出樣品中Na2O2的含量。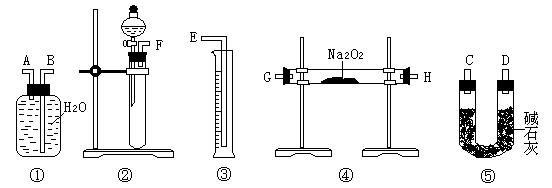
⑶該方案的實驗過程中,儀器的連接順序是 (填儀器下方序號),①中的進氣口為 (填“A”或“B”)
⑷裝置⑤的作用是 。
⑸你認為方案一、方案二中測定結(jié)果比較準確的是 。
查看答案和解析>>
科目:高中化學 來源:遼寧省撫順市六校聯(lián)合體2009-2010學年度高三二模(理綜)試題化學部分 題型:實驗題
(14分)
Ⅰ.玻璃棒是中學化學實驗室中常用的儀器。下列實驗過程中,一般不需要用玻璃棒的是
(填寫編號)
①用pH試紙測定Na2CO3溶液的pH ②配制一定物質(zhì)的量濃度的氯化鈉溶液
③將適量氯化鐵飽和溶液滴入沸水中制備氫氧化鐵膠體
④探究Ba(OH)2 8H20晶體和NH4Cl晶體反應過程中的能量變化 ⑤用蒸餾法分離兩種沸點差距較大的液體 ⑥過濾分離互不相溶的固體和液體
⑦用已知濃度的鹽酸滴定待測濃度的NaOH溶液的酸堿中和滴定過程 ⑧稀釋濃H2SO4的過程
8H20晶體和NH4Cl晶體反應過程中的能量變化 ⑤用蒸餾法分離兩種沸點差距較大的液體 ⑥過濾分離互不相溶的固體和液體
⑦用已知濃度的鹽酸滴定待測濃度的NaOH溶液的酸堿中和滴定過程 ⑧稀釋濃H2SO4的過程
Ⅱ.為測定某含有雜質(zhì)Na2O的Na2O2樣品的純度,某小組同學分別設計了如下方案。
【方案一】準確稱量樣品mg,與水充分反應后將溶液的體積稀釋為VmL,從中取出V1mL溶液,裝入錐形瓶,用已知濃度的鹽酸進行滴定,以確定溶液的濃度,再計算出樣品中Na2O2的含量。
⑴此方案中,酸堿中和滴定時應選用 滴定管。
⑵寫出此方案中涉及到的反應的離子方程式 。
【方案二】準確稱量樣品mg,將樣品與二氧化碳充分反應,通過測定反應產(chǎn)生氧氣的體積,計算出樣品中Na2O2的含量。
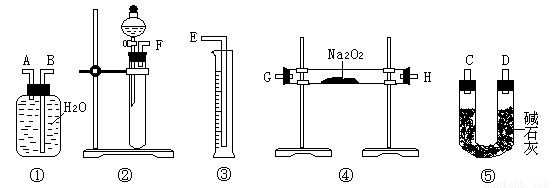
⑶該方案的實驗過程中,儀器的連接順序是 (填儀器下方序號),①中的進氣口為 (填“A”或“B”)
⑷裝置⑤的作用是 。
⑸你認為方案一、方案二中測定結(jié)果比較準確的是 。
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com