
| A、5.6g | B、8.4g | C、2.8g | D、16.8g |
| 2mol/L×0.1L |
| 2 |
| 3 |
| 2 |


科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解

| 實驗操作 | 預期現象與結論 |
| 步驟1:取適量“吸收液”于小燒杯中,用膠頭滴管取1mol/L BaCl2溶液向小燒杯滴加直至過量. | 若出現白色渾濁,則溶液中存在SO32-或 SO42-. |
| 步驟2:將小燒杯中的濁液過濾、洗滌,再用適量水把附在濾紙上的固體沖入另一小燒杯中;向沖下的固體 滴入1滴(或少量)品紅 滴入1滴(或少量)品紅 再滴入過量2mol/L鹽酸,振蕩 再滴入過量2mol/L鹽酸,振蕩 . |
若品紅褪色(或有氣泡),則“吸收液”中存在 SO32-. 若品紅褪色(或有氣泡),則“吸收液”中存在 SO32-. 若品紅不褪色(或無有氣泡),則“吸收液”中不存在 SO32- 若品紅不褪色(或無有氣泡),則“吸收液”中不存在 SO32- |
| 步驟3: 用試管取適量濾液 用試管取適量濾液 向其中滴入過量的1mol/LBa(OH)2溶液[或滴入1滴(或少量)品紅溶液,再滴入2-3滴(或過量)的2mol/L鹽酸],振蕩 向其中滴入過量的1mol/LBa(OH)2溶液[或滴入1滴(或少量)品紅溶液,再滴入2-3滴(或過量)的2mol/L鹽酸],振蕩 . |
若出現白色沉淀(或品紅溶液褪色,或有氣泡),則“吸收液”中存在 HSO3-. 若出現白色沉淀(或品紅溶液褪色,或有氣泡),則“吸收液”中存在 HSO3-. 若不出現白色沉淀(或品紅溶液不褪色,或沒有氣泡),則“吸收液”中不存在 HSO3-. 若不出現白色沉淀(或品紅溶液不褪色,或沒有氣泡),則“吸收液”中不存在 HSO3-. |
查看答案和解析>>
科目:高中化學 來源: 題型:
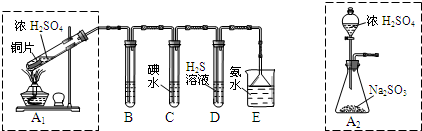
2- 3 |
2- 4 |
- 3 |
2- 3 |
- 3 |
| 實驗操作 | 預期現象與結論 | ||||
| 步驟1:取適量“吸收液”于小燒杯中,用膠頭滴管取1mol/L BaCl2溶液向小燒杯滴加直至過量. | 若出現白色渾濁,則溶液中存在 SO
| ||||
| 步驟2:將小燒杯中的濁液過濾、洗滌,再用適量水把附在濾紙上的固體沖入另一小燒杯中;向沖下的固體 |
|||||
| 步驟3: |
查看答案和解析>>
科目:高中化學 來源: 題型:
現有2mol/L鹽酸和硫酸溶液各100mL,分別加入等量的鐵粉,反應結束后,所生成的氫氣質量比為23,則往酸中加入的鐵粉的質量為
A.2.8g B.5.6g C.8.4g D.16.8g
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com