
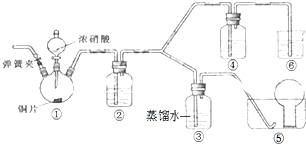
 某學習小組探究濃、稀硝酸氧化性的相對強弱,按如圖裝置進行實驗(夾持儀器已略去).實驗表明濃硝酸能將NO氧化成NO2,而稀硝酸不能氧化NO.由此得出的結論是濃硝酸的氧化性強于稀硝酸.
某學習小組探究濃、稀硝酸氧化性的相對強弱,按如圖裝置進行實驗(夾持儀器已略去).實驗表明濃硝酸能將NO氧化成NO2,而稀硝酸不能氧化NO.由此得出的結論是濃硝酸的氧化性強于稀硝酸.分析 驗證濃硝酸的氧化性,應首先檢查裝置的氣密性,硝酸與銅發生反應生成二氧化氮,通入水后生成一氧化氮,然后通過濃硝酸,如無色氣體生成紅棕色氣體,可證明硝酸具有氧化性,可氧化一氧化氮,生成的氣體不能直接排放到空氣中,應有尾氣處理裝置,以此解答該題.
(1)結合實驗目,根據裝置特點分析各裝置的作用,再根據物質的性質的判斷,裝置③、④、⑥中盛放的藥品依次是3mol/L稀硝酸、濃硝酸、氫氧化鈉溶液;
(2)NO易與氧氣反應生成二氧化氮,裝置中殘存的空氣能氧化NO而對實驗產生干擾;
(3)裝置①中銅與濃硝酸反應生成硝酸銅、二氧化氮與水;
(4)進入裝置②中的氣體為二氧化氮,二氧化氮與水反應生成硝酸與NO;
(5)根據對比實驗③、④的實驗現象判斷;
(6)根據是否改變溶液中硝酸銅的質量分數或溶解氣體的濃度判斷.
解答 解:(1)根據裝置特點和實驗目的,裝置⑤是收集NO,裝置⑥中盛放NaOH溶液吸收NO2防止污染大氣;因為要驗證稀HNO3不能氧化NO,所以裝置③中應該盛放稀硝酸.
故答案為:3mol/L稀硝酸、濃硝酸、氫氧化鈉溶液;
(2)由于裝置中殘存的空氣,能氧化NO而對實驗產生干擾,所以滴加濃HNO3之前需要通入一段時間CO2趕走裝置中的空氣,
故答案為:排出體系中的空氣,防止NO被氧化成NO2;
(3)裝置①中Cu與濃HNO3反應生成Cu(NO3)2、NO2、H2O,反應方程式為Cu+4HNO3(濃)=Cu(NO3)2+2NO2↑+2H2O,離子反應為:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O,
故答案為:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O;
(4)裝置①中反應生成了二氧化氮,在裝置②中二氧化氮會與水反應,即3NO2+H2O=2HNO3+NO,所以裝置②的作用是將NO2轉化為NO,
故答案為:將NO2轉化為NO;3NO2+H2O=2HNO3+NO;
(5)NO通過稀HNO3溶液后,若無紅棕色NO2產生,說明稀HNO3不能氧化NO,所以盛放稀HNO3裝置的液面上方沒有顏色變化即可說明之.裝置④中盛放的是濃HNO3,若濃HNO3能氧化NO則裝置④液面的上方會產生紅棕色氣體,
故答案為:裝置③中液面上方氣體仍為無色,裝置④中液面上方氣體由無色變為紅棕色;
(6)要證明是Cu(NO3)2濃度過低或是溶解了NO2導致裝置①中溶液呈綠色,一是可設計將溶解的NO2趕走,再觀察顏色變化,a、c方案符合;二是增加或稀釋溶液中Cu(NO3)2溶液的濃度,觀察反應后的顏色變化,bd方案符合.
故選:ab c d.
點評 本題主要考查HNO3的性質、屬物質驗證性實驗設計,利用對比的方法判斷硝酸的性質.結合已知的物質具有的性質,選擇合適的試劑,設計具體實驗方案驗證物質是否具有該性質.對有毒氣體要設計尾氣處理裝置,防止污染環境.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 實驗 序號 | 溫度℃ | 初始CCl4濃度 (mol•L-1) | 初始H2濃度(mol•L-1) | CCl4的平衡轉化率 |
| 1 | 110 | 1 | 1.2 | A |
| 2 | 110 | 1 | 1 | 50% |
| 3 | 100 | 1 | 1 | B |

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 沸點/℃ | 水溶性 | |
| 甲醇 | 65 | 混溶 |
| 甲醛 | -21 | 混溶 |

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 碳酸鈉一過氧化氫加合物(aNa2CO3•bH2O2)具有漂白、殺菌作用.實驗室用“醇析法”制備該物質的實驗步驟如下:
碳酸鈉一過氧化氫加合物(aNa2CO3•bH2O2)具有漂白、殺菌作用.實驗室用“醇析法”制備該物質的實驗步驟如下:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 500 mL 1 mol/L的HNO3溶液 | B. | 1 L 0.5 mol/L的Fe(NO3)3溶液 | ||
| C. | 100 mL 0.5 mol/L的Mg(NO3)2溶液 | D. | 300 mL 1 mol/L的Mg(NO3)2溶液 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com